Canker and decline caused by Neofusiccocum parvum on Acacia melanoxylon in Italy
Forest@ - Journal of Silviculture and Forest Ecology, Volume 13, Pages 41-46 (2016)
doi: https://doi.org/10.3832/efor2041-013
Published: Oct 14, 2016 - Copyright © 2016 SISEF
Research Articles
Abstract
In the spring of 2012, in reforested areas of Peloritani Mountains (Sicily, Italy) a severe dieback of Acacia melanoxylon R. Brown was observed. The main symptoms on both young and adults plants consisted of elongated cankers on the trunks and epicormic shoots, wilt of the canopy and dieback interested mostly aged trees. The woody tissues showed browning beyond the cankers. Sapwood and heartwood appeared decayed with a brown to gray-greenish discoloration. One fungal species was consistently isolated from infected woody tissues, which was morphologically attributed to Neofusiccocum sp. The sequencing of the ITS regions of a representative isolate allowed to identify (99% similarity) the species Neofusiccocum parvum (Pennycook & Samuels) Crous, Slippers and Phillips, teleomorph Botryosphaeria parva Pennycook & Samuels. The pathogenicity tests have reproduced symptoms similar to those observed in the field. N. parvum is the aetiologic agent of mortality of australian blackwood observed in Sicily and to our knowledge this is the first report of this fungus on Acacia melanoxylon. It is a generalist pathogen, cosmopolitan, present in many temperate areas, Mediterranean and subtropical. The older Peloritani Mountains populations of australian blackwood seem particularly susceptible to the pathogen, the latter favored by the lack of silvicultural interventions that generate interspecific and intraspecific competition, as well as the increase and spread of the fungus. To minimize the consequential damage is necessary to adopt sanitation measures that would lower the fungal inoculum and program substitutions of this exotic species with others that have multiple functions suited to environments (e.g., Chestnut) or encouraging the establishment and development of native species, such as the holm oak and shrub.
Keywords
Australian Blackwood, Cankers, Botryosphaeriaceae, Italy, Sapwood
Introduzione
Acacia melanoxylon R. Brown è una specie esotica appartenente alla famiglia delle Mimosaceae. Essa è originaria dell’Australia orientale, da dove per le sue molteplici peculiaritàè stata diffusa in vaste aree a clima tropicale e sub-tropicale, trovando una maggiore diffusione in Nuova Zelanda, Brasile, India, Sudafrica e, su minori estensioni, in Tanzania, Etiopia, Zimbabwe, Madagascar, Mauritius e Ruanda e in alcuni Paesi del bacino del Mediterraneo. In Italia, l’acacia dal legno nero è stata impiegata in rimboschimenti nelle regioni Liguria, Toscana, Lazio, Sicilia e Sardegna. La specie può raggiungere 15-20 m in altezza ed è caratterizzata da un legno duro, compatto, nero con sfumature verdastre ([1]). Le caratteristiche del legno conferiscono ad A. melanoxylon una buona capacità nel rallentare l’avanzata degli incendi. Questa peculiarità, la spiccata capacità pollonifera e la rapidità di crescita hanno creato, negli anni ’50-’60 del secolo scorso, i presupposti per un suo impiego in ampi programmi di rimboschimento finalizzati a costituire filari antincendio e, come specie accessoria al pino domestico e al pino marittimo, per ricoprire in tempi brevi le estese superfici denudate dei versanti ionici e tirrenici dei Monti Peloritani (ME). Questi impianti sono stati realizzati su pendii collinari, situati a circa 500- 600 m s.l.m., costituiti prevalentemente da suoli di arenaria facilmente disgregabili o asportabili dalle acque piovane e caratterizzati da elevati indici di piovosità.
Nei demani forestali regionali di Sant’Anna-Celle e di S. Leone-Pantani, Comune di Messina, a partire dal 2012, è stata osservata una diffusa moria di polloni e alberi adulti di A. melanoxylon riconducibile ad infezioni di origine fungina. Allo scopo di descrivere il quadro sintomatico, raccogliere campioni vegetali per l’isolamento e la successiva identificazione e caratterizzazione in laboratorio dell’agente causale della malattia, sono stati effettuati sopralluoghi in diversi periodi dell’anno nei rimboschimenti coinvolti. Sono stati, inoltre, condotti saggi di patogenicità in vivo su semenzali per la verifica dei postulati di Koch.
Materiali e metodi
Isolamento e identificazione del fungo associato alla malattia
Gli isolamenti sono stati effettuati trasferendo in piastre Petri, contenenti agar-patata-destrosio (PDA, pH 5.6), frammenti di tessuto infetto prelevati da campioni di piante giovani e adulte sintomatiche, raccolti in differenti periodi dell’anno. Le piastre Petri sono state poste ad incubare in termostato a 22 ± 1 °C al buio, e trascorsi 2-3 giorni dai tessuti è emerso frequentemente micelio fungino di colore bianco. Le colonie sono state trasferite in coltura pura su PDA (Potato Dextrose Agar) e mantenute a 24 ± 1° C in termostato a luce diffusa. Al fine di identificare il fungo a livello specifico è stata effettuata l’analisi delle regioni ITS (Internal Transcribed Spacer) del DNA ribosomale, estraendo il DNA da una coltura di 7 giorni di età di un isolato rappresentativo. L’estrazione di DNA dall’isolato fungino è avvenuta tramite il metodo hyphal tipping ([11]). Questo metodo ha previsto la raccolta di alcuni apici ifali in 100 μl di acqua sterile, seguita da successivi shock termici in azoto liquido, passaggi in termoblocco a 70°C e omogeneizzazione tramite uso del Vortex. L’estratto di DNA ottenuto è stato sottoposto ad analisi molecolare PCR con i primer universali per funghi ITS1f (5’-CTTGGTCATTTAGAGGAAGTAA-3’) e ITS 4 (5’-TCCTCCGCTTATTGATATGC-3’ ’Â’ [16]). La reazione di amplificazione (PCR) è stata effettuata in un volume di 25 μl contenente 1X di tampone PCR, 0.2 mM di nucleotidi trifosfati (dNTPs), 0.5 μM di ciascun primer, 0.025 U μl-1 di Taq polymerasi (Promega, USA) e 6.25 μl di estratto di DNA. I parametri della reazione hanno previsto una fase di denaturazione iniziale a 94 °C per 5 minuti, 35 cicli comprendenti una fase di denaturazione a 94 °C per 45 secondi, una di ibridazione a 60 °C per 45 secondi, una di allungamento a 72 °C per 45 secondi, ed infine una fase di allungamento a 72 °C per 7 minuti. Il prodotto amplificato della PCR è stato purificato per via enzimatica tramite l’aggiunta di 2 μl di ExoSAP-IT (Affimetrix) e successivamente incubato per 15 minuti a 37 °C e 15 minuti a 80 °C. Il sequenziamento in entrambe le direzioni del prodotto amplificato (con i primer ITS1f/ITS4) è avvenuto presso la BMR Genomics S.R.L. (Padova). Il confronto della sequenza consenso ottenuta contro quelle presenti nel database Genbank (NCBI) è avvenuto tramite analisi BLASTn.
Prove di patogenicità
La patogenicità degli isolati ottenuti in vitro è stata verificata su semenzali di acacia dal legno nero di due anni di età allevati in vaso, regolarmente irrigati. Le inoculazioni sono state eseguite praticando un’incisione con un bisturi a lama sterile ed inserendo, sotto la corteccia del fusto, tasselli di micelio di 3-5 mm2, prelevato al margine di una colonia di 7 giorni di età accresciutasi su PDA. Dieci piantine di A. melanoxylon sono state inoculate all’altezza di 25 cm dal colletto. Il punto di inoculazione è stato ricoperto con un batuffolo di cotone idrofilo imbevuto di acqua sterile e successivamente sigillato con Parafilm® per evitarne la rapida disidratazione. Le piante testimoni (n = 5) sono state trattate allo stesso modo, inserendo però tassellini di agar sterile. Le piante sono state inoculate nella prima decade di maggio 2013 e collocate in ambiente esterno per tutto il periodo della prova che ha avuto una durata complessiva di 16 mesi. I sintomi sono stati monitorati ogni settimana nei primi due mesi e ogni 30 giorni nel restante periodo di prova.
Risultati
Sintomatologia
I sintomi osservati consistevano in arrossamenti e disseccamenti sparsi della chioma e morie diffuse di polloni e piante adulte di 30-50 anni. Sul tronco erano visibili la corteccia sollevata o del tutto assente, lesioni e spaccature che evolvevano in vistosi cancri allungati (Fig. 1), a direzione basipeta, dai quali nel periodo di maggiore piovosità colava un essudato rossastro. I tessuti legnosi presentavano imbrunimenti e necrosi, a sviluppo prevalentemente longitudinale, che si estendevano oltre la lunghezza dei cancri. In sezione trasversale, porzioni più o meno estese dell’alburno e del cilindro centrale mostravano una colorazione variabile dal marrone al grigio-verdastro e carie che aveva origine in corrispondenza della necrosi corticale esterna (Fig. 2). Quando i tessuti legnosi venivano colonizzati per intero, la parte sovrastante il cancro si presentava disseccata e si sviluppavano rametti epicormici al di sotto delle lesioni. Sulla corteccia necrotizzata di vecchi cancri, specialmente al confine tra parte infetta e parte sana, erano visibili picnidi globosi, singoli o aggregati, di colore nero, erompenti dallo strato sottocorticale.
Fig. 1 - Cancro allungato e necrosi corticale su fusto di acacia dal legno nero causato da N. parvum.
Identificazione della specie fungina associata alla malattia
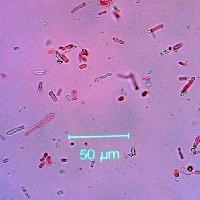
Dopo 2-3 giorni di incubazione tutte le colture mostravano micelio aereo e compatto, a sviluppo circolare, di colore bianco virante prima al verde-chiaro e poi al verde-scuro olivaceo, rispettivamente, dopo circa 7 e 14 giorni di crescita. Dopo 20-25 giorni sono stati osservati corpi fruttiferi globosi di colore nero. Le osservazioni al microscopio ottico condotte sui picnidi rilevati in natura e su quelli ottenuti in laboratorio hanno evidenziato la presenza di conidi privi di setti, ialini, fusoidali, con apice arrotondato e base tronca, misuranti in media 15.5-21 × 4.5-6.5 μm. Successivamente, essi diventavano uno-due settati e la cellula centrale assumevano una colorazione marrone scuro. Sulla base delle caratteristiche morfo-colturali, le colonie fungine isolate sono state associate al genere Neofusiccocum. L’analisi BLAST della sequenza consenso ha mostrato una similarità nucleotidica del 99% con una sequenza di Neofusiccocum parvum (Pennycook & Samuels) Crous, Slippers & Phillips (isolato ALG6 da vite in Algeria - accessione no.: KJ657701.1) e con altre sequenze ITS di isolati del genere Neofusiccocum depositate in GenBank. La sequenza è stata depositata presso l’European Nucleotide Archive - EMBL (numero di accessione LN832409) e resa pubblica dal 3 maggio 2015. Il teleomorfo della specie fungina isolata è Botryosphaeria parva Pennycook & Samuels.
Prove di patogenicità
Dopo due-tre settimane dall’inoculazione, i semenzali mostravano l’appiattimento, l’imbrunimento e la necrosi della corteccia e del legno sottostante e l’emissione di rametti epicormici. Sulle piantine, dopo 2 mesi, si sono sviluppati cancri allungati mentre la colonizzazione della corteccia si estendeva, in media, 10 - 12 cm con andamento prevalentemente basipeto (in media 3.5/5 - 6.5/7 cm, rispettivamente, verso l’alto e verso il basso). Alla fine della prova, la metà dei semenzali erano morti mentre gli altri presentavano disseccamenti diffusi, cancri estesi, l’imbrunimento e la necrosi di gran parte dell’alburno e della zona cambiale. Le piantine di controllo mostravano la completa cicatrizzazione delle ferite. I reisolamenti effettuati dall’alburno delle piantine inoculate hanno dato esito positivo mentre quelli delle piante di controllo sono stati negativi.
Discussione
Le caratteristiche morfologiche delle colonie fungine isolate, le strutture riproduttive osservate in natura e in laboratorio, l’analisi molecolare e le prove di patogenicità hanno permesso di identificare in Neofusiccocum parvum (Pennycook & Samuels) Crous, Slippers and Phillips l’agente eziologico responsabile delle morie di A. melanoxylon osservate in Sicilia. Sulla base delle nostre conoscenze, questa è la prima segnalazione di N. parvum su A. melanoxylon.
N. parvum è un fungo ascomicete appartenente alla famiglia Botryosphaeriaceae, ordine Botryosphaeriales. Esso è un patogeno generalista, cosmopolita, presente in svariati ambienti a clima temperato, mediterraneo e subtropicale, strettamente associato ad almeno 90 entità botaniche, soprattutto, angiosperme arboree ed arbustive, coltivate, ornamentali o forestali, ma è segnalato anche su alcune conifere e sui frutti di piante coltivate ([2], [14], [6], [9]). In Europa, è stato segnalato in Francia, Grecia, Portogallo, Spagna e Italia su eucalipto, sughera, leccio, drupe di olivo e vite ([3], [10], [13]).
N. parvum assume una particolare importanza fitosanitaria in Australia e in SudAfrica come agente responsabile di cancri, deperimenti e morie su diverse specie di eucalipto e su vite. Il materiale di propagazione, prevalentemente di queste ultime due specie, è considerato il principale responsabile della diffusione del fungo in differenti Paesi dell’emisfero sud del pianeta ([10]), in ciò facilitato dal comportamento endofitico che gli consente di vivere in maniera asintomatica su un’ampia varietà di ospiti ([7], [8], [12]).
Riguardo al contesto ecologico - colturale dei popolamenti siciliani di acacia dal legno nero interessati dagli attacchi della specie fungina si evidenzia, in particolare, come questi impianti misti, come del resto tanti altri a gestione demaniale, non sono stati oggetto negli anni di pianificazione strategica, né degli ordinari interventi selvicolturali. Tutto ciò ha, di conseguenza, generato fenomeni di competizione interspecifica ed intraspecifica che hanno determinato uno stato di sofferenza generalizzata dei popolamenti, aggravata dal superamento della maturazione fisiologica e, quindi, dall’invecchiamento delle piante adulte, quest’ultime maggiormente interessate dai fenomeni di deperimento. Questi fattori predisponenti agevolano l’azione patogena di N. parvum già dimostrata anche nel nostro paese su vite, quercia da sughero e leccio ([4], [5], [15]). L’elevata adattabilità ecologica di N. parvum, l’aggressività e la capacità di passare da una fase di latenza a una di virulenza al verificarsi di condizioni di stress per le piante e la presenza di diverse essenze arboree ed arbustive endemiche, potenzialmente ospiti, nei boschi demaniali limitrofi ai popolamenti di A. melanoxylon, costituiscono delle precondizioni ottimali affinché si possano verificare in tale contesto fenomeni di passaggio del fungo da un ospite ad un altro (host jumps) e costituire delle possibili e pericolose nuove associazioni ospite-patogeno. Per evitare o contenere i possibili danni conseguenziali è necessario adottare misure repentine di sanitizzazione che abbassino drasticamente la carica d’inoculo fungino e pianificare interventi di sostituzione di questa specie esotica con altre che abbiano funzioni molteplici adatte agli ambienti (ad es., castagno) o favorendo l’insediamento e lo sviluppo di specie autoctone come il leccio e altre di tipo arbustivo.
L’ampliamento del monitoraggio fitosanitario alle altre formazioni boschive dei Monti Peloritani consentirà, infine, la possibile individuazione di popolamenti di altre essenze forestali interessati dalle infezioni di N. parvum e di programmare, in tal caso, adeguate misure gestionali e di difesa.
Ringraziamenti
Si ringrazia il Prof. Paolo Gonthier del DISAFA, Università degli Studi di Torino, per il contributo alla stesura del testo.
References
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar