Acacia saligna: an invasive species on the coast of Molise (southern Italy)
Forest@ - Journal of Silviculture and Forest Ecology, Volume 14, Pages 28-33 (2017)
doi: https://doi.org/10.3832/efor2211-013
Published: Jan 31, 2017 - Copyright © 2017 SISEF
Research Articles
Abstract
Italy is one of the European countries most affected by biological invasions. In this study, we focused on the impact of Acacia saligna, an Australian invasive plant species, on the coastal ecosystem’s ecology and biodiversity along the sandy coasts of Molise (southern Italy). We analyzed data from 61 vegetation plots recorded in coastal pine forest and Mediterranean scrub habitats of Molise throughout the preparatory actions of the “LIFE Maestrale” project (NAT/IT/000262). In order to study the ecological impact of Acacia saligna comparing invaded and non-invaded areas, we first assigned the Ellenberg’s indicator values to each plant species, which were then used to relate the presence of Acacia saligna with ecological characteristics of sites through a generalized linear model (GLM). Our results showed a significant positive relationship between the presence of Acacia saligna and high levels of soil nutrients and, on the contrary, a negative relationship with the presence of mesophilic species, which are typical of the community interest habitats of pine forest (2270*). The use of ecological indicators is effective to pinpoint the ecological effects of biological invasions, as well as to evaluate habitat conservation state and to identify vulnerable native species.
Keywords
Alien Species, Acacia Saligna, EC Priority Habitat, Nitrophilous Species, Molise
Introduzione
Le invasioni biologiche da parte di specie non native sono una delle cause più rilevanti di perdita di biodiversità e alterazione degli ecosistemi su scala globale ([28], [13], [30]). Le specie esotiche, quando assumono un comportamento di tipo invasivo, comportano una serie di conseguenze negative sia sulla componente naturale degli ecosistemi che sull’economia e sulla salute umana ([15]); basti pensare che i problemi causati dalle specie invasive vegetali comportano danni per oltre 3.7 miliardi di euro ogni anno in Europa ([18]).
Tra gli ambienti più sensibili all’invasione di specie non native ci sono sicuramente le dune costiere, dove sono state censite numerose specie esotiche erbacee e legnose ([1], [6], [26]) e sono state registrate profonde alterazioni del suolo causate dall’accumulo della loro lettiera ([16], [27]). Nello specifico, le dune costiere in Italia sono particolarmente minacciate dalla pressione antropica ([25], [2]) e risentono fortemente del problema delle specie esotiche invasive. Allo stesso tempo, molti tratti della costa Italiana sono caratterizzati da un elevato valore naturalistico e di biodiversità e, per questo motivo, sono tutelati a livello nazionale ed internazionale attraverso la creazione di aree protette incluse nella rete Natura 2000, istituita ai sensi della direttiva Habitat (92/43/EEC - [12]), che rappresenta uno degli strumenti Europei più efficaci in materia di tutela della biodiversità. Per questi motivi è di fondamentale importanza studiare quali siano gli effetti dell’invasione delle specie esotiche sulla biodiversità degli ambienti naturali, al fine di adottare specifiche strategie di contenimento ed eradicazione di quelle maggiormente invasive.
Lungo la costa molisana numerosi habitat di interesse comunitario sono ancora abbastanza diffusi e ben rappresentati, in particolare in tre Siti di Importanza Comunitaria (S.I.C.) all’interno della rete Natura 2000 ([29]). Tuttavia, gli habitat di interesse comunitario presenti in queste aree sono costantemente minacciati da progetti di sfruttamento antropico del litorale e da processi invasivi di specie esotiche ([1], [17], [29]). Una delle specie esotiche che da tempo colonizza gli ambienti naturali e semi-naturali del litorale molisano è Acacia saligna ([10]), leguminosa di origine australiana introdotta intenzionalmente in passato per alcuni interventi di rimboschimento lungo il litorale adriatico, in seguito naturalizzata e divenuta poi invasiva negli habitat di duna e retroduna.
In questo articolo si riportano i risultati di uno studio che ha valutato l’impatto della specie esotica Acacia saligna sulla biodiversità e l’ecologia degli ecosistemi dunali del litorale molisano. Nello specifico sono state valutate, attraverso il campionamento della vegetazione, le caratteristiche ecologiche delle aree invase e non invase. La nostra ipotesi preliminare è che Acacia saligna sia in grado di modificare le condizioni micro ambientali (in termini di disponibilità di luce, nutrienti, umidità, ecc.) con conseguenze negative sulla flora autoctona. La ricerca è stata svolta nell’ambito del progetto LIFE “Maestrale” (NAT/IT/ 000262) che ha come obiettivo la conservazione degli habitat dunali della costa molisana.
Materiali e metodi
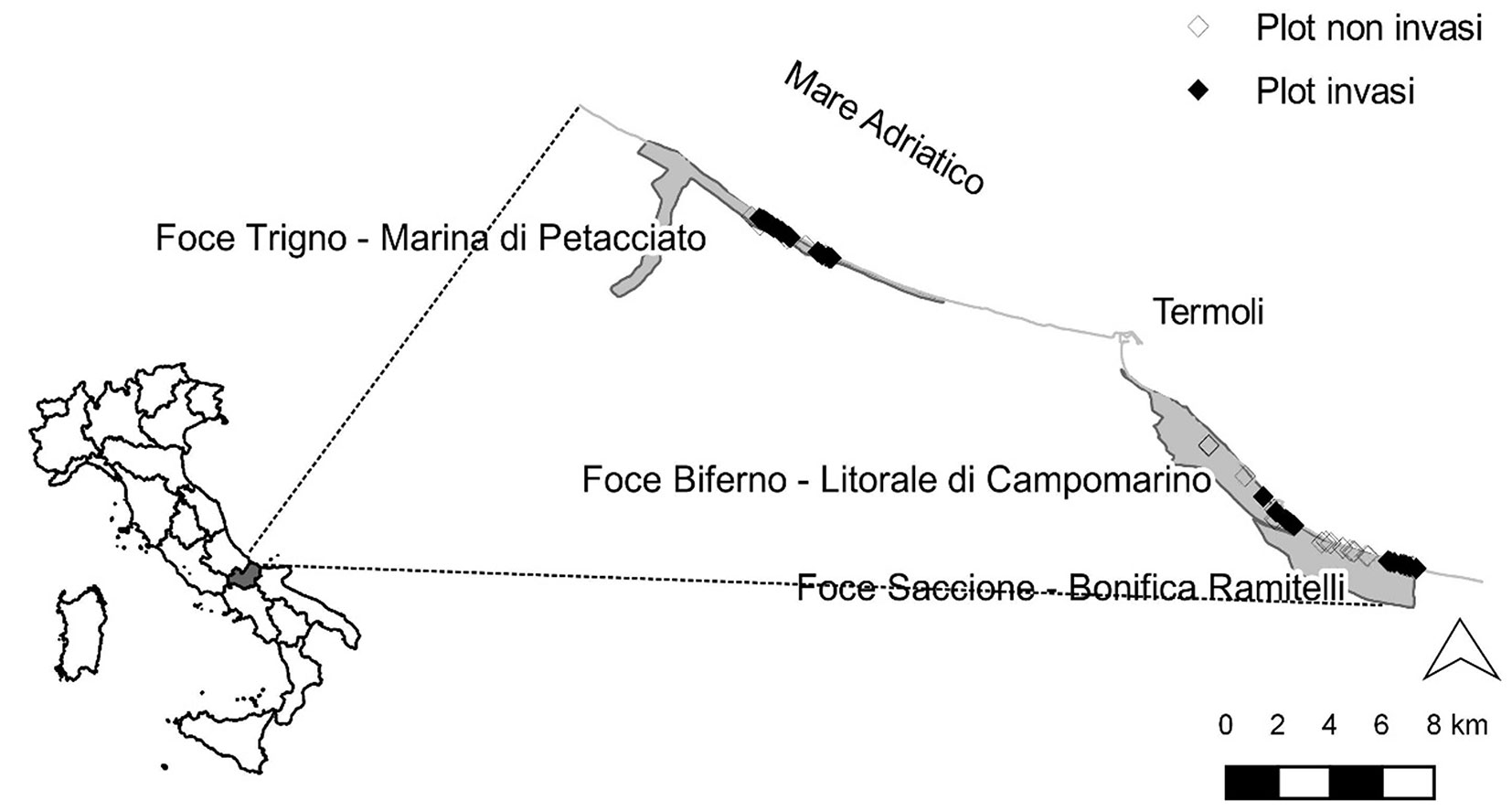
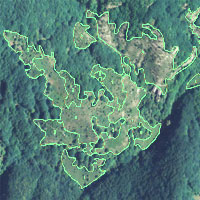
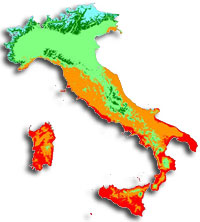
L’area oggetto di analisi è compresa nei S.I.C. “Foce Trigno-Marina di Petacciato”, ”Foce Biferno-Litorale di Campomarino” e “Foce-Saccione-Bonifica Ramitelli” (Fig. 1). Sono presenti numerosi habitat di interesse comunitario, tra i quali risultano essere di interesse prioritario la macchia a ginepri (H2250* - Dune costiere con Juniperus spp.) e la pineta litoranea (H2270* - Dune con foreste di Pinus pinea e/o Pinus pinaster), che coprono complessivamente 117.32 ha. A contatto con questi habitat, 16.50 ha ettari risultano occupati da boscaglie ad Acacia saligna.
Diversi studi hanno dimostrato che Acacia saligna, leguminosa originaria dell’Australia dove è molto comune sui terreni sabbiosi, è in grado di indurre cambiamenti microclimatici, dei regimi di umidità e del livello di nutrienti nel suolo ([21], [20], [32], [19]). Molti cambiamenti sono direttamente attribuibili alle caratteristiche chiave della specie, come la produzione di un gran numero di semi che si accumulano nel terreno e che possono germinare rapidamente dopo incendi o pioggia, l’elevato tasso di crescita e la produzione di un’elevata biomassa ([31]), che le consentono di competere con le specie legnose ([33]). Nel Mediterraneo, in Nord Africa, in Medio Oriente, Sud Africa e Uruguay questa specie è stata utilizzata per contenere l’erosione costiera e come frangivento grazie alla capacità delle sue radici di trattenere la sabbia ([22]). In Italia è stata introdotta nelle zone costiere a scopo di rimboschimento e per la stabilizzazione delle dune, tuttavia la sua diffusione non è stata controllata e attualmente risulta invasiva in molte regioni: Liguria, Toscana, Campania, Basilicata, Calabria, Puglia, Molise, Sicilia e Sardegna ([10]). È diffusa in particolare sulla costa adriatica meridionale (centro e sud Italia), dove cresce tra la macchia mediterranea e la foresta sempreverde delle dune fisse ([17]).
Campionamento della vegetazione
Per verificare l’impatto di Acacia saligna sulla biodiversità e l’ecologia degli ecosistemi dunali del Molise, sono stati analizzati i dati relativi a 61 campionamenti floristico-vegetazionali degli ambienti di pineta costiera e macchia mediterranea, effettuati nell’ambito delle azioni preparatorie del progetto LIFE “Maestrale” (Fig. 1). Si tratta di plot quadrati di 4 × 4 m, distribuiti in maniera casuale nelle aree invase da Acacia saligna (34 plot) e nelle aree di pineta e macchia non invase limitrofe (29 plot). In ciascun plot, è stata registrata la lista delle specie di flora vascolare presente e, a ciascuna specie è stata attribuita una stima visuale della copertura in percentuale. Il riconoscimento dei campioni è stato effettuato utilizzando le chiavi dicotomiche presenti nella “Flora d’Italia” ([23]) mentre la nomenclatura segue quanto riportato nella “Checklist della Flora Italiana” ([8]).
Analisi dei dati
Al fine di caratterizzare le aree invase e non invase dal punto di vista ecologico, a ciascuna specie di pianta vascolare censita è stato associato il suo valore ecologico indicativo secondo Ellenberg ([14]) e adattato alla flora italiana da Pignatti ([24]). Tali valori di bioindicazione consentono di classificare le specie in base alle loro preferenze ecologiche in termini di tipo di suolo, di nutrienti, di umidità, temperatura e altro e rappresentano uno strumento efficace per la descrizione dei gradienti e delle condizioni ambientali ([11], [5]). Gli indici di Ellenberg sono espressi in un range di valori che va da 1 a 9 oppure da 1 a 12 a seconda dell’indice utilizzato ([24]). In questo lavoro sono stati considerati i seguenti indici di Ellenberg: luminosità (L), umidità (U), nutrienti (N), temperatura (T) e continentalità (C). Per caratterizzare in maniera efficace le aree invase e non invase, per ogni plot è stato ricavato un valore sintetico di ciascun indice di Ellenberg, utilizzando la presenza delle specie di flora vascolare come segue. Data pij la presenza della specie i nel plot j e Xik il valore dell’indice k di Ellenberg assegnato alla specie i, il valore di Ellenberg per quel plot viene calcolato come segue (eqn. 1):
Gli Indici di Ellenberg per i plot invasi e non invasi così ottenuti, sono stati utilizzati come variabili esplicative (indipendenti) nella costruzione di un modello in grado di predire la probabilità di presenza di Acacia saligna in funzione delle caratteristiche ecologiche dei plot. Per tale scopo è stato usato un modello lineare generalizzato (GLM) di tipo binomiale che segue la seguente formula (eqn. 2):
La variabile di risposta (Y) rappresenta la probabilità di presenza dell’Acacia saligna nei plot e può variare tra 0 (assenza) e 1 (presenza); β0 è l’intercetta, mentre β1, β2, β3, β4 β5 rappresentano rispettivamente le pendenze delle rette in funzione dei valori di umidità (U), nutrienti (N), luminosità (L), temperatura (T) e continentalità (C). Il modello è stato inizialmente parametrizzato utilizzando tutte le variabili indipendenti e, attraverso una procedura di selezione basata sull’AIC (Akaike’s Information Criterion), è stato selezionato il modello ottimale, ovvero quello che contiene solo le variabili indipendenti più significative. Tale procedura calcola vari modelli con diversa combinazione di variabili e seleziona il modello con il valore di AIC più basso (ovvero il modello meno complesso che presenta il miglior adattamento ai dati osservati).
Successivamente, per identificare quali specie contribuiscono maggiormente nel determinare le differenze in termini di composizione ed ecologia dei plot invasi e non invasi, è stata effettuata l’analisi SIMPER (similarity percentages - [7]).
Risultati
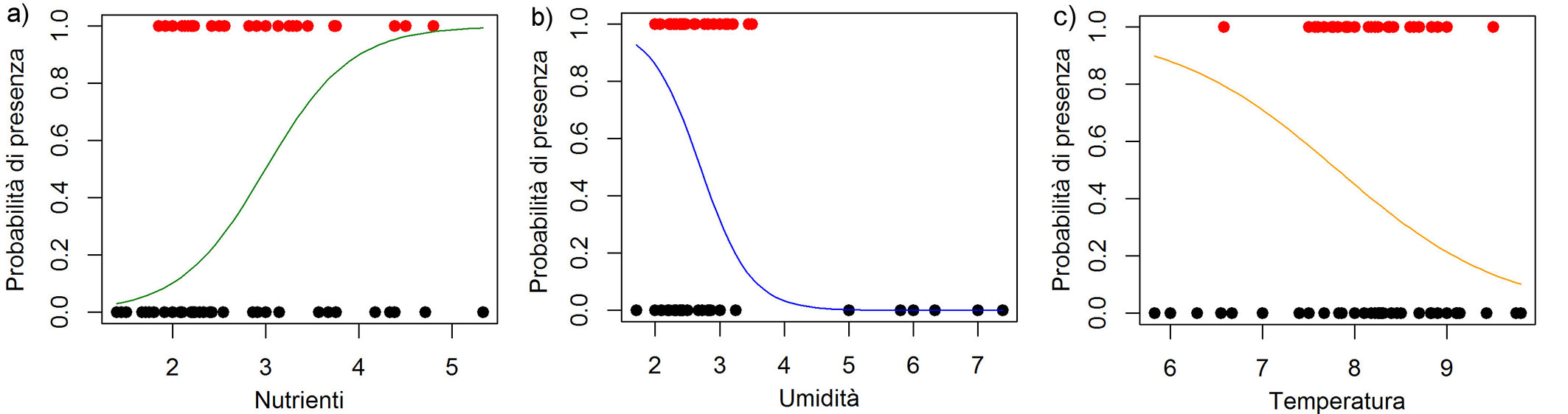
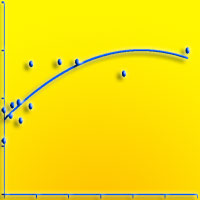
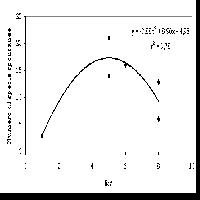
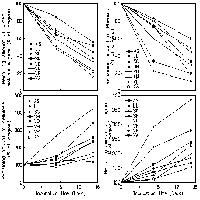
Nelle aree analizzate sono stati censiti 89 taxa (specie e sottospecie). La procedura di selezione delle variabili ha restituito un modello finale che comprende gli indici di umidità, temperatura e nutrienti. Il modello GLM risulta essere adeguato, riuscendo a spiegare il 20% della devianza (D2 = 0.20). Il modello ha messo in evidenza che la probabilità di presenza di Acacia saligna è spiegata significativamente dai valori di Ellenberg di umidità (U), temperatura (T) e di nutrienti (N). Nello specifico la probabilità di presenza è associata positivamente ad alti valori di nutrienti nel suolo (z = 2.975, p = 0.002), mentre è negativamente correlata a valori medio-alti di umidità (z = -2.876, p = 0.004) e di temperatura (z = -2.023, p = 0.043 - Fig. 2).
Fig. 2 - Probabilità di presenza di Acacia saligna in funzione dei valori di Ellenberg di nutrienti (a), di umidità (b) e temperatura (c).
Dall’analisi SIMPER emerge che 17 delle 89 specie vegetali contribuiscono per il 50% alle differenze osservate tra i plot invasi e non invasi (Tab. 1).
Tab. 1 - Contributo delle specie (in % e cumulato) nel determinare le differenze in termini di composizione specifica tra i plot invasi e i plot non invasi. La dissimilarità media indica la differenza tra i gruppi di plot (invasi e non invasi) calcolata sulla base dell’indice di Bray-Curtis. I simboli “+” e “-” indicano associazione positiva e negativa ai plot invasi. (U): indice di Ellenberg di umidità; (N): indice di Ellenberg di nutrienti; (T): indice di Ellenberg di temperatura.
| Specie | Dissimilarità media |
Contributo % |
Cumulativo % |
Associazione | U | N | T |
|---|---|---|---|---|---|---|---|
| Asparagus acutifolius | 3.11 | 4.05 | 4.05 | + | 2 | 5 | 9 |
| Lotus cytisoides | 3.09 | 4.03 | 8.08 | + | 1 | 1 | 10 |
| Pinus halepensis | 2.86 | 3.73 | 11.81 | + | 2 | 2 | 10 |
| Rosmarinus officinalis | 2.52 | 3.28 | 15.09 | - | 2 | 1 | 8 |
| Lagurus ovatus | 2.48 | 3.24 | 18.33 | + | 3 | 2 | 9 |
| Sonchus bulbosus | 2.48 | 3.26 | 21.56 | + | 3 | 3 | 8 |
| Phillyrea angustifolia | 2.46 | 3.21 | 24.78 | - | 1 | 2 | 10 |
| Cistus incanus | 2.45 | 3.15 | 27.93 | - | 2 | 2 | 9 |
| Silene vulgaris | 2.37 | 3.09 | 31.02 | + | 4 | 2 | - |
| Oryzopsis miliacea | 2.36 | 3.08 | 34.10 | + | 4 | 5 | 7 |
| Smilax aspera | 2.33 | 3.03 | 37.13 | - | 2 | 3 | 10 |
| Pistacia lentiscus | 2.29 | 2.98 | 40.11 | - | 2 | 2 | 10 |
| Rhamnus alaternus | 2.20 | 2.86 | 42.98 | + | 2 | 4 | 9 |
| Geranium purpureum | 2.07 | 2.69 | 45.67 | + | 3 | 3 | 8 |
| Vulpia fasciculata | 2.01 | 2.62 | 48.29 | - | 1 | 1 | 10 |
| Cerastium semidecandrum | 1.97 | 2.59 | 50.88 | + | 4 | 0 | 7 |
Discussioni e conclusioni
Dalle analisi condotte emerge che Acacia saligna si associa con maggiore probabilità a specie nitrofile e che non si consocia alle specie mesofile di pineta e macchia mediterranea. Tale comportamento è in linea con quanto recentemente osservato da Del Vecchio et al. ([10]), che evidenziavano l’aumento di specie ruderali (per lo più nitrofile) nelle aree invase da Acacia saligna.
Probabilmente l’aumento del livello di nitrati nel suolo nelle aree invase ([9]) è da imputare sia al fatto che le radici di A. saligna sono in simbiosi con batteri capaci di fissare l’azoto, che alle caratteristiche biochimiche della lettiera di questi popolamenti.
Inoltre è stata osservata una diminuzione delle specie mesofile nelle aree invase da A. saligna, evidenziando la sua capacità di inaridire i suoli e di escludere molte specie focali, tipiche degli habitat di interesse comunitario di pineta e macchia. La presenza di A. saligna è correlata ad un aumento di specie ruderali nelle dune costiere come Geranium purpureum e Oryzopsis miliacea ([4]), a scapito delle specie focali tipiche dell’habitat *2270 e dell’habitat *2250 quali Smilax aspera e Pistacia lentiscus. Probabilmente anche la presenza di sostanze allelopatiche contenute nella corteccia, nei fiori e nelle foglie di A. saligna e riversate nella lettiera possono avere un ruolo importante nel limitare la germinazione di molte specie native, come descritto da Alhammadi ([3]). La maggior parte degli effetti negativi causati dalle piante esotiche è dovuta infatti alla presenza di sostanze allelopatiche che provocano interferenze con i processi fisiologici e biochimici nella vegetazione autoctona.
L’uso dei valori di biondicazione della flora vascolare ha consentito quindi di evidenziare un’alterazione della struttura e dell’ecologia degli habitat prioritari di interesse comunitario H2270* e H2250* in presenza di popolamenti invasivi di A. saligna lungo le coste molisane. L’applicazione dei valori ecologici indicativi risulta pertanto efficace per individuare i macro effetti ecologici dei processi invasivi di specie esotiche vegetali e può essere utilizzata anche in altri contesti interessati da questi fenomeni, ad esempio per valutare lo stato di conservazione degli habitat di interesse comunitario e contribuire ad individuare le specie native vulnerabili e quelle invece idonee a contrastare la capacità invasiva delle specie esotiche.
References
CrossRef | Google Scholar
Online | Google Scholar
Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar