Drought and heat waves, cues for an adaptive silviculture
Forest@ - Journal of Silviculture and Forest Ecology, Volume 18, Pages 49-57 (2021)
doi: https://doi.org/10.3832/efor0054-018
Published: Jul 09, 2021 - Copyright © 2021 SISEF
Commentaries & Perspectives
Abstract
We propose some ideas for an adaptive silviculture in the Mediterranean biogeographic region that could assist in shaping forests which are less vulnerable to extreme climatic events, such as those drought and heat waves that are expected to be more intense and frequent in the future. We discuss about silvicultural approaches that would aim to: regulate competition and density-dependent effects; enhance functional diversity; increase the complexity of forest communities. These approaches are especially advisable in the Mediterranean region, which is a hotspot for climate change and where forests have been exploited for many centuries and are only recently taking advantage of a recovery phase.
Keywords
Forest, Tree, Drought, Decline, Management, Functional Diversity, Mediterranean
Introduzione
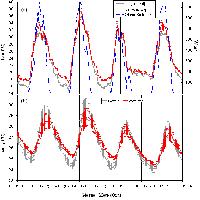
Le foreste ospitano gran parte della biodiversità e del carbonio degli ecosistemi terrestri, svolgono una parte importante nella mitigazione climatica e procurano alla società un ampio ventaglio di benefici ambientali ed economici. Alcune di queste funzioni potrebbero essere messe a rischio dal cambiamento climatico antropogenico: il riscaldamento globale e le variazioni nei regimi pluviometrici determinano più intense e frequenti ondate di siccità e calore (OSC), che stanno innescando fenomeni di declino e mortalità nelle foreste di diversi biomi e in diversi continenti ([4], [14], [54]). Un effetto OSC in Italia meridionale è documentato in Fig. 1 e Fig. 2; una ricognizione delle crisi da siccità osservate nei querceti mediterranei è reperibile in Gentilesca et al. ([28]).
Fig. 1 - Danni alle chiome in un bosco a prevalenza di roverella (in alto) e in una formazione a prevalenza di leccio (in basso) (Basilicata, Parco Regionale di Gallipoli Cognato - Piccole Dolomiti Lucane, agosto 2017). L’effetto è imputabile a una OSC, documentata da Rita et al. ([51]).
Fig. 2 - Seccumi apicali dovuti a crisi del sistema di trasporto idraulico in condizioni di forte stress idrico. A sinistra: alberi di roverella nel bosco del Comune di Gorgoglione (Matera), colpiti da OSC. A destra, alberi di farnia del Parco del Ticino (Milano). In questo caso la causa dello stress idrico è rappresentata, probabilmente, da un abbassamento della falda freatica ([22]). Nel parco del Ticino sono in corso ricerche per esplorare il ruolo della diversità genetica e della plasticità fenotipica nel determinare la risposta delle piante di farnia alla carenza idrica.
La risposta degli alberi al fenomeno OSC coinvolge numerosi aspetti morfo-funzionali, tuttavia c’è accordo su un fatto: il fattore che innesca il declino fisiologico è rappresentato, anzitutto, dal collasso del sistema di trasporto idraulico ([1] - vedi Box 1).
Box 1 - Una vita in tensione, gli alberi fra necessità e vulnerabilità.
Gli alberi, come tutte le piante terresti, hanno la necessità di sollevare l’acqua dal suolo alle foglie, dove questa viene utilizzata per la fotosintesi e le altre funzioni vitali. Questo trasporto è assolto dal sistema xilematico: una matrice di elementi porosi (i condotti xilematici), finemente interconnessi, attraverso i quali l’acqua risale, suddivisa in innumerevoli filetti, verso la chioma. Assolvere a questa necessità implica però una condizione di vulnerabilità, proprio a carico del sistema xilematico: si tratta, a conti fatti, del prezzo che le piante devono pagare per la colonizzazione degli ambienti terrestri. Negli alberi, a causa delle grandi dimensioni, questa vulnerabilità è accentuata e quando si trovano esposti a prolungate e intense siccità il sistema xilematico può subire dei danni, che insorgono a causa del fenomeno della cavitazione xilematica, che qui descriviamo per sommi capi.
La risalita dell’acqua avviene grazie alla forza traente della traspirazione: una forza che “tira” verso l’alto i filetti di acqua che scorrono nei condotti xilematici. Come elastici tirati, questi filetti sono sottoposti a una tensione, che aumenta col crescere del deficit idrico del suolo e con il potere evaporante dell’atmosfera. Raggiunto un certo livello, la tensione diventa una forza in grado di aspirare, attraverso le interruzioni (punteggiature) della parete xilematica, l’aria presente negli spazi esterni, che entra così nel condotto in forma di minuscole bolle. Per via dell’instabile equilibrio fisico dell’acqua quando è sotto tensione, queste bolle si aggregano rapidamente fra di loro e formano delle cavità occupate da emboli gassosi. Gli emboli bloccano il flusso idrico nel condotto xilematico e sono in grado di diffondersi a cascata da un condotto all’altro con il medesimo meccanismo, estendendo l’area xilematica inattiva sul piano della funzionalità idraulica. Questi fenomeni sono stati descritti e interpretati fin dagli anni âÂÂ80 del secolo scorso (v. [61], [56]). Alla lunga, si può innescare un circolo vizioso in cui cavitazione e tensione xilematica si alimentano a vicenda, così da causare condizioni di embolia sempre più estese, che possono dar luogo a un vero e proprio collasso del trasporto idraulico. In condizioni estreme, si può arrivare alla completa recisione della continuità idraulica e del rifornimento idrico alla chioma, che entra così in sofferenza, iniziando dai rametti apicali dove più alta è la tensione xilematica (Fig. 2). Per approfondimenti: Tyree & Ewers ([55]), Borghetti et al. ([10]), Tyree & Zimmermann ([57]), Choat et al. ([19]).
Negli anni a venire sono previste OSC più frequenti e intense ([32]). Ciò desta interrogativi circa la possibilità che nelle zone maggiormente esposte al fenomeno, come la regione biogeografica mediterranea, le foreste siano in grado di mantenere le loro caratteristiche e la piena funzionalità. OSC frequenti sono in grado di ridurre l’assorbimento del carbonio, la produttività primaria come quella strettamente legnosa, di accelerare i cambiamenti nella composizione e nella struttura della comunità, di modificare le componenti del bilancio idrologico, ecc. ([14], [43]).
In una rassegna a scala globale ([6]) è stato messo in evidenza che la mortalità provocata da OSC è spesso seguita da modificazioni della composizione e della struttura della comunità forestale con accelerazione dei processi di successione ecologica, che spesso assumono connotazione regressiva. Frequentemente, è stato osservato, la specie arborea dominante viene sostituita da altre specie e in un significativo numero di situazioni la foresta evolve verso comunità a prevalenza di arbusti, con perdita di biodiversità e di funzioni. Estesi eventi di questo tipo potrebbero imporre scelte gestionali che facilitino i processi di successione, con riconsiderazione dei benefici, produttivi e ambientali, che si attendevano in precedenza. Esempi di modificazioni della comunità forestale e di successioni ecologiche accelerate da OSC sono documentate in Fig. 3 e Fig. 4. Le traiettorie ecologiche post-OSC variano, come direzione e velocità, a seconda degli ambienti, delle caratteristiche della comunità, e della gestione forestale, che non è quindi neutra rispetto agli effetti OSC: sono riportate situazioni in cui gli effetti ne risultano inaspriti, così come situazioni in cui appaiono attenuati ([6]).
Fig. 3 - Aragona nord-orientale, Spagna. Effetti OCS su evoluzione e struttura della comunità forestale. In un bosco con pino marittimo dominante si notano evidenti effetti dovuti a OSC: a partire dal 2017 i pini manifestano sintomi di ingiallimento e trasparenza della chioma e forti segni di declino. La rarefazione della copertura del pino determina un’accelerazione della successione ecologica, con evoluzione verso una comunità a prevalenza di leccio, visibile nel piano inferiore.
Fig. 4 - Pirenei aragonesi, Spagna. Nell’immagine a sinistra, abetine di abete bianco con faggio: l’abete bianco appare più OCS-sensibile del faggio, anche se conserva buone capacità di rinnovarsi. Si tratta di boschi in evoluzione controllata, in cui non sono previsti interventi colturali. Nell’immagine a destra, boschi misti di abete bianco e pino silvestre: l’abete bianco mostra segni di declino per stress climatico, a differenza del pino silvestre. Nelle foto si notano chiome spezzate di abete che originano dei gap nella copertura di dimensioni considerevoli. Il declino causato dalla siccità sta esponendo l’abete agli agenti del marciume radicale.
L’idea qui svolta è che una selvicoltura adattativa, impostata su basi ecosistemiche, potrebbe aumentare la possibilità delle foreste di fronteggiare lo stress OSC. Sulla base di recenti risultati sperimentali in campo, di studi ecofisiologici e di ecologia di comunità, proponiamo qualche spunto di riflessione sul tema, facendo soprattutto riferimento ai boschi (semi-naturali, di origine artificiale, in corso di rinaturalizzazione) della regione biogeografica mediterranea. Ragioniamo, in particolare, sulla prospettiva di metodi colturali volti a: (i) regolare la competizione e gli effetti densità-dipendenti; (ii) agevolare la diversità funzionale della comunità forestale; (iii) promuoverne la complessità.
Regolazione della competizione e degli effetti densità-dipendenti
È un argomento centrale della selvicoltura, nella sua essenza di ecologia applicata ai popolamenti forestali: diradare, cioè ridurre il numero di alberi che crescono su una determinata superficie, è lo strumento di cui il selvicoltore dispone per regolare la competizione per le risorse nel popolamento e per distribuire la crescita fra gli individui in funzione degli obbiettivi produttivi ([25]). È quindi naturale che ai diradamenti si guardi come metodo per migliorare l’uso della risorsa idrica, al fine di ridurre la vulnerabilità del popolamento al fenomeno OSC e di conferirgli resistenza di lunga durata.
Un lavoro recente ([17]) definisce i limiti di questa prospettiva. La riduzione della competizione con il diradamento, viene mostrato, non influenza in modo univoco la risposta (valutata in termini di accrescimento) degli alberi alla siccità; si mette in evidenza l’effetto di alleviamento dello stress idrico nei popolamenti diradati, ma anche l’ampia variabilità di risposta in funzione di fattori locali, da considerare quindi nella definizione dei metodi colturali e della strategia gestionale. La risposta in termini di accrescimento non è, peraltro, l’unico metro di valutazione della reazione della foresta di fronte a un fattore di perturbazione; sono descritti, ad esempio, effetti positivi dei diradamenti sulla resistenza all’attacco di agenti biotici che intervengano successivamente al disturbo abiotico ([16]).
La mancanza di una regola di carattere generale non toglie comunque interesse al tentativo di mettere ordine nella casistica, valutando i risultati della ricerca per categorie entro le quali chi ha pratica di selvicoltura può orientarsi. Così, una valutazione delle evidenze sperimentali più recenti ci porta a individuare alcune tipologie di risposta che potrebbero avere validità al di là del singolo caso; e che potrebbero rappresentare un riferimento sul piano colturale per alleviare gli effetti OSC attraverso una regolazione della competizione e degli effetti densità-dipendenti. Le appuntiamo, qui di seguito, con i riferimenti bibliografici necessari per gli approfondimenti applicativi:
- in popolamenti di conifere a comportamento isoidrico (specie che chiudono gli stomi e riducono la traspirazione ai primi segnali di stress idrico, in modo da evitare un eccessivo aumento della tensione idrica xilematica - vedi Box 1) i diradamenti limitano spesso gli effetti negativi durante il periodo di stress e riducono i tempi richiesti per il ripristino della crescita dopo il periodo di crisi ([2], [11], [58]). Nella prospettiva di OSC a breve tempo di ritorno, la riduzione dei tempi di ripristino assume maggior rilievo;
- l’effetto del diradamento ha una durata che può dipendere dall’intensità con cui viene effettuato. In boschi di conifere dell’ambiente mediterraneo, effetti duraturi (fino a 20 anni dall’intervento) sono stati osservati in caso di diradamenti forti con prelievo di oltre la metà dell’area basimetrica ([46], [41]). In querceti di leccio un diradamento con asportazione del 30% dell’area basimetrica ha ridotto, anche sul lungo periodo, la mortalità e gli effetti negativi della siccità sperimentalmente imposta con l’esclusione delle precipitazioni ([27]); sempre nella lecceta, è stato visto che la riduzione della densità prolunga la crescita in condizioni di stress idrico ([15]);
- il tipo di diradamento (definito in base alle classi arboree sulle quali si interviene) può avere un effetto significativo. Il diradamento di tipo alto, con il quale si interviene sulla classe delle piante dominanti e co-dominanti, favorisce una maggior differenziazione strutturale, la quale può avere un effetto benefico sulla risposta allo stress e sui tempi di ripristino, soprattutto in boschi misti ([34]);
- i diradamenti d’intensità moderata e di tipo basso, con i quali si interviene sulla classe delle piante dominate, potrebbero risultare di effetto modesto nel caso di boschi in cui la resistenza allo stress idrico e il mantenimento del vigore sono la conseguenza di un comportamento anisoidrico, cioè di evasione dallo stress, legata ad esempio allo sviluppo di radici profonde che consentono l’accesso alle zone più umide del suolo. Casi di questo genere sono stati messi in evidenza in querceti della fascia sub-mediterranea caratterizzati da segni di declino e mortalità per OSC ([21], [49] - Fig. 5);
- la durata dell’effetto del diradamento sull’alleviamento dello stress idrico dipende in buona parte dal periodo necessario per la ricostituzione dell’indice di area fogliare (LAI) della copertura arborea, e dall’equilibrio fra LAI arboreo e LAI del sottobosco, il cui sviluppo e la cui traspirazione possono aumentare in rapporto al maggiore afflusso di radiazione luminosa (Box 2). Vi sono casi che dimostrano come una riduzione del sottobosco possa determinare un miglioramento dello stato idrico degli alberi dopo il diradamento ([29]). In ambiente mediterraneo il controllo del sottobosco, che può essere ottenuto con un esercizio regolato del pascolo, viene ad assumere significato anche in relazione alla prevenzione degli incendi boschivi ([40]).
Fig. 5 - Pannelli in alto: bosco di cerro nel Comune di Gorgoglione (Matera); pannello in basso: bosco di farnetto nel Comune di San Paolo Albanese (Potenza). In entrambi i boschi, con sintomi di declino da siccità, sono stati effettuati diradamenti per ridurre la competizione e gli effetti densità-dipendenti; i risultati sono in corso di valutazione.
Box 2 - I fattori di controllo dell’evapotraspirazione nell’ecosistema forestale.
I fattori di controllo dell’evapotraspirazione degli ecosistemi forestali sono: (A) l’umidità dell’aria; (B) l’indice di area fogliare (LAI) e il grado di apertura degli stomi; (C) l’energia a disposizione sotto forma di radiazione netta. Senza entrare in dettagli (si rimanda a [33] come lavoro fondamentale, e a [31] per una trattazione tecnico-divulgativa), a causa del diverso grado di turbolenza dell’atmosfera al di sopra e al di sotto delle chiome degli alberi, la traspirazione del piano arboreo dominante è prevalentemente guidata dai fattori A e B, quella del sottobosco dal fattore C. Secondo un’ipotesi avanzata quasi quarant’anni fa da Roberts ([53]), l’evapotraspirazione degli ecosistemi forestali è un processo abbastanza conservato, grazie al diverso tipo di controllo ambientale cui sono assoggettate la traspirazione del piano dominante e quella del sottobosco, e ad altri processi di compensazione fra le varie componenti dell’ecosistema. Quando, eseguendo un diradamento, si determina una riduzione del LAI del piano dominante, questo provoca una diminuzione della traspirazione arborea e quindi un miglioramento dello stato idrico del suolo e delle piante. Tuttavia, l’effetto può essere vanificato dall’aumento della traspirazione del sottobosco, che beneficia dell’aumento dell’energia radiativa a disposizione per la diminuzione del LAI arboreo ([12], [37]). Il controllo del sottobosco può quindi assumere un ruolo importante per mantenere gli effetti benefici del diradamento sullo stato idrico del suolo.
Esistono quindi possibilità, da valutare caso per caso con esperta professionalità, per applicare interventi di regolazione della competizione che possano mitigare gli effetti OSC. Nella bioregione mediterranea, questa appare una prospettiva con ampi ambiti applicativi: pinete mediterranee, naturali o derivanti da piantagione, rimboschimenti puri o misti, in corso o meno di rinaturalizzazione, pinete oro-mediterranee, popolamenti transitori derivanti da tagli di avviamento all’alto fusto, fustaie monoplane di querce e faggio, ecc.
Agevolazione della diversità funzionale
Le specie arboree mettono in atto un numero elevato di soluzioni, in termini di tratti morfo-funzionali, per adattarsi alle condizioni di siccità (Box 3). L’elevata variabilità che si osserva in campo è un effetto sia della diversità genetica (fra le specie e gli individui al loro interno) che della plasticità fenotipica, cioè della capacità degli alberi di modificare le proprie caratteristiche somatiche a seconda delle specifiche condizioni ambientali.
Box 3 - Tratti morfo-funzionali arborei per l’adattamento alla siccità.
Come visto nel Box 1, la tensione xilematica rappresenta per gli alberi una condizione di rischio: sul suo controllo s’impernia la strategia di adattamento degli alberi alla siccità. La soglia critica di tensione in grado di innescare il fenomeno della cavitazione xilematica varia da specie a specie. Questa variabilità è legata a differenze nella struttura anatomica dello xilema: dimensioni dei condotti e loro interconnessione, porosità delle pareti cellulari, caratteristiche della membrana delle punteggiature, ecc. Una valutazione del ruolo delle caratteristiche xilematiche nel mantenimento del vigore arboreo in ambiente mediterraneo è stata svolta recentemente da Borghetti et al. ([8]). Oltre all’anatomia funzionale dello xilema, molto variabile in funzione dell’ambiente ([9]), vi sono numerosi tratti della pianta collegati all’adattamento alla siccità, che variano in modo coordinato così da bilanciare il controllo della tensione xilematica con l’assimilazione del carbonio per via fotosintetica ([44]). In più, nel corso del loro lungo ciclo vitale, gli alberi sono in grado di “aggiustare” la loro struttura, in particolare di modificare il rapporto fra l’area delle foglie e l’area dei tessuti di conduzione, in un processo di acclimatazione strutturale ([39]). In Tab. 1 si riportano alcuni dei più importanti caratteri morfologici, strutturali e fisiologici dell’albero coinvolti nell’adattamento alla siccità (molti di questi caratteri sono riportati, per le diverse specie, in banche dati di pubblico dominio). Alcuni caratteri strutturali possono essere visti sia come fattori che determinano, sul breve periodo, lo stato idrico della pianta sia come conseguenza dei processi di acclimatazione che l’albero mette in atto, sul lungo periodo, per mantenere uno stato idrico che garantisca la sicurezza del trasporto idraulico. Ad esempio, l’altezza degli alberi, che nella foresta determina fortemente i dinamismi di comunità, può essere vista come la conseguenza della necessità di mantenere la tensione xilematica nella chioma entro le soglie di sicurezza per scongiurare la cavitazione. In questo senso, a parità di altri fattori, si può fare la previsione di una diminuzione dell’altezza degli alberi se il cambiamento climatico porterà a un inasprimento del deficit idrico del suolo. Una rassegna recente dei cambiamenti strutturali della foresta di fronte al riscaldamento globale e all’inasprimento della siccità si trova in McDowell et al. ([43]).
Tab. 1 - Alcuni dei più importanti caratteri morfologici, strutturali e fisiologici dell’albero coinvolti nell’adattamento alla siccità.
| Caratteri morfologici e strutturali | Caratteri fisiologici |
|---|---|
| • Densità e dimensioni dei condotti xilematici • Densità del legno e connettività xilematica • Porosità della membrana delle punteggiature • Segmentazione idraulica • Altezza della pianta • Area fogliare totale e specifica • Rapporto area fogliare/area di conduzione xilematica • Rapporto area fogliare/ biomassa delle radici fini • Profondità delle radici • Rigenerazione vegetativa • Fenologia |
• Soglie di tensione per la cavitazione xilematica • Conduttanza idraulica del fusto e della radice • Regolazione stomatica • Tensione xilematica a chiusura stomatica • Tasso traspirativo per unità di area fogliare • Traspirazione cuticolare • Efficienza d’uso dell’acqua • Elasticità del parenchima • Permeabilità e canali della membrana cellulare • Conduttanza idraulica suolo-radice • Turnover dell’alburno e delle radici fini |
Spesso si osserva variabilità anche all’interno di comunità forestali adattate a difficili condizioni ambientali, ad esempio di comunità che colonizzano gli habitat siccitosi nell’ambiente schiettamente mediterraneo, come se l’ambiente lasciasse passare fra le sue maglie selettive diverse possibili soluzioni di adattamento; ciò può trovare spiegazione nel fatto che le strategie di tolleranza o evasione dallo stress idrico possono essere molto diverse fra le specie, e più o meno efficaci a seconda di come la siccità si sviluppa ([7]). Si osserva pure che specie apparentemente simili, si differenziano nel modo con cui affrontano i periodi post-siccità: vi sono specie che, dopo la reidratazione del suolo, procedono a una rapida sostituzione dello xilema danneggiato con nuovo tessuto legnoso, in un processo che può comunque portare alla deplezione delle riserve di carbonio e a una situazione di debolezza, ad esempio nei confronti di attacchi da parte di agenti biotici; come vi sono specie che reagiscono investendo prevalentemente in area fogliare invece che nella ricrescita legnosa, esponendosi a maggiori rischi di fronte alle siccità successive, per il sotto-dimensionamento del sistema di trasporto (vedi [14]).
In rapporto a questa variabilità ecofisiologica e alle differenti strategie di risposta, una selvicoltura adattativa OCS può essere pensata come quella che cerchi di integrare, fra i criteri di scelta colturale, la dimensione della diversità funzionale. In particolare, proponendosi: (i) d’interpretare e dare un peso alla diversità dei tratti adattativi delle specie arboree sulla base della variabilità micro-ambientale, tenendo anche conto della prospettiva del cambiamento climatico; (ii) di procedere con scelte colturali che promuovano la diversità funzionale nella data situazione stazionale e nelle specifiche condizioni del popolamento ([5]).
Vi sono strumenti e procedure che possono essere d’aiuto in questo approccio colturale, rendendolo realistico nell’ambito di procedure di gestione forestale; ad esempio:
- la disponibilità di banche dati, ormai molto estese e in continuo aggiornamento, sui tratti funzionali delle specie arboree. Citiamo, come esempio, la banca dati TRY: ⇒ http://www.try-db.org/TryWeb/Home.php ([35]). In analogia ai metodi della precision forestry ([24]), queste informazioni possono essere incrociate con dati di composizione specifica per area, classi dimensionali e sociali, ricavabili da indagini inventariali o da ricognizioni da remoto, le cui potenzialità interpretative e facilità d’uso aumentano quasi giornalmente ([18], [26]). Si possono produrre, in questo modo, cartografie funzionali da utilizzare come guida operativa negli approcci colturali a scala di popolamento/comunità, e di indirizzo nelle decisioni gestionali a scala aziendale e territoriale; si rimanda a Lavorel et al. ([36]) per un’applicazione della diversità funzionale a scala di paesaggio e a Borghetti et al. ([8]) per un esercizio in cui la foresta mediterranea è stata descritta, ad ampia scala geografica, in termini di diversità funzionale basandosi sui caratteri dello xilema delle diverse specie che edificavano la comunità forestale;
- la disponibilità di modelli di simulazione che forniscano previsioni di supporto per le decisioni colturali e gestionali. Sono in corso progressi, nella modellistica empirica e di processo, affinché possano essere oggetto di simulazione: la probabilità di crisi nelle diverse classi dimensionali e sociali del popolamento arboreo; le probabilità di ripresa post-siccità a seconda delle strategie adottate dalle specie che edificano la comunità e dell’insorgenza di condizioni di debolezza che favoriscano attacchi parassitari; le risposte funzionali modulate da variazioni topo-climatiche a scala geografica fine; a scala territoriale, le risposte di comunità forestali funzionalmente simili in ambienti eterogenei, ecc. ([23], [3], [52], [59]).
È ragionevole pensare che il rapido sviluppo dei data-base di pubblico dominio, dei sistemi di monitoraggio, delle piattaforme hardware e del software renderanno questi strumenti utilizzabili anche in ambito professionale.
Promozione della complessità
Connesso all’aspetto trattato nel precedente paragrafo, è questo uno dei punti più importanti: una comunità forestale complessa, a elevata biodiversità funzionale e strutturale, si candida come quella maggiormente in grado di conservare la funzionalità in ambienti sottoposti a forti stress ambientali.
È tutt’ora argomento di studio il peso relativo dei filtri competitivi, della complementarietà di nicchia e delle interazioni facilitanti sul dinamismo delle comunità nelle diverse situazioni ambientali ([45]). Tuttavia, sono numerose le ricerche che mettono in evidenza una relazione positiva fra biodiversità, funzionalità e produttività degli ecosistemi forestali (vedi [38] per una valutazione a scala globale). Le interazioni facilitanti appaiono frequenti in condizioni ambientali difficili e questo può spiegare le più strette relazioni fra ricchezza specifica e produttività che si osservano nel bioclima mediterraneo rispetto a quello temperato ([50]).
Di fronte ai fenomeni OCS, si tratta peraltro di passare dalla prospettiva di una foresta ad alta ricchezza specifica, che potrebbe rivelarsi funzionalmente debole e incapace di fronteggiare il disturbo, ad una foresta, come proposto nel paragrafo precedente, che sia ad alta ricchezza funzionale ([5]). In questo senso, una selvicoltura adattativa va configurata come una selvicoltura di sistema e di copertura che miri a: un alto grado di di diversità strutturale e d’integrazione funzionale; alla promozione dei processi di rinnovazione gamica e al sostegno dei processi di autorganizzazione; al rispetto di livelli minimi di consistenza in termini di biomassa; a valorizzare gli effetti “lascito e ritenzione”, ecc. (v. [20], [30], [48]).
Appaiono vasti gli ambiti applicativi per questa prospettiva selvicolturale nella regione biogeografica mediterranea in cui nel corso del tempo le foreste (dalla fascia schiettamente mediterranea a quella oro-mediterranea: leccete meso-termofile, querceti xerofili e mesofili, puri o misti, faggete termofile, montane e alto-montane, boschi con conifere montane, ecc.) hanno subito cospicui impoverimenti in termini di consistenza e biodiversità compositiva, strutturale e funzionale.
Conclusioni
Nella regione biogeografica mediterranea, al pari di altre zone del nostro paese, da qualche decennio i boschi mostrano, in seguito alla rivoluzione nell’approvvigionamento energetico avvenuta nell’ultimo dopoguerra e alle mutate condizioni socio-economiche, una fase di ripresa ([42]). La quale, per ora, si è tradotta in apprezzabili aumenti di superficie e di incremento, meno nel recupero della biodiversità compositiva, strutturale e funzionale, che pure si avverte in qualche caso. Questi boschi si trovano ora ad affrontare il cambiamento del clima e, come abbiamo visto, rischiose ondate di siccità e di calore.
In questa situazione non si ravvisa di certo la necessità di una gestione frettolosa che, dando per garantite dinamiche di crescita e accumulo di carbonio che scontate invece non sono ([13]), riproponesse vecchi schemi di utilizzazione: nell’illusione che questo possa essere motore di una valorizzazione territoriale e progresso economico e sociale; o che tollerasse raccolte di biomassa legnosa per usi energetici non compatibili con gli obbiettivi della mitigazione climatica e di conservazione della biodiversità ([60]). Auspichiamo, invece, una selvicoltura che applichi i suoi fondamenti ecologici nella gestione dei popolamenti che possono svolgere una funzione produttiva; che sappia assecondare i dinamismi della foresta, promuovere la rinnovazione naturale e l’evoluzione a fustaia, valorizzare la diversità funzionale, interpretare e rispettare una foresta semi-naturale che in molti casi deve ancora recuperare dal passato sfruttamento, e deve poterlo fare nel quadro di una gestione impostata in una prospettiva di sistema e di regolare controllo dei risultati ([47]); e che talvolta sappia anche percorrere la strada della prudenza e dell’attesa.
L’aumento della diversità biologica e la capacità di fronteggiare gli eventi climatici estremi sono obbiettivi qualificanti della Strategia Forestale Nazionale (SFN). In questa nota abbiamo ragionato su approcci di selvicoltura adattativa, nell’idea che interventi di regolazione della competizione e approcci colturali volti incentivare la diversità funzionale in una rete di accresciute connessioni strutturali, siano un modo per favorire la capacità della foresta di fronteggiare fenomeni estremi come le ondate di siccità e calore. Si parla spesso, nei documenti di indirizzo, delle foreste come “capitale naturale” da difendere e valorizzare. Per noi questo implica, anzitutto, investimenti sul “capitale umano” che ruota intorno alla foresta, nelle sue varie componenti: formazione, professionalità, proprietà e imprenditorialità. La sfida è infatti quella di coniugare, in una strategia “win-win” la gestione forestale adattativa, per sua natura spesso non finanziariamente redditizia nel breve periodo, con il diritto dei proprietari boschivi (pubblici e privati) di trarre beneficio dai loro beni e di fare impresa fruttuosa anche nelle ricadute ambientali e sociali.
Ringraziamenti
Lavoro svolto con il contributo del progetto: “Advanced EO Technologies for studying Climate Change impacts on the environment - OT4CLIMA” finanziato dal MIUR, D.D. 2261del 6.9.2018, PON R&I 2014-2020 & FSC.
References
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar