Preliminary antagonistic tests of endophytic fungi against Diplodia corticola and silvicultural practices to contrast oak decline
Forest@ - Journal of Silviculture and Forest Ecology, Volume 3, Pages 78-85 (2006)
doi: https://doi.org/10.3832/efor0351-0030078
Published: Mar 17, 2006 - Copyright © 2006 SISEF
Research Articles
Guest Editors: 5° SISEF Congress (Grugliasco, TO - 2005)
« Forests and Society - Changes, Conflicts, Sinergies »
Collection/Special Issue: E. Lingua, R. Marzano, G. Minotta, R. Motta, A. Nosenzo, G. Bovio
Abstract
In southern Italy, many oak stands have been affected by the decline syndrome attributed to several biotic and abiotic causes. Various fungal microorganisms, such as Diplodia corticola A.J.L. Phillips, Alves & Luque, were found to be associated with the syndrome, demonstrating either an endophytic asymptomatic or a pathogenetic behaviour, or both, in succession. The objective of this study was to examine a first series of in vitro tests conducted on the antagonistic activity of some endophytic fungi belonging to the species Trichoderma viride Pers.: Fries, Epicoccum nigrum Link., Fusarium tricinctum (Corda) Sacc., Alternaria alternata (Fries) Keissler, Sclerotina sclerotiorum (Libert) De Bary and Cytospora sp. towards D. corticola. These endophytic fungi were obtained from four declining oak woods in Southern Italy. A secondary aim was to define a correct silvicultural interventions to contain decline in the oak stands from which the fungi were extracted.
Keywords
Oak, Decline, Fungi, Endophyte, Silvicultural treatment, Southern Italy
Introduzione
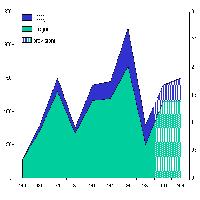
Il genere Quercus nelle regioni temperate e temperato-calde dell’emisfero boreale, comprende circa 300 specie di alberi e arbusti con foglie persistenti, semipersistenti o caduche, molte delle quali sono diffuse in Europa. In Italia, le formazioni più diffuse sono proprio rappresentate dai boschi a prevalenza di specie caducifoglie del genere Quercus (27% della superficie forestale totale), seguono i boschi a prevalenza di Fagus sylvatica L. (12%) e quelli di altre latifoglie mesofite e mesotermofite (12%) a prevalenza di specie del genere Acer, Carpinus, Ostrya e Fraxinus ([6] - Tab. 1). Negli ultimi decenni le cenosi quercine sono state interessate da una grave sindrome nota come “deperimento delle querce”, diffusa nell’intero areale italiano delle querce ed in quello di numerosi Paesi europei ed extraeuropei (Fig. 1 - [19], [26], [29], [32], [34]). In Italia le specie più interessate dal deperimento sono Quercus cerris L. e Q. pubescens Willd. che costituiscono cedui puri e/o misti, nonché, fustaie di grande valore naturalistico e paesaggistico nell’Appennino meridionale. I fattori coinvolti nel deperimento sono numerosi, e di diversa natura: abiotici, biotici ed antropici, che assumono ruoli diversi, agendo come predisponenti (abbandono o errata conduzione colturale, pascolamento irrazionale, condizioni edafiche sfavorevoli, competizione radicale, anomalie meteoriche), scatenanti (susseguirsi di annate siccitose, diffusione di parassiti animali e vegetali particolarmente aggressivi) o concomitanti (incendi, tagli abusivi, diffusione di parassiti di debolezza capaci di aggravare lo stato di salute di piante già fortemente debilitate - [19], [22]). Tra i fattori biotici che assumono rilevanza ci sono alcuni funghi endofiti capaci di comportarsi da patogeni di debolezza fra cui Diplodia corticola A.J.L. Phillips, Alves & Luque,Biscogniauxia mediterranea (De Not.), O. Kuntze, Discula quercina (West) von Arx e Phomopsis quercina (Sacc.) Höhn ([2], [11], [15]). Ad altri funghi endofiti appartenenti ai generi Acremonium, Cytospora, Epicoccum, Fusarium e Trichoderma sono attribuite proprietà antagonistiche nei confronti dei suddetti patogeni ([10]; [28]; [20]). Nel campo forestale l’impiego di fungicidi e, più in generale di fitofarmaci di natura chimica è da sempre circoscritto all’ambito vivaistico, e alla forme più intensive di arboricoltura da legno, per ragioni non solo tecnico-economiche ma soprattutto di ordine ambientale, per gli effetti deleteri che l’uso indiscriminato degli stessi produrrebbe sugli ecosistemi forestali ([14]). Considerate le peculiari caratteristiche del nostro territorio boschivo, in gran parte collinare e montano, l’importanza strategica del patrimonio forestale nazionale ed il ruolo polifunzionale di molti popolamenti di conifere e latifoglie (naturali o seminaturali), la lotta biologica contro gli organismi nocivi alle piante forestali rappresenta una prospettiva di difesa potenzialmente in grado di garantire una protezione eco-compatibile del patrimonio boschivo. Risultati promettenti sono stati ottenuti, di recente, utilizzando funghi antagonisti in prove di lotta biologica contro i marciumi radicali delle piante forestali da Heterobasidion annosum Fr. (Bref). e Armillaria spp. ([3], [27]). In particolare, per H. annosum l’attività antagonistica dei basidiomiceti lignicoli Hypholoma fasciculare (Huds.: Fr.) Kummel e Ptychogaster rubescens Bound, emersa in prove preliminari, è stata confermata da risultati ottenuti in prove in vivo utilizzando come riferimento positivo anche un isolato fungino di Phlebiopsis gigantea (Fr.) Jülich, un antagonista già commercializzato nell’Europa settentrionale con la denominazione Rotstop ([33]). Anche contro il cancro corticale del castagno da Cryphonectria parasitica (Murr.) Barr sono stati eseguiti numerosi interventi di lotta biologica basati sulla diffusione di ceppi ipovirulenti locali del patogeno ([35], [4], [24]).
Tab. 1 - Estensione delle superfici forestali italiane suddivise in tipologie fisionomiche in Italia ([6]).
| Categoria fisionomica | Superficie | |
|---|---|---|
| ha | % | |
| Boschi a prevalenza di querce caducifoglie | 2.134.733 | 27 |
| “ “ altre latifoglie mesofite e mesoxerofite native | 973 | 12 |
| “ “ faggio | 960 | 12 |
| “ “ abete bianco e/o rosso | 779 | 9 |
| “ “ leccio e sughera | 781 | 9 |
| Macchia bassa e garighe | 715 | 9 |
| Boschi a prevalenza di pini montani e oromediterranei | 404 | 5 |
| “ “ larice e/o pino cembro | 298 | 3 |
| Macchia alta | 278 | 3 |
| Boschi a prevalenza di castagno | 158 | 3 |
| “ “ pini mediterranei | 157 | 2 |
| “ “ latifoglie non native | 135 | 1 |
| “ “ latifoglie igrofite | 73 | 0 |
| “ “ conifere non native | 11 | 0 |
| Totale | 7.862.937 | 100 |
Scopo del presente lavoro, condotto nell’ambito del Progetto Nazionale “Ruolo degli endofiti fungini nel deperimento delle querce”, è stato quello di valutare l’attività antagonistica di alcuni endofiti appartenenti alle specie T. viride, E. nigrum, F. tricinctum, A. alternata, S. sclerotiorum e al genere Cytospora sp. verso D. corticola riscontrati in precedenti studi in 4 boschi deperienti. Nella presente nota sono riportate anche le indicazioni gestionali da adottare negli stessi boschi.
Materiali e Metodi
Boschi esaminati e isolati fungini utilizzati
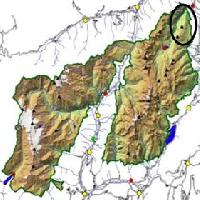
In 4 boschi dell’Italia meridionale, oggetto di studi da alcuni anni per il reperimento della micoflora endofitica associata al deperimento delle querce ([25]), sono stati effettuati dei sopralluoghi allo scopo di valutare le condizioni ecofisiologiche dei soprassuoli considerati. I suddetti boschi sono ubicati in quattro regioni dell’Italia meridionale: Basilicata (Bosco Grancia, Brindisi di Montagna, Potenza), Campania (Valle Franca, Dragoni, Caserta), Calabria (Bosco della Cava, San Donato di Ninea, Cosenza) e Puglia (Difesa Grande, Gravina in Puglia, Bari). Le principali caratteristiche stazionali di tali querceti e gli indici di deperimento sono riportati in Tab. 2. Il “Bosco Grancia” è un ceduo di Q. cerris (60 %) e Q. pubescens (40 %) rado e pascolato di circa 50 anni di età con sottobosco di Crataegus monogyna Jacq., Ligustrum vulgare L., Rosa canina L., Cystus scoparius Lk. e Asparagus acutifolius L. Il “Bosco della Cava”, è un ceduo invecchiato di Q. cerris (55 %) e Q. pubescens (45 %) rado e pascolato, di circa 40 anni di età in cui si rinviene Ostrya carpinifolia Scop., C. monogyna, Pyrus amygdaliformis Vill. e Spartium junceum L. Il bosco “Difesa Grande” è un ceduo di oltre 40 anni di età avviato a fustaia costituito mediamente da Q. cerris (40 %), Q. frainetto Ten. (40 %) e Q. pubescens (20 %), con sottobosco a prevalenza di Sorbus domestica L., L. vulgare, C. monogyna, e Cystus villosus P. Il bosco “Valle Franca”, è un ceduo matricinato di Q. cerris (80 %) e Q. pubescens (20 %) in cui si rinviene anche la presenza di Fraxinus ornus L., S. domestica, C. monogyna e Ruscus aculeatus L. Nei suddetti querceti la chioma delle specie quercine presenti è popolata da una comunità di funghi endofiti che include miceti ad attività patogenetica più o meno spiccata (D. corticola, D. quercina) ed altri quali T. viride, E. nigrum, F. tricinctum, A. alternata, S. sclerotiorum e Cytospora sp. ad attività potenzialmente antagonistica (Ubaldo et al. dati in corso di pubblicazione).
Tab. 2 - Caratteristiche stazionali dei querceti indagati e indici di deperimento medio. a = Dati forniti dal Servizio Idrografico della Presidenza del Consiglio dei Ministri, Ufficio di Bari (a’) e Napoli (a’’); b = Da Cantore et al. ([9]); c = Da Ciancio ([12]).
| Località | Ordinamento colturale | Altitudine (m s.l.m.) | Esposizione prevalente | Pendenza media (%) | T media (°C) | Precipitazione media annua (mm) |
Indice di deperimento medio |
|---|---|---|---|---|---|---|---|
| “Difesa Grande” Gravina in Puglia (Bari) | Ceduo invecchiato | 450 | SE | 10 | 15.0 (a’) |
610 (a’) |
1 |
| “Valle Franca” Dragoni (Caserta) | Ceduo matricinato | 480 | SW | 30 | 14.0 (a’’) |
1320 (a’’) |
0 |
| “Bosco Grancia” Brindisi di Montagna (Potenza) | Ceduo invecchiato | 750 | SE | 35 | 12.5 (b) |
790 (b) |
1 |
| “Bosco della Cava” San Donato di Ninea (Cosenza) | Ceduo invecchiato | 850 | NE | 45 | 12.5 (c) |
1590 (c) |
1 |
Valutazione dell’attività antagonistica in vitro di funghi endofiti contro D. corticola
L’attività antagonistica di T. viride, E. nigrum,F. tricinctum, A. alternata, S. sclerotiorum e Cytospora sp. verso D. corticola è stata valutata utilizzando due metodologie: il metodo degli accrescimenti ([1]) e quello delle interazioni ifali ([5]). Per entrambi i metodi per ogni coppia di microrganismi da saggiare (antagonista/patogeno) sono state allestite cinque piastre Petri contenenti ciascuna 20 ml di agar-patata-destrosio (PDA). In ciascuna piastra così preparata sono stati collocati sterilmente due cilindretti di agar di 6 mm di diametro, posti equidistanti dal bordo della piastra e tra loro colonizzati, rispettivamente, dal micelio dell’antagonista da saggiare e del patogeno. Tali cilindretti sono stati prelevati dal margine di piastre madri di 4 giorni di età. Nel testimone il micelio di D. corticola è stato confrontato con agar sterile; le piastre così ottenute sono state incubate in termostato a 25 °C ed in assenza di luce. Per il metodo degli accrescimenti, dopo 24 ore dall’inoculazione è stato misurato l’accrescimento radiale delle due colonie lungo due direttrici tra loro ortogonali. I rilievi sono continuati fino a quando le colonie del testimone raggiungevano il margine della piastra. L’inibizione percentuale dell’accrescimento (I) è stata calcolata applicando la seguente formula (eqn. 1):
Tab. 3 - Caratteristiche delle interazioni ifali e valori numerici attribuiti secondo la scala di Badalyan et al. ([5]).
| Tipologie di interazioni ifali |
Caratteristiche | Valori numerici |
|---|---|---|
| A | Arresto della crescita delle colonie per contatto con reciproca inibizione. | 1 |
| B | Arresto a distanza senza contatto miceliare. | 2 |
| C | Crescita di una colonia sull’altra senza arresto iniziale. | 3 |
| CA1 | Parziale crescita di una colonia sull’altra dopo arresto iniziale per contatto. | 3 |
| CA2 | Completa crescita di una colonia sull’altra dopo arresto iniziale per contatto. | 4 |
| CB1 | Parziale crescita di una colonia sull’altra dopo arresto iniziale a distanza. | 4 |
| CB2 | Completa crescita di una colonia sull’altra dopo arresto iniziale a distanza. | 5 |
dove r.m. è il raggio delle colonie in direzione dell’antagonista e R.M. è la media dei tre raggi della colonia nelle altre direzioni. I dati ottenuti sono stati elaborati statisticamente, previa trasformazione angolare, mediante Anova e test di Duncan. Nel metodo delle interazioni ifali, ogni due giorni sono state valutate le tipologie di interazioni tra i funghi antagonisti e D. corticola per un periodo complessivo di due mesi. A tal fine è stata considerata una scala proposta da Badalyan et al. ([5]) (Tab. 3) e l’indice di antagonismo (I.A.) è stato calcolato utilizzando la seguente formula (eqn. 2):
dove N è la frequenza di ciascuna tipologia di interazione e V è il valore numerico attribuito alla tipologia di interazione.
Risultati
Nei querceti oggetto di studio sono state riscontrate condizioni edafiche non ottimali, cure colturali inadeguate e un progressivo stato di abbandono, con conseguente diminuzione della resistenza delle piante verso i funghi endofiti patogeni come D. corticola. I boschi più colpiti dal deperimento sono i cedui invecchiati, specialmente se abbandonati e non avviati ad alto fusto. Infatti la conversione del ceduo a fustaia rappresenta l’obiettivo prioritario da conseguire, ma richiede una fase transitoria di interventi tesi alla graduale e tempestiva riduzione del numero dei polloni. Il semplice abbandono può costituire un momento assai critico, soprattutto per quei popolamenti che già versano in condizioni di scarsa vigoria vegetativa ([13]). È noto, infatti, che in condizioni pedoclimatiche estreme i boschi cedui, invecchiando vanno incontro ad una precoce stasi incrementale sintomatica di uno squilibrio sempre più accentuato tra apparato radicale e parte epigea che può sfociare in manifestazioni fitopatologiche ma che potrebbe invece essere mitigata da opportuni diradamenti ([21], [23], [7], [8]). Pertanto, allo scopo di mantenere il più possibile gli ecosistemi forestali in equilibrio e contenere il deperimento, grande importanza assumono gli interventi selvicolturali, che si possono riassumere essenzialmente in: diradamento dei soprassuoli più densi, con bruciatura e/o allontanamento di materiale legnoso non utilizzabile; tramarrature di ceppaie intristite; avviamento alla conversione dei cedui invecchiati con rilascio delle migliori matricine e rinfoltimento delle radure ricche di vegetazione erbacea eliofila. La valutazione dell’attività antagonistica dei funghi endofiti verso D. corticola ha dato risultati differenti con i due metodi. I risultati ottenuti con il metodo degli accrescimenti, riportati in Tab. 4, evidenziano che l’isolato T. viride è particolarmente efficace nel ridurre lo sviluppo miceliare di D. corticola, mentre modesta è stata la riduzione causata da tutti gli altri funghi, con l’eccezione di F. tricinctum che non ha ridotto in maniera significativa la crescita di D. corticola (Fig. 2). Nello studio delle interazioni fra le colonie sono state osservate 3 tipologie di interazioni: CA2, CB1, e A, a conferma di quelle riscontrate da Badalyan et al. ([5]) (Tab. 5). Con F. tricinctum l’interazione di tipo CB1 è stata preceduta da un arresto a distanza 4 giorni dopo l’inoculazione e, successivamente, da una crescita parziale sulle colonie di D. corticola. Sebbene tutti i funghi abbiano mostrato una certa attività antagonistica, questa è risultata elevata da parte di F. tricinctum e T. viride, più moderata da parte degli altri funghi (vedi Tab. 5). I differenti risultati conseguiti possono essere spiegati considerando l’impostazione delle prove sperimentali. Nel metodo degli accrescimenti ifali la valutazione dell’interazione patogeno/antagonista è stata effettuata misurando gli accrescimenti radiali delle due colonie e pertanto il parametro più importante per la valutazione dell’attività antagonistica è stato la velocità di accrescimento delle colonie fungine. Di conseguenza T. viride, con velocità di crescita uguale a quella del testimone, ha manifestato una efficace competitività, mentre F. tricinctum, caratterizzato da un accrescimento più lento, ha evidenziato un’attività antagonistica quasi nulla. Nel secondo metodo sono state considerate solo le interazioni ifali patogeno/antagonista e quindi isolati fungini come T. viride e F. tricinctum, nonostante le velocità di crescita differenti, hanno mostrato, entrambi, elevata capacità di contenimento. In base ai risultati ottenuti il metodo delle interazioni ifali è risultato il più efficace per la valutazione delle proprietà antagonistiche degli isolati fungini.
Tab. 4 - Percentuali di riduzione dell’accrescimento radiale delle colonie di D. corticola determinata dai funghi antagonisti. Sulle colonne, a valori seguiti dalla medesima lettera, corrispondono valori significativamente non differenti per p=0.05, secondo il test di Duncan; *: Colonie di D. corticola cresciute in assenza di antagonisti.
| Funghi antagonisti | D. corticola Riduz. accr. (%) |
|---|---|
| T. viride | 28.5 A |
| Cytospora sp. | 19.2 AB |
| E. nigrum | 16.7 AB |
| A. alternata | 9.5 AB |
| S. sclerotiorum | 5.7 AB |
| F. tricinctum | 4.2 BC |
| Testimone* | 0.0 C |
Fig. 2 - Interazioni ifali tra colonie di D. corticola e di Cytospora sp., T. viride e F. tricinctum di tipo A (in alto a sinistra), di tipo CA2 (in alto a destra) dopo 30 giorni di incubazione e di tipo CB1 dopo 8 giorni (in basso a sinistra) e dopo 30 giorni (in basso a destra) allevate in capsule Petri contenenti un substrato agarizzato incubate in termostato a 23±1 °C.
Tab. 5 - Tipologie di interazioni ifali e valori dell’indice di antagonismo riscontrati in vitro tra alcuni antagonisti e D. corticola.
| Combinazione antagonista/patogeno |
Tipologia di interazione ifale |
Indice di antagonismo |
|---|---|---|
| T. viride / D. corticola | CA2 | 18 |
| F. tricinctum / D. corticola | CB1 | 16 |
| Cytospora sp. / D. corticola | A | 4 |
| E. nigrum / D. corticola | A | 4 |
| A. alternata / D. corticola | A | 4 |
| S. sclerotiorum / D. corticola | A | 4 |
Discussione
I soprassuoli quercini indagati hanno evidenziato i segni di un diffuso e generalizzato deperimento fisiologico verificatosi alla fine degli anni ’90-inizio del 2000, (piante disseccate, deperienti, emissione di rami epicormici lungo il fusto, accrescimenti vegetativi stentati, clorosi fogliare, chioma trasparente ecc.). A tal proposito risulta quanto meno opportuno effettuare tagli fitosanitari e tramarrature di vecchie ceppaie per consentire l’emissione di polloni vigorosi e sani e migliorare in tal modo le condizioni ecofisiologiche dei soprassuoli considerati. Campanile & Manicone ([7]), hanno dimostrato l’effetto positivo dei tagli fitosanitari e delle tramarrature di ceppaie in alcuni querceti deperienti della Puglia, in agro di Cassano delle Murge (Bari), di Laterza e Mottola (Taranto), ecc. Tali interventi di riduzione della densità del soprassuolo hanno incrementato le disponibilità idriche e trofiche delle singole piante che risultano quindi più vigorose e resistenti alle annate particolarmente siccitose. Il deperimento è più grave nei boschi non trattati selvicolturalmente rispetto ad altri, nelle stesse condizioni, ma trattati razionalmente ([18]). Sempre nell’ambito delle misure dirette alla prevenzione del deperimento, si ribadisce ancora una volta l’opportunità da parte dei tecnici forestali di riconsiderare sotto l’aspetto ecologico-selvicolturale, i vari motivi che per molto tempo hanno portato a trascurare l’applicazione delle classiche norme di igiene forestale. Tra le numerose azioni che in passato venivano eseguite nei boschi, si ricordano quelle che prevedevano il tempestivo allontanamento di piante, o parti di esse, morte o seriamente danneggiate da avversità climatiche o biotiche ([16], Manicone et al. 1993). Su queste scelte sicuramente ha influito l’onerosità delle stesse operazioni. Dallo screening effettuato in vitro è emerso che T. viride e F. tricinctum hanno esplicato una elevata azione antagonistica verso D. corticola. Se questi risultati saranno confermati in planta, in serra e in pieno campo, sarà possibile mettere a punto tecniche di lotta biologica contro endofiti coinvolti nel deperimento delle querce. A tal fine sarà opportuno caratterizzare i metaboliti prodotti da T. viride e F. tricinctum e studiare la capacità di penetrazione attiva o passiva degli stessi all’interno della pianta. Ricerche fatte da Schulz e colleghi ([30], [31]), su un gran numero di endofiti di piante erbacee e arboree hanno dimostrato che la produzione in coltura di metaboliti secondari supera almeno due volte quella di funghi fitopatogeni isolati dalle stesse piante. Gli autori hanno altresì dimostrato che questi metaboliti possono influire positivamente sulle attività fisiologiche della pianta esercitando un’azione protettiva con la produzione di metaboliti attivi verso parassiti vegetali e animali. Chiarire le complesse interazioni tra piante e funghi endofiti e i meccanismi biochimici e fisiologici che le determinano, così come è avvenuto per i funghi fitopatogeni negli ultimi decenni, rimane uno dei principali obiettivi della ricerca in questo campo ([17]). Nella consapevolezza che almeno nel breve termine per contenere il fenomeno del deperimento, sia improponibile un ricorso esclusivo ai mezzi biologici, sono da privilegiare gli interventi selvicolturali. Infatti, una corretta gestione forestale meno legata a rigidi schemi, bensì più attenta alle variabili auxometriche e alle condizioni stazionali, assicurerebbe alle piante le migliori condizioni possibili per ostacolare il comportamento patogenetico di alcuni funghi endofiti come D. corticola.
References
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar