Does a universal scaling factor for plant respiration exist?
Forest@ - Journal of Silviculture and Forest Ecology, Volume 3, Pages 12-14 (2006)
doi: https://doi.org/10.3832/efor0356-0003
Published: Mar 17, 2006 - Copyright © 2006 SISEF
Commentaries & Perspectives
Abstract
A recent study based on data from 500 laboratory and field-grown plants (43 species, 4 experiments), published in the journal Nature, questioned the validity of the 3/4 scaling law for organism metabolism in the case of plants, proposing rather an isometric scaling and nitrogen as a key factor for respiratory scaling. The main results of the paper are briefly presented and commented.
Keywords
Tradizionalmente, gli studi di fisiologia ed ecofisiologia vegetale si sono concentrati molto di più sui processi fotosintetici che sulla respirazione. Questo sia per motivazioni di carattere scientifico che, probabilmente, per maggiori difficoltà nella misura della respirazione, che non è limitata ad un solo organo (le foglie, nel caso della fotosintesi), è il risultato di più processi (mantenimento, crescita) ed è più difficile da modellizzare. In effetti, ad oggi, esiste un modello biochimico della fotosintesi universalmente accettato ([2], [8]) mentre non ne esiste uno analogo per la respirazione, in genere collegata empiricamente a fattori quali la biomassa o, più meccanicisticamente, al contenuto di azoto ([7], [5], [10]).
Nel passato, ci sono stati tentativi di interpretare e spiegare i tassi metabolici delle piante tramite una legge universale [Y = Y0 Mb, dove Y è il tasso metabolico, Y0 una costante di normalizzazione, M è la massa dell’organismo e b il fattore di scala, ([6])], ed alcuni ricercatori hanno proposto che la relazione tra respirazione e dimensioni, legge fondamentale per il regno animale, fosse valida anche per le piante, con lo stesso fattore di scala dei 3/4 ([3], [1]). Tali studi, però, erano limitati nel numero di piante o parti di esse utilizzato (20), rendendo necessari successivi approfondimenti che includessero un campione maggiore con più generi, tipologie e condizioni ambientali sperimentate.
In un articolo apparso recentemente sulla rivista Nature ([6]), 4 ricercatori forestali, utilizzando dati di quattro esperimenti, con circa 500 piante, di 43 specie sia arboree che erbacee, cresciute in serra, camera di crescita o in bosco, tra 1 e 25 anni di età, hanno rianalizzato la questione, giungendo a conclusioni interessanti e diverse rispetto a quelle della relazione universale tra respirazione e massa con un fattore 3/4.
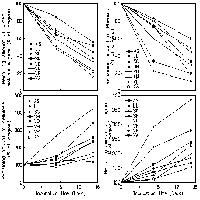
Reich e colleghi hanno misurato la respirazione autotrofa al buio, sia in piante intere che nelle diverse componenti separate (radici, fusti, foglie), in diverse condizioni ambientali (luce, temperatura, concentrazioni di CO2, fertilizzazione) verificando che, per i singoli esperimenti, esisteva una relazione lineare (su scala logaritmica) tra respirazione e biomassa totale delle piante (e tra respirazione epigea e biomassa epigea) e che questa relazione era tendenzialmente isometrica, vale a dire il fattore di scala era circa 1, comunque significativamente diverso da 3/4. Tali relazioni, sebbene con esponente non significativamente diverso tra loro, non erano però riconducibili, statisticamente, ad un’unica relazione tra respirazione e biomassa, in contrasto, quindi, con una legge universale.
Il punto più interessante del lavoro, e forse più rilevante per l’ecologia e l’ecofisiologia vegetale, è l’analisi successiva: infatti, quando la respirazione (totale o epigea) è stata messa in relazione al contenuto di azoto (totale o epigeo) delle piante i ricercatori hanno verificato che la relazione trovata era unica per tutti i generi, tipologie, condizioni ambientali ed esperimenti considerati. Tale relazione, sebbene meno significativa, si mantiene anche tra respirazione specifica (per unità di massa) e concentrazione di azoto. I risultati sono quindi in accordo con il ruolo fondamentale dell’azoto nella biochimica della respirazione autotrofa, che è legata ad enzimi ricchi di azoto ed alla disponibilità di substrato (legata a meccanismi source-sink con la fotosintesi - [6]).
Il contenuto di azoto nelle piante non è solamente legato alla loro dimensione ma è determinato da un ciclo complesso che coinvolge anche processi di riassorbimento e riallocazione: non è quindi in relazione semplice e diretta con la struttura della rete vascolare, la cui geometria “frattale” è stata invocata per spiegare la relazione universale tra respirazione e dimensioni degli organismi ([9], [1]).
Un ulteriore elemento che può spiegare la mancanza di una relazione universale tra respirazione e dimensioni valida per il regno animale e quello vegetale è il fatto che le piante, in particolare quelle arboree, diversamente dagli animali, accumulino, nel tempo, massa morta, riallochino nutrienti tra le componenti e siano soggette a fenomeni di competizione fondamentalmente diversi da quelli del regno animale. In relazione a questo, Hedin ([4]), nello stesso numero di Nature, nella rubrica News & Views dedicata all’articolo di Reich e colleghi, segnala che per lo studio in questione (che è limitato ad alberi piccoli come piante in vaso, semenzali di qualche anno o alberi di dimensione ridotta) andrà verificata l’estendibilità dei risultati a piante adulte, per le quali non è semplice la misura della respirazione e l’estrapolazione dei dati alla biomassa intera.
Tra gli altri aspetti interessanti per l’ecologia forestale che si possono ricavare dai dati presentati nell’articolo, si segnala il fatto che gli alberi cresciuti in bosco rispetto alle piante in serra o camera di crescita abbiano una respirazione minore a parità di biomassa: questo può essere legato ad una maggior presenza di tessuti con tassi di respirazione più bassi (come i fusti), ma anche ad una maggiore efficienza d’uso dell’azoto rispetto alle piante cresciute in ambiente controllato e, probabilmente, fertilizzate. Inoltre, analizzando i dati per specie forestali, il fattore di scala tra respirazione e biomassa totale di specie tipicamente pioniere (Betula spp., Populus tremuloides) risulta sistematicamente più basso delle altre specie (0.71-0.93 rispetto a 0.93-1.30, sebbene non sia possibile dire se la differenza sia significativa): in pratica queste specie, a parità di biomassa o all’aumentare della stessa, respirano proporzionalmente di meno rispetto a specie di stadi successionali più avanzati.
In conclusione, il lavoro di Reich e colleghi contribuirà sicuramente al dibattito tra ecologi e fisiologi sulla esistenza di leggi universali sul metabolismo in biologia ([4]) ma, sicuramente, costituisce un ulteriore passo avanti verso una migliore comprensione della fisiologia della respirazione e per la sua modellizzazione.
References
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar