Management of genetic resources in the nursery system of wild cherry (Prunus avium L.)
Forest@ - Journal of Silviculture and Forest Ecology, Volume 3, Pages 496-510 (2006)
doi: https://doi.org/10.3832/efor0416-0030496
Published: Dec 18, 2006 - Copyright © 2006 SISEF
Research Articles
Abstract
Knowledge of genetic and adaptive traits of reproductive materials used in the nursery system of wild cherry, could be an useful instrument to improve ecological and economic sustainability of plantation ecosystems. This work reports results from a research which the objectives were: 1) to study the genetic variation of a Prunus avium L. Population, used for seed harvesting, through its multi-locus genotypes detected by starch gel electrophoresis; 2) to analyze the level of genetic variation within and among different steps in a commercial nursery system (basic population and sub-populations, seedlings aged S1 T1 and S1 T2, plantation). Results showed low genetic variation levels of the basic population, similar to a reference system of other 12 wild cherry Italian populations and to other French and Caucasian materials. The genetic distances among Monte Baldo and some closer Lombardy provenances (Area Garda, Bosco Fontana, Valtellina) were smaller than the Venice Region populations (Monti Lessini and Asiago). Number of alleles and percentage of polymorphic loci within the complex of Monte Baldo provenance and multiplication materials were similar, whilst a variable value of Fis was noted. Indeed, along with the nursery system until the plantation, heterozygosis initially (S1 T1) increased, then decreased proceeding to the plantation. This fluctuation of FIS values could be determined by seed lots characterized initially by higher levels of variation, due to self-incompatibility. In the following steps, a possible selection pressure can affect randomly the genotypic structure of wild cherry by increasing the homozygosity. There is not among population a well defined geographic characterization, as suggested by genetic distances, therefore homogeneous seed harvest could be established an area larger than geographic and administrative borders. On this way we could have reproductive material with a wide genetic base and environmental adaptability. To increase variability in the progenies, populations characterised by wider cross pollination rates should be selected, harvest seed by all plants of population, reduce selection on seedlings during nursery growth.
Keywords
Introduzione
L’adattabilità e la sostenibilità di un ecosistema naturale o artificiale è legato al livello di diversità in esso presente ([31], [46]). Questa assume grande importanza nelle specie forestali poiché, a causa della lunghezza del loro ciclo biologico, sono maggiormente esposte a rischi determinati dall’ambiente circostante. Un’ampia variabilità genetica conferisce alle popolazioni naturali ed alle piantagioni migliore plasticità evolutiva e di adattamento ai possibili cambiamenti ambientali, sia biotici che abiotici.
Il mantenimento di sufficienti livelli di variabilitàè, quindi, uno degli elementi principali che deve considerare chi opera in vivaistica forestale. A questo scopo diventa fondamentale una corretta gestione della filiera e va posta particolare attenzione nell’individuazione dei materiali di base, nella loro raccolta e conservazione, nell’allevamento in vivaio.
In generale, sino ad oggi non ci si è posti il problema di monitorare la variabilità o le possibili alterazioni delle risorse genetiche durante il loro percorso nella filiera vivaistica e, le scarse conoscenze sulle caratteristiche genetiche ed ecologiche del germoplasma di base impiegato, possono aver contribuito all’insorgere di problemi di adattamento osservati in molte piantagioni.
Il primo passo per creare le premesse per una buona gestione delle risorse forestali è la caratterizzazione ecologica e genetica delle specie, poiché consente non solo di individuare materiali di base adeguati alle caratteristiche degli ambienti in cui si opera, ma anche di poterli certificare, come richiesto dalla Direttiva europea 1999/105/CE ([4]) e dal DLgs 386/2003 ([19]). La definizione di regioni di provenienza (per le specie a maggiore distribuzione sul territorio) o di aree di raccolta (per le specie sporadiche e per i popolamenti misti), dalle quali raccogliere materiali forestali di moltiplicazione, permette di stabilire una base formale di approvvigionamento del seme, la conservazione del patrimonio genetico in situ e, quindi, di intraprendere attività capaci di limitare l’erosione delle risorse stesse.
Esiste, tuttavia, un altro importante punto focale in cui verificare l’eventuale perdita di diversità: le tecniche di produzione vivaistica ed il loro effetto sulla variabilità del postime rispetto a quello della popolazione di partenza.
Da questa esigenza si è sviluppato il presente lavoro, il cui obiettivo è verificare e quantificare l’eventuale riduzione di variabilità genetica nel materiale di propagazione ottenuto da una popolazione di Prunus avium L. impiegata usualmente per la raccolta di seme (vedi capitolo: “Note al lavoro”).
È stato scelto il ciliegio selvatico poiché, tra le latifoglie nobili, è per il momento una delle più usate e più studiate per gli aspetti genetici ([11], [9], [1]).
In ambiente mediterraneo non è possibile identificare popolazioni pure, estese e continue di P. avium, ma solo piccoli gruppi (costituiti generalmente da poche piante madri e dai loro polloni radicali), o piante isolate ([7], [36], [40], [18], [10]). In natura, infatti, il ciliegio selvatico può presentare due diversi comportamenti: nei primi stadi successionali può essere una specie colonizzatrice, propagandosi rapidamente per polloni radicali, mentre in ecosistemi forestali più maturi (vicini al climax), partecipa alla formazione di cenosi miste, grazie alla disseminazione zoocora del seme ([21]).
In Italia P. avium è ampiamente diffusa nella parte subalpina dell’areale naturale, dove ne sono stati individuati gruppi più o meno ampi all’interno di boschi misti ([35]), mentre nelle aree appenniniche le popolazioni coprono superfici più ristrette, sono più isolate, concentrate frequentemente nei fondovalle freschi e formate da pochi individui. Anche i trattamenti selvicolturali possono influenzarne la distribuzione, favorendo ad esempio nei cedui la propagazione vegetativa per polloni radicali rispetto a quella generativa, più frequente in soprassuoli più naturaliformi.
Materiali e Metodi
La filiera vivaistica
L’analisi della variabilità e della differenziazione genetica è stata effettuata su tre livelli della filiera vivaistica commerciale:
- la popolazione di base impiegata per la raccolta del seme;
- il postime allevato in vivaio di due diverse classi di età (S1 T1 e S2 T2);
- la piantagione.
Il materiale vegetale
La popolazione madre scelta è situata sul versante occidentale del Monte Baldo (VR), ed è una tra quelle usualmente impiegate per la produzione di postime commerciale in quel distretto geografico. Essa è costituita da due sotto-popolazioni, che presentano le caratteristiche strutturali tipiche del ciliegio, identificate come A e B. La popolazione A, comprendente 15 piante madri, è situata a valle, in località Lumini, comune di S. Zeno di Montagna (VR), ad una altitudine di 750 - 679 m. La popolazione B è invece localizzata più a monte, tra le località Senaga, Prada e Le Fasse, ad una altitudine compresa tra 1009 e 560 m ed è composta da 16 piante madri.
Il Monte Baldo (45° 35’ di latitudine Nord e 10° 46’ di longitudine Est) è situato nelle Prealpi Venete e costeggia il Lago di Garda. Dal punto di vista climatico, ricade nella fascia meridionale e periferica della regione alpina. Può, perciò, risentire sia del clima sub-continentale della Pianura Padana, che di quello temperato freddo della zona alpina ([47], [24]). A 1000 m di quota le temperature medie annue sono pari a circa 8°C (di poco superiori ad 1°C a gennaio ed inferiori a 18°C a luglio) e le precipitazioni medie annue sono stimate tra 1200 e 1300 mm.
Le 31 piante madri scelte per la raccolta del seme sono quasi tutte coetanee (età media 50 anni circa) e derivano dalla colonizzazione di prati, oggi lentamente riconquistati dal bosco. Nella zona di Prada la vegetazione arborea è prevalentemente costituita da ceduo di faggio, mentre a Lumini sono presenti castagno, acero e frassino maggiore. I singoli individui utilizzati per la raccolta del seme distano fra di loro almeno 50 m.
Lo studio della variabilità genetica è stato eseguito su gemme in riposo vegetativo, tramite elettroforesi orizzontale su gel di amido. Sono state analizzate: 31 piante madri; 40 trapianti S1 T1 (scelti a casualmente tra quelli prodotti nel vivaio di Dogana di Peri nel 2001) e 40 trapianti S1 T2 (anno di semina 2000); 60 individui della piantagione di Grezzana (VR), realizzata con postime di provenienza Monte Baldo.
La popolazione di riferimento
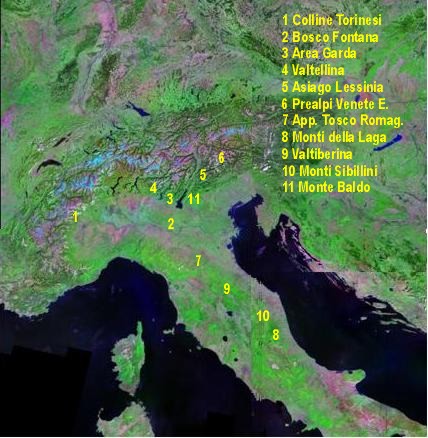
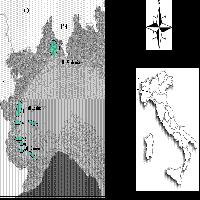
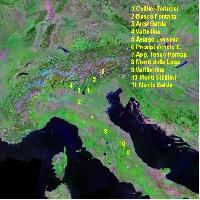
I dati ottenuti sono stati confrontati con 10 popolazioni italiane di P. avium ([11], AA.VV. 2005a), selezionate nel Nord e nel Centro-Sud Italia ([7] - Fig. 1).
Secondo la densità e l’ampiezza delle popolazioni nelle differenti stazioni, sono stati esaminati in media 20 individui per provenienza, posti ad almeno 50 - 80 m di distanza tra loro per evitare di campionare polloni radicali ([20], [18], [10]). Le caratteristiche bio-ecologiche del ciliegio selvatico, specie a distribuzione sparsa, limitano la possibilità di campionare un ampio numero di piante adulte per ciascuna popolazione, contrariamente a quanto avviene per piante a comportamento sociale.
L’analisi isoenzimatica
Per l’analisi interna alla popolazione di Monte Baldo ed alla sua filiera vivaistica sono stati analizzati i seguenti sistemi isoenzimatici, secondo i protocolli di Kaurish et al. ([28]), Santi ([40]), Santi & Lemoine ([41]): deidrogenasi isocitrica (IDH, E.C. 1.1.1.42), deidrogenasi malica (MDH, 1.1.1.37), glutamato-oxalacetato transaminasi (GOT, E.C. 2.6.1.1), fosfo-glucosio isomerasi (PGI, E.C., 5.3.1.9), deidrogenasi 6-fosfogluconica (6-PGD, E.C. 1.1.1.44), deidrogenasi glutammica (GDH, E.C. 1.4.1.3), fosfo-glucosio mutasi (PGM, E.C. 2.7.5.1), aconitasi (ACO, E.C. 4.2.1.3) e deidrogenasi scichimica (SKDH, E.C. 1.1.1.25), per un totale di 15 loci genici, di cui 10 polimorfici, per 21 varianti alleliche. Per il confronto tra la popolazione di Monte Baldo e quelle di riferimento sono stati considerati i primi 5 sistemi isoenzimatici, per un totale di 6 loci polimorfici e 12 varianti alleliche.
La stima dei livelli di variabilità genetica è stata effettuata considerando i seguenti parametri, elaborati statisticamente con il software BIOSYS-1 ([45]): frequenze alleliche, numero medio di alleli per locus (n), percentuale di loci polimorfici (P5%; un locus è considerato polimorfo quando la frequenza dell’allele più comune è inferiore al 95%), eterozigosi osservata (Ho) ed attesa (He), distanza genetica tra popolazioni ([33]). Sulle frequenze alleliche è stato condotto il test c 2 di eterogeneità ([22]) per verificare se le differenze tra popolazioni sono significative, mentre sulle frequenze genotipiche è stato effettuato il test del c 2 per controllare la rispondenza alla legge dell’equilibrio di Hardy-Weinberg ([33]). Il dendrogramma UPGMA (Unweighted Pair-Group Method with Arithmetic averaging - [44]), basato sulle distanze genetiche di Nei ([33]), è stato realizzato al fine di suddividere le popolazioni in cluster e verificare l’eventuale rispondenza ad una strutturazione geografica dell’informazione genetica ottenuta ([17]).
Sono stati infine calcolati gli indici HT (diversità genetica totale), HS (componente della diversità genetica dovuta a differenze interne alle singole popolazioni), DST (componente della diversità genetica dovuta a differenze tra le diverse popolazioni) e GST (differenziazione genetica: GST =DST /HT) per conoscere la differenziazione tra le popolazioni ([34], [27]); sono stati calcolati anche gli F statistici ([48]), che descrivono la struttura genetica delle popolazioni: FIT (variabilità genetica nella popolazione totale), FST (componente della variabilità genetica tra popolazioni) e FIS (componente della variabilità genetica entro ciascuna popolazione). Entrambi questi due gruppi di indici stimano la differenziazione genetica tra popolazioni: sono, infatti, indici di fissazione che valutano l’eventuale eccesso o difetto di omozigoti rispetto a determinati valori di riferimento. L’F di Wright ([49]), o coefficiente di inbreeding F = 1-(Ho/He), è stato impiegato per misurare la deviazione della composizione genotipica dall’equilibrio di Hardy - Weinberg (-1 ≤ F ≤ 1; valori negativi indicano eccesso di eterozigoti, mentre valori positivi indicano eccesso di omozigoti; l’equilibrio si ha per valori assoluti di F tendenti a 0).
Per identificare le variabili genetiche (frequenze alleliche) a carico delle quali si esprime la maggiore variabilità, per tutti gli individui del Monte Baldo (piante madri e discendenze) e per tutti i sistemi enzimatici studiati, è stata condotta con il software NTSYS-pc versione 2.1 ([39]) l’analisi delle componenti principali della matrice di dispersione ([16]) ed è stato realizzato il dendrogramma UPGMA per i singoli individui della popolazione Monte Baldo A e Monte Baldo B.
È stato applicato il metodo del bootstrapping ([38]) per ridurre l’effetto di dati mancanti e/o di eventuali difetti di campionamento ([48], [3]), utilizzando il programma FSTAT, versione 2.9.3.2 ([22]).
Risultati
La popolazione del Monte Baldo e la filiera vivaistica
In Tab. 1 sono riportate le frequenze alleliche, mentre nella 2 sono riassunti i principali parametri genetici dei 3 livelli della filiera vivaistica. La distribuzione dei 21 alleli nei 10 loci polimorfici è simile nella popolazione madre Monte Baldo e nelle discendenze. Fa eccezione l’allele GOT-2a nella popolazione della Piantagione che, avendo una frequenza minore del 5%, si presenta come allele raro. Anche P5% è simile nei 5 gruppi. Il coefficiente di inbreeding è sempre positivo, perciò tutti i gruppi si discostano dall’equilibrio Hardy-Weinberg per eccesso di omozigoti. Il deficit di eterozigosi è massimo nella popolazione di Monte Baldo B (popolazione di quota più elevata) e minimo tra le piantine della classe di età S1 T1.
Tab. 1 - Frequenze alleliche nei 10 sistemi isoenzimatici analizzati nella filiera vivaistica del Monte Baldo.
| Locus | Numerosità campionaria/ Allele |
Popolazione | ||||
|---|---|---|---|---|---|---|
| Monte Baldo A |
Monte Baldo B |
S1 T1 | S1 T1 | Piantagione | ||
| IDH-1 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .667 | .594 | .512 | .500 | .492 | |
| B | .333 | .406 | .488 | .500 | .508 | |
| IDH-2 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .300 | .281 | .287 | .175 | .192 | |
| B | .700 | .719 | .712 | .825 | .808 | |
| PGI-1 | (N) | 15 | 16 | 40 | 40 | 60 |
| Monomorfico | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| PGI-2 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .300 | .125 | .213 | .225 | .342 | |
| B | .700 | .875 | .788 | .775 | .658 | |
| GOT-1 | (N) | 15 | 16 | 40 | 40 | 60 |
| Monomorfico | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| GOT-2 | (N) | 15 | 16 | 40 | 39 | 60 |
| A | .267 | .250 | .287 | .269 | .042 | |
| B | .733 | .750 | .712 | .731 | .958 | |
| GDH-1 | (N) | 13 | 16 | 40 | 39 | 60 |
| A | .577 | .375 | .575 | .179 | .550 | |
| B | .423 | .625 | .425 | .821 | .450 | |
| PGM-1 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .333 | .406 | .313 | .363 | .408 | |
| B | .667 | .594 | .688 | .637 | .592 | |
| SDH-1 | (N) | 15 | 14 | 40 | 40 | 59 |
| A | .700 | .786 | .363 | .488 | .500 | |
| B | .300 | .214 | .637 | .512 | .500 | |
| 6PGD1 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .867 | .875 | .863 | .813 | .808 | |
| B | .133 | .125 | .138 | .188 | .192 | |
| 6PGD2 | (N) | 15 | 16 | 40 | 40 | 60 |
| Monomorfico | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| MDH-1 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .967 | .938 | .962 | .925 | .933 | |
| B | .033 | .063 | .038 | .075 | .067 | |
| MDH-2 | (N) | 15 | 16 | 40 | 40 | 60 |
| Monomorfico | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| ACO-1 | (N) | 15 | 16 | 40 | 40 | 60 |
| Monomorfico | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| ACO-2 | (N) | 15 | 16 | 40 | 40 | 60 |
| A | .267 | .219 | .300 | .200 | .175 | |
| B | .467 | .500 | .213 | .488 | .442 | |
| C | .267 | .281 | .488 | .313 | .383 | |
Se si esclude il locus PGI-2, la carenza di eterozigoti (Tab. 3) è significativa soprattutto nelle 3 popolazioni costituite dalle progenie. Gli F statistici (Tab. 4), indicano che il 96% della variabilità totale è comune ai 5 gruppi (FST = 0.040; FIT = 0.238) e che la variabilità esistente è dovuta per il 79.4 % ai singoli individui (FIS = 0.206).
Tab. 3 - Indice di fissazione medio FIS calcolato per i tre livelli della filiera vivaistica esaminati (*P<0.05; **P<0.01).
| Popolazione | locus | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| MDH-1 | 6PGD-1 | IDH-1 | IDH-2 | PGI-2 | GOT-3 | GDH-1 | PGM-2 | SKDH-1 | ACO-2 | |
| 1. Monte Baldo A | -0.034 | -0.154 | -0.111 | 0.4 | 0.524* | -0.023 | -0.103 | 0.4 | 0.206 | 0.062 |
| 2. Monte Baldo B | -0.067 | -0.143 | 0.227 | 0.611** | 0.429* | 0.333 | 0.2 | 0.352 | 0.152 | 0.298 |
| 3. S1 T1 | -0.039 | 0.051 | -0.037 | 0.049 | 0.328* | -0.037 | 0.182 | 0.244 | 0.08 | 0.442** |
| 4. S1 T2 | -0.081 | 0.097 | -0.212 | 0.3* | 0.427** | 0.283 | 0.129 | 0.405** | 0.049 | 0.4** |
| 5. Piantagione | -0.071 | -0.13 | 0.193 | 0.3** | 0.518** | -0.043 | 0.192 | 0.138 | 0.085 | 0.469** |
Tab. 4 - F-statistico medio nei 3 livelli della filiera vivaistica di Monte Baldo, calcolati su 10 loci.
| Locus | FIS | FIT | FST |
|---|---|---|---|
| IDH-2 | 0.329 | 0.341 | 0.018 |
| PGI-2 | 0.454 | 0.471 | 0.031 |
| GOT-3 | 0.127 | 0.169 | 0.048 |
| GDH-1 | 0.119 | 0.204 | 0.097 |
| PGM-2 | 0.307 | 0.311 | 0.006 |
| SDH-1 | 0.109 | 0.195 | 0.096 |
| 6PGD1 | -0.05 | -0.043 | 0.006 |
| MDH-1 | -0.064 | -0.058 | 0.005 |
| IDH-2 | 0.016 | 0.03 | 0.015 |
| ACO-2 | 0.333 | 0.354 | 0.031 |
| Media | 0.206 | 0.238 | 0.040 |
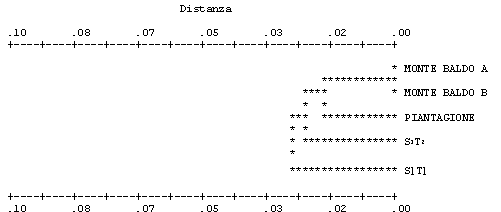
Il dendrogramma UPGMA (Fig. 2), realizzato usando le distanze genetiche di Nei ([33]), unisce nello stesso cluster le due popolazioni madri del Monte Baldo e quella della Piantagione, mentre le piantine rispettivamente delle classi S1 T2 e S1 T1 costituiscono cluster a sé.
Fig. 2 - Dendrogramma UPGMA per la filiera vivaistica stimato secondo Nei ([33]).
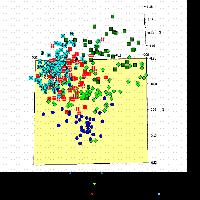
Secondo l’analisi delle componenti principali sono necessarie le prime 6 componenti per spiegare il 54.8% della varianza totale e gli alleli che in maggior misura contribuiscono a discriminare i diversi gruppi sono: 6PGD-1a, ACO-2a, GDH-1b, 6PGD-1b, ACO-2c e ACO-2b.
La popolazione Monte Baldo ed il sistema di riferimento
Per i loci isoenzimatici comuni sia alla popolazione di riferimento che alla filiera vivaistica, le frequenze e la distribuzione degli alleli ed i principali parametri genetici di Monte Baldo (considerata come popolazione unica) e delle sue discendenze, hanno valori compatibili con quelli delle popolazioni italiane campionate (Tab. 5, Tab. 6). Dal punto di vista del polimorfismo genetico la popolazione di base di Monte Baldo, i trapianti S1 T1 e la Piantagione hanno valori simili a Bosco Fontana (popolazione isolata e ridotta, ma costituita da piante tutte molto vecchie e distanziate) ed ai Monti della Laga (molto più ampia e sparsa).
Tab. 5 - Frequenze alleliche nelle popolazioni italiane di confronto e nella filiera vivaistica per i sistemi isoenzimatici comuni. 1) Colline Torinesi (TO); 2) Bosco Fontana (MN); 3) Area Garda (BS); 4) Valtellina (SO); 5) Asiago- Lessinia (VI-VR); 6) Prealpi venete Est (BL-TV); 7) Appennino Tosco-Romagnolo (FO-AR); 8) Monti della Laga (TE); 9) Valtiberina (AR-PU); 10) Monti Sibillini (MC-AP); 11) Monte Baldo (VR); 12) Piantagione; 13) S1 T1; 14) S1 T2. Monom. = monomorfico.
| Locus | N / Alleli | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MDH-1 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| A | 0.864 | 0.964 | 0.794 | 0.833 | 0.932 | 0.94 | 0.921 | 0.94 | 0.8 | 0.918 | 0.952 | 0.933 | 0.962 | 0.925 | |
| B | 0.136 | 0.036 | 0.206 | 0.167 | 0.068 | 0.06 | 0.079 | 0.06 | 0.2 | 0.082 | 0.048 | 0.067 | 0.038 | 0.075 | |
| MDH-2 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| Monom. | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| 6PGD1 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| A | 0.818 | 0.893 | 0.882 | 0.944 | 0.705 | 0.86 | 0.947 | 0.82 | 0.867 | 0.394 | 0.871 | 0.808 | 0.863 | 0.813 | |
| B | 0.182 | 0.107 | 0.118 | 0.056 | 0.295 | 0.14 | 0.053 | 0.18 | 0.133 | 0.606 | 0.129 | 0.192 | 0.138 | 0.188 | |
| 6PGD2 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| Monom. | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| IDH-1 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| A | 0.5 | 0.214 | 0.206 | 0.361 | 0.455 | 0.28 | 0.408 | 0.32 | 0.333 | 0.376 | 0.29 | 0.192 | 0.287 | 0.175 | |
| B | 0.5 | 0.786 | 0.794 | 0.639 | 0.545 | 0.72 | 0.592 | 0.68 | 0.667 | 0.624 | 0.71 | 0.808 | 0.712 | 0.825 | |
| IDH-2 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 35 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| A | 0.545 | 0.607 | 0.618 | 0.556 | 0.386 | 0.46 | 0.457 | 0.82 | 0.633 | 0.541 | 0.629 | 0.492 | 0.512 | 0.5 | |
| B | 0.455 | 0.393 | 0.382 | 0.444 | 0.614 | 0.54 | 0.543 | 0.18 | 0.367 | 0.459 | 0.371 | 0.508 | 0.488 | 0.5 | |
| PGI-1 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| Monom. | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| PGI-2 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| A | 0.636 | 0.607 | 0.441 | 0.361 | 0.614 | 0.4 | 0.618 | 0.04 | 0.4 | 0.059 | 0.21 | 0.342 | 0.213 | 0.225 | |
| B | 0.364 | 0.393 | 0.559 | 0.639 | 0.386 | 0.6 | 0.382 | 0.96 | 0.6 | 0.941 | 0.79 | 0.658 | 0.788 | 0.775 | |
| GOT-1 | (N) | 11 | 14 | 17 | 18 | 22 | 25 | 38 | 25 | 15 | 85 | 31 | 60 | 40 | 40 |
| Monom. | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | |
| GOT-2 | (N) | 11 | 14 | 17 | 18 | 21 | 25 | 38 | 25 | 15 | 83 | 31 | 60 | 40 | 39 |
| A | 0.5 | 0.25 | 0.294 | 0.25 | 0.524 | 0.42 | 0.25 | 0.24 | 0.2 | 0.253 | 0.258 | 0.042 | 0.287 | 0.269 | |
| B | 0.5 | 0.75 | 0.706 | 0.75 | 0.476 | 0.58 | 0.75 | 0.76 | 0.8 | 0.747 | 0.742 | 0.958 | 0.712 | 0.731 |
Tab. 6 - Variabilità genetica (stimata per i loci comuni) nelle popolazioni italiane di confronto e nella filiera vivaistica del Monte Baldo. N/L: Dimensione media del campione per locus; n: Numero medio di alleli per locus; P5%: Percentuale di loci polimorfici (un locus è considerato polimorfo se la frequenza dell’allele più comune è inferiore al 95%); Ho: Eterozigosi media osservata; He: Eterozigosi media attesa (stimata secondo [33]); F: Indice di fissazione medio per popolazione.
| Popolazione | N/L | n | P5% | Ho | He | F |
|---|---|---|---|---|---|---|
| 1. Colline Torinesi (TO) | 11 | 1.6 | 60 | 0.209 | 0.261 | 0.199 |
| (0.0) | (0.2) | - | (0.062) | (0.077) | - | |
| 2. Bosco Fontana (MN) | 14 | 1.6 | 50 | 0.121 | 0.2 | 0.395 |
| (0.0) | (0.2) | - | (0.043) | (0.067) | - | |
| 3. Area Garda (BS) | 17 | 1.6 | 60 | 0.141 | 0.231 | 0.39 |
| (0.0) | (0.2) | - | (0.044) | (0.068) | - | |
| 4. Valtellina (SO) | 18 | 1.6 | 60 | 0.194 | 0.224 | 0.134 |
| (0.0) | (0.2) | - | (0.064) | (0.071) | - | |
| 5. Asiago-Lessinia (VI, VR) | 21.9 | 1.6 | 60 | 0.239 | 0.254 | 0.059 |
| (0.1) | (0.2) | - | (0.082) | (0.077) | - | |
| 6. Prealpi venete Est (BL, TV) | 25 | 1.6 | 60 | 0.176 | 0.227 | 0.225 |
| (0.0) | (0.2) | - | (0.057) | (0.073) | - | |
| 7. App. Tosco-Romagnolo (FO, AR) | 37.7 | 1.6 | 60 | 0.186 | 0.21 | 0.114 |
| (0.3) | (0.2) | - | (0.076) | (0.071) | - | |
| 8. Valtiberina (AR, PU) | 15 | 1.6 | 60 | 0.207 | 0.234 | 0.115 |
| (0.0) | (0.2) | - | (0.071) | (0.068) | - | |
| 9. Monti Sibillini (MC, AP) | 84.8 | 1.6 | 60 | 0.134 | 0.21 | 0.362 |
| (0.2) | (0.2) | - | (0.046) | (0.07) | - | |
| 10. Monti della Laga (TE) | 25 | 1.6 | 50 | 0.148 | 0.161 | 0.081 |
| (0.0) | (0.2) | - | (0.052) | (0.055) | - | |
| 11. Monte Baldo (VR) | 31 | 1.6 | 50 | 0.145 | 0.194 | 0.253 |
| (0.0) | (0.2) | - | (0.047) | (0.062) | - | |
| 12. S1 T1 | 40 | 1.6 | 50 | 0.185 | 0.199 | 0.07 |
| (0.0) | (0.2) | - | (0.062) | (0.065) | - | |
| 13. S1 T2 | 39.9 | 1.6 | 60 | 0.161 | 0.2 | 0.195 |
| (0.1) | (0.2) | - | (0.048) | (0.062) | - | |
| 14. Piantagione | 60 | 1.6 | 50 | 0.138 | 0.179 | 0.229 |
| (0.0) | (0.2) | - | (0.046) | (0.063) | - |
Nelle popolazioni di riferimento la deviazione dall’equilibrio di Hardy-Weinberg è significativa, per eccesso di omozigoti, tranne che per Asiago-Lessinia (0.059), la Valtiberina (0.115) ed i Monti della Laga (0.081), che non differiscono significativamente dall’equilibrio panmittico. Tra le provenienze con più alto valore di F ci sono quelle di Bosco Fontana, dell’Area del Garda (che include materiali della Valvestino (BS), della Val Sabbia e delle Valli Giudicarie (TN), situate sulla sponda occidentale del Lago di Garda) e dei M. Sibillini (MC, AP).
In Tab. 7 sono riportati i valori medi di differenziazione genetica calcolati per tutti i loci comuni alle popolazioni di riferimento ed ai 3 livelli della filiera vivaistica. Anche in questo caso solo una piccola parte della variabilità genetica totale (GST = 0.064) è dovuta a differenze tra popolazioni, mentre più del 90% è riconducibile a differenze interne ai popolamenti. Il locus con minor variabilità totale è MDH-1 (HT = 0.161), mentre PGI-2 (GST = 0.126) e 6PGD-1 (0.112) sono i più efficaci nel differenziare le popolazioni.
Tab. 7 - Valori di differenziazione genetica in tutte le popolazioni analizzate (filiera vivaistica compresa), calcolati per i loci genici polimorfici comuni.
| Locus | HT | HS | DST | GST |
|---|---|---|---|---|
| MDH-1 | 0.161 | 0.165 | 0.004 | 0.024 |
| MDH-2 | 0.000 | 0.000 | 0.000 | 0.000 |
| 6PGD1 | 0.294 | 0.331 | 0.037 | 0.112 |
| 6PGD2 | 0.000 | 0.000 | 0.000 | 0.000 |
| IDH-1 | 0.423 | 0.437 | 0.014 | 0.031 |
| IDH-2 | 0.486 | 0.493 | 0.007 | 0.015 |
| PGI-1 | 0.000 | 0.000 | 0.000 | 0.000 |
| PGI-2 | 0.401 | 0.459 | 0.058 | 0.126 |
| GOT-1 | 0.000 | 0.000 | 0.000 | 0.000 |
| GOT-2 | 0.377 | 0.403 | 0.026 | 0.065 |
| Media | 0.214 | 0.229 | 0.015 | 0.064 |
Nella Tab. 8 sono riportati i valori medi delle statistiche F di Wright, calcolati per tutti i loci comuni a tutte le popolazioni. FIS (0.182) e FIT (0.249) medi sono entrambi positivi, confermando sia l’eccesso di omozigoti nei singoli gruppi studiati, che il peso maggiore della diversità genetica tra individui sulla diversità totale osservata. Il locus PGI-2 contribuisce più di tutti a questo risultato, mentre MDH-1, IDH-1 e 6PGD-1 hanno valori negativi.
Tab. 8 - F-statistico medio per i loci comuni ai 3 livelli del Monte Baldo ed alle popolazioni italiane di confronto.
| Locus | FIS | FIT | FST |
|---|---|---|---|
| MDH-1 | -0.037 | 0.001 | 0.037 |
| 6PGD1 | -0.058 | 0.067 | 0.118 |
| IDH-1 | -0.018 | 0.025 | 0.042 |
| IDH-2 | 0.240 | 0.271 | 0.042 |
| PGI-2 | 0.658 | 0.714 | 0.164 |
| GOT-2 | 0.102 | 0.163 | 0.068 |
| Media | 0.182 | 0.249 | 0.081 |
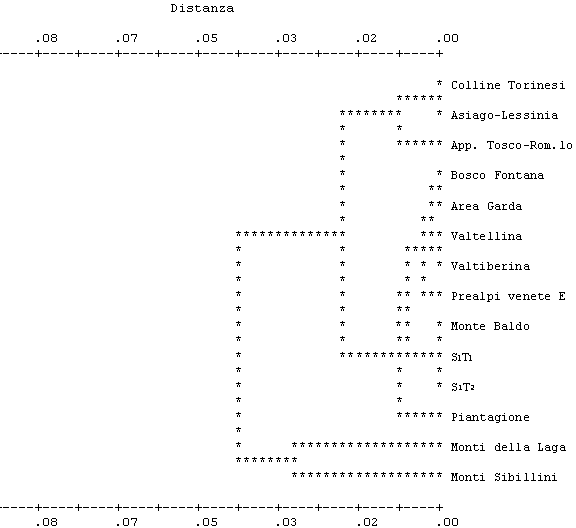
Il dendrogramma UPGMA (Fig. 3) costruito sulle distanze genetiche di Nei ([33]) non individua cluster geografici completamente omogenei per le 11 popolazioni considerate. I tre livelli della filiera vivaistica di Monte Baldo appartengono allo stesso cluster principale (confermando la provenienza del materiale), del quale fanno parte anche popolazioni limitrofe (tra cui Area Garda e Valtellina). Questo gruppo di popolazioni affini risponde bene ad una logica geografica e riunisce tutte quelle del distretto alpino centrale.
Fig. 3 - Dendrogramma UPGMA, stimato secondo Nei ([33]), per i quattro livelli del Monte Baldo e per le popolazioni italiane di confronto.
Discussione e Conclusioni
Il caso di studio presentato offre lo spunto a varie considerazione relative all’organizzazione della filiera vivaistica, sia di ordine generale, che specifiche per specie con caratteristiche biologiche simili al ciliegio selvatico.
La popolazione di partenza
La popolazione madre di Monte Baldo, come altre italiane di riferimento, ha livelli di eterozigosi relativamente elevati, analogamente a quanto riscontrato in media per il ciliegio in Italia ([9], [11]). Questa situazione è stata descritta anche in altre regioni dell’Europa occidentale. Infatti valori comparabili a quelli riscontrati nel nostro lavoro sono stati stimati per eterozigosi attesa (He), numero medio di alleli per locus e percentuale di loci polimorfici da Santi (comunicazione personale) su popolazioni francesi e georgiane di ciliegio selvatico. Queste stime sono superiori ai valori medi proposti da Hamrick ([25]) e Hamrick et al. ([26]) per le Angiosperme. Vanno tuttavia considerate le caratteristiche bio-ecologiche che distinguono le Rosacee, come ad esempio il ciliegio ed i sorbi, dalle altre specie. Infatti, i valori da noi stimati sono comparabili a quelli forniti da Raspé & Jacquemart ([37]) per Sorbus aucuparia. Anche per Sorbus torminalis i valori degli stessi parametri sono superiori a quelli medi indicati da Hamrick e colleghi ([6]). Secondo questi Autori, nelle specie arboree ad ampio areale, questa caratteristica sarebbe da attribuire al sistema riproduttivo di eso-incrocio (il ciliegio presenta auto-incompatibilità obbligata e impollinazione entomogama) ed alla dispersione zoocora, che permettono di conservare in maggior misura la diversità intraspecifica rispetto a specie con altre caratteristiche riproduttive.
A conferma di quanto sopra, la diversità tende ad aumentare nel ciliegio quando le popolazioni si rarefanno ed entrano a far parte di ecosistemi più maturi e complessi ([40], [41], [5], [18]). Le popolazioni francesi, ad esempio, pur occupando nicchie ecologiche simili alle nostre, presentano un numero maggiore di individui, sono più disetanee, sono in fasi della successione ecologica più avanzate e sono sottoposte a trattamenti selvicolturali adeguati, presentando così indicatori di diversità migliori ([10]). Al contrario le popolazioni italiane, compresa quella di Monte Baldo, spesso situate ai margini della foresta, nei pascoli o in ex coltivi dove, grazie alla capacità pollonifera, tendono a colonizzare velocemente gli spazi liberi, sono caratterizzate frequentemente da stadi evolutivi giovanili. Ciò è confermato dall’F positivo (deviazione dall’equilibrio panmittico verso l’omozigosi) e dai valori mediamente superiori di FST nelle popolazioni italiane rispetto a quelli segnalati dagli autori francesi. L’effetto “del fondatore”, la capacità pollonifera spiccata ed altri fattori indotti da cause naturali o antropiche (ceduazione), possono aver limitato l’evoluzione ed il dinamismo delle strutture genetiche oltre i limiti consentiti dalla biologia caratteristica della specie.
Le distanze genetiche (Tab. 9) hanno evidenziato che Monte Baldo A e B, pur trovandosi a quote e fasce fito-climatiche diverse, probabilmente derivano da un’unica popolazione. Considerato il livello elevato di omozigosi, soprattutto del gruppo B, e le strategie di propagazione vegetativa del ciliegio che, se presente, tendono a favorirla, sarebbe auspicabile allargare la raccolta anche ad altri individui, eventualmente presenti nell’area considerata e nei boschi limitrofi, per poter aumentare l’effettivo della popolazione di base.
Tab. 9 - Distanze genetiche nella filiera vivaistica calcolate su tutti i loci analizzati (sopra la diagonale sono state stimate secondo [33], mentre sotto la diagonale sono state stimate secondo [32]).
| Popolazione | 1 | 2 | 3 | 4 | 5 |
|---|---|---|---|---|---|
| 1. Monte Baldo A | ***** | 0 | 0.006 | 0.01 | 0.015 |
| 2. Monte Baldo B | 0.008 | ***** | 0.014 | 0.02 | 0.007 |
| 3. Piantagione | 0.014 | 0.021 | ***** | 0.011 | 0.015 |
| 4. S1 T1 | 0.019 | 0.028 | 0.014 | ***** | 0.018 |
| 5. S1 T2 | 0.024 | 0.015 | 0.019 | 0.023 | ***** |
Sul piano pratico, per assicurare la raccolta del seme da piante geneticamente diverse, potrebbe essere utile anche un ciclo di osservazione su due caratteri ad alta ereditabilità in senso lato: la fenologia fiorale e la sensibilità a Cilindrosporium sp. ([9]). In questo modo è possibile evidenziare se esiste corrispondenza tra distribuzione topografica dei genotipi enzimatici ed i caratteri considerati e, di conseguenza, individuare la presenza di gruppi di piante geneticamente omogenei.
Per quanto riguarda la differenza del valore di F tra Monte Baldo A e B, questa potrebbe essere legata alla disposizione topografica dei due gruppi di piante madri. Infatti, l’adattamento a quote superiori potrebbe aver favorito solo alcuni genotipi (che potrebbero essere i responsabili dell’“effetto del fondatore” nella popolazione) o, quanto meno, dell’antica popolazione solo alcuni di essi potrebbero essere arrivati in quota. L’isolamento, inoltre, limitando lo scambio con le altre popolazioni, potrebbe aver determinato la maggiore distanza genetica di Monte Baldo B sia con le altre popolazioni venete che con quelle dell’area del Garda ([13]).
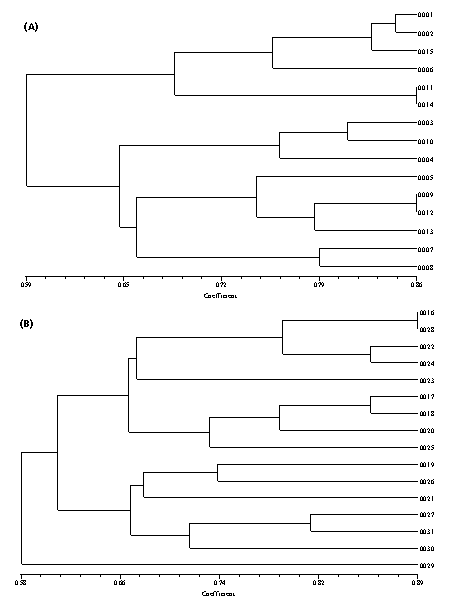
Comunque, nonostante il valore alto di F, Monte Baldo B (sotto-popolazione con più marcate caratteristiche di soprassuolo forestale di quota) ha una percentuale di loci polimorfici superiore rispetto a Monte Baldo A (più sottoposta all’azione antropica nel corso della sua storia) e un buon livello di eterozigosi attesa. Nella sotto-popolazione B, forse a causa delle condizioni micro-ambientali (altitudine superiore), sembra che sia stato sì favorito un elevato livello di omozigosi, ma che questo fenomeno sia stato in parte compensato dalla conservazione di un maggiore polimorfismo. Questo risultato sembra analogo a quanto descritto per popolazioni marginali di altre specie che vegetano in quota ([30], [12]). Anche il dendrogramma dei singoli genotipi della popolazione ha evidenziato maggiore diversificazione nel gruppo B (Fig. 4a-4b). Questi elementi indicherebbero che Monte Baldo B è stata probabilmente in passato una popolazione più estesa, della quale sono rimasti pochi individui. Anche in altre specie forestali, quando lo studio della variabilità genetica è stato effettuato tramite profili enzimatici, sono stati ottenuti valori opposti di F e P5% ([23]).
Fig. 4 - Dendrogrammi UPGMA ottenuti con il programma NTSYS 2.1 ([39]): (A) popolazione Monte Baldo A; (B) popolazione Monte Baldo B.
Rispetto alle popolazioni italiane di riferimento, le distanze genetiche (Tab. 10) evidenziano maggiore vicinanza tra la popolazione del Monte Baldo e le provenienze lombarde individuate sul lato opposto del Lago di Garda (Area Garda, Bosco Fontana e Valtellina), che con le altre popolazioni venete (Monti Lessini e Asiago).
Tab. 10 - Distanze genetiche fra le popolazioni studiate, calcolate per i loci isoenzimatici comuni (sopra la diagonale sono state stimate secondo [33], mentre sotto la diagonale sono state stimate secondo [32]).
| Popolazione | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1. Colline Torinesi (TO) | ***** | 0.008 | 0.012 | 0.011 | 0 | 0.006 | 0.003 | 0.058 | 0.012 | 0.071 | 0.029 | 0.042 | 0.027 | 0.034 |
| 2. Bosco Fontana (MN) | 0.021 | ***** | 0 | 0.005 | 0.019 | 0.005 | 0.002 | 0.041 | 0.001 | 0.07 | 0.014 | 0.011 | 0.016 | 0.015 |
| 3 Area Garda (BS) | 0.024 | 0.007 | ***** | 0 | 0.025 | 0.002 | 0.009 | 0.023 | 0 | 0.052 | 0.004 | 0.009 | 0.006 | 0.005 |
| 4. Valtellina (SO) | 0.023 | 0.013 | 0.005 | ***** | 0.024 | 0.001 | 0.005 | 0.019 | 0 | 0.048 | 0.001 | 0.008 | 0.001 | 0.005 |
| 5. Asiago-Lessinia (VI-VR) | 0.006 | 0.028 | 0.033 | 0.032 | ***** | 0.008 | 0.012 | 0.075 | 0.027 | 0.063 | 0.039 | 0.046 | 0.032 | 0.036 |
| 6. Prealpi venete Est (BL, TV) | 0.016 | 0.012 | 0.009 | 0.008 | 0.015 | ***** | 0.008 | 0.031 | 0.005 | 0.046 | 0.007 | 0.016 | 0.003 | 0.004 |
| 7. App. Tosco-Romagnolo (FO, BO) | 0.013 | 0.008 | 0.015 | 0.011 | 0.018 | 0.013 | ***** | 0.058 | 0.007 | 0.08 | 0.024 | 0.021 | 0.021 | 0.026 |
| 8. Monti della Laga (TE) | 0.068 | 0.047 | 0.03 | 0.024 | 0.081 | 0.036 | 0.061 | ***** | 0.016 | 0.03 | 0.004 | 0.028 | 0.012 | 0.016 |
| 9. Valtiberina (AR, PU) | 0.025 | 0.011 | 0.004 | 0.002 | 0.036 | 0.013 | 0.014 | 0.023 | ***** | 0.042 | 0.001 | 0.005 | 0.004 | 0.006 |
| 10. Monti Sibillini (MC,AP) | 0.08 | 0.076 | 0.057 | 0.052 | 0.068 | 0.049 | 0.082 | 0.032 | 0.048 | ***** | 0.031 | 0.04 | 0.03 | 0.029 |
| 11. Monte Baldo (VR) | 0.039 | 0.021 | 0.011 | 0.007 | 0.045 | 0.011 | 0.027 | 0.008 | 0.008 | 0.034 | ***** | 0.009 | 0 | 0.001 |
| 12. Piantagione | 0.051 | 0.017 | 0.014 | 0.013 | 0.051 | 0.02 | 0.023 | 0.031 | 0.011 | 0.042 | 0.012 | ***** | 0.009 | 0.006 |
| 13. S1 T1 | 0.036 | 0.022 | 0.012 | 0.007 | 0.037 | 0.007 | 0.024 | 0.016 | 0.011 | 0.032 | 0.002 | 0.011 | ***** | 0 |
| 14. S1 T2 | 0.043 | 0.021 | 0.011 | 0.01 | 0.041 | 0.009 | 0.029 | 0.019 | 0.012 | 0.031 | 0.004 | 0.008 | 0.002 | ***** |
Una possibile spiegazione di questo risultato potrebbe essere la particolare collocazione geografica della popolazione, situata sul versante occidentale del Monte Baldo. Ad un primo esame potrebbe sembrare che il bacino del lago di Garda abbia rappresentato una barriera geografica ai flussi di geni tra le popolazioni del lato veneto e quelle lombarde, come avrebbero suggerito precedenti studi ([11]). Probabilmente, Il microclima particolarmente mite sulle rive del lago (di tipo mediterraneo) potrebbe, invece, aver favorito gli scambi genici tra le due sponde, attraverso l’avifauna. Al contrario, le comunicazioni tra i due versanti del Baldo hanno sicuramente trovato un ostacolo nello spartiacque piuttosto elevato e ventoso, quindi poco ospitale per l’avifauna e ancor meno favorevole per i trasferimenti di polline da parte di api e bombi, insetti pronubi che favoriscono la fecondazione incrociata.
In relazione alla struttura genetica, le due sotto-popolazioni sembrerebbero più giovanili, come stadio evolutivo e caratteristiche generali, rispetto a quelle venete. Infatti, l’area di diffusione del ciliegio sui Monti Lessini e sull’altopiano di Asiago è molto estesa, situata all’interno del bosco, in condizioni prossime al climax ed in cui gli individui adulti, molto distanziati tra loro, sono originati probabilmente in gran parte da seme (come mostrano i ridotti valori di F nella regione). Nelle Prealpi venete orientali e sul Monte Baldo, come anche sulla sponda opposta del lago di Garda (Valvestino), il ciliegio sta invece lentamente colonizzando aree non più coltivate, per cui i nuclei individuati sono costituiti da poche piante, spesso poco distanti tra loro, o che comunque costituiscono gruppi relativamente densi ed isolati (caratterizzati da F positivo), la cui struttura potrebbe risentire fortemente dell’”effetto del fondatore”.
La filiera vivaistica
Abbiamo potuto esaminare solo parte della filiera vivaistica, non essendo disponibili al momento delle analisi né semi, né semenzali (S1) della stessa provenienza. Tuttavia, dall’analisi della parte di filiera che è stato possibile studiare, si possono trarre alcune indicazioni a nostro avviso importanti:
1. i valori di n (numero medio di alleli/locus) non variano in alcuna sotto-popolazione;
2. vari parametri genetici mostrano relazioni tra probabili luoghi di raccolta e materiali di moltiplicazione nella filiera:
2.1. le distanze genetiche (Tab. 9) mostrano legami tra la sotto-popolazione A, il gruppo S1 T1 e la Piantagione di Grezzana e tra la sotto-popolazione B ed il gruppo S1 T2. Perciò i due gruppi di trapianti probabilmente derivano dall’una o dall’altra sotto-popolazione e non da entrambe;
2.2. anche la percentuale di loci polimorfici (P5 %), l’eterozigosi osservata (Ho) e i coefficienti di inbreeding (F) variano in funzione dell’area di raccolta probabilmente impiegata per approvvigionarsi di seme (Tab. 2);
Tab. 2 - Variabilità genetica nei 3 livelli della filiera vivaistica del Monte Baldo. N/L: Dimensione media del campione per locus; n: Numero medio di alleli per locus; P5%: Percentuale di loci polimorfici (un locus è stato considerato polimorfo quando la frequenza dell’allele più comune era inferiore al 95%); Ho: Eterozigosi media osservata; He: Eterozigosi media attesa (stimata secondo [33]); F: Indice di fissazione medio per popolazione.
| Popolazione | N/l | n | P5% | Ho | He | FIS |
|---|---|---|---|---|---|---|
| 1. Monte Baldo A (VR) | 14.9 | 1.7 | 60 | 0.227 | 0.274 | 0.172 |
| (0.1) | (0.2) | - | (0.054) | (0.061) | - | |
| 2. Monte Baldo B (VR) | 15.9 | 1.7 | 66.7 | 0.177 | 0.257 | 0.311 |
| (0.1) | (0.2) | - | (0.04) | (0.058) | - | |
| 4. S1 T1 | 40 | 1.7 | 60 | 0.223 | 0.268 | 0.168 |
| (0) | (0.2) | - | (0.049) | (0.06) | - | |
| 5. S1 T2 | 39.9 | 1.7 | 66.7 | 0.199 | 0.26 | 0.235 |
| (0.1) | (0.2) | - | (0.042) | (0.057) | - | |
| 3. Piantagione | 59.9 | 1.7 | 60 | 0.199 | 0.261 | 0.238 |
| (0.1) | (0.2) | - | (0.046) | (0.062) | - |
3. la Piantagione è caratterizzata da un valore di F elevato, superiore agli altri sotto-gruppi a cui sembra correlato geneticamente. Questo potrebbe essere spiegato dalla selezione fenotipica che normalmente viene effettuata, nella pratica vivaistica, quando i trapianti sono posti in vendita, o dalla pressione selettiva determinata da fattori microambientali nelle varie fasi produttive che si susseguono dalla semina;
4. i differenti lotti di piantine in vivaio (S1 T1 e S1 T2) e quelle della piantagione sono geneticamente più prossimi all’una o all’altra delle due sotto-popolazioni di origine, probabilmente perché il seme da cui derivano è stato raccolto in funzione della fruttificazione verificatasi in quantità più o meno abbondante nelle due località in annate diverse.
L’esame del cluster genotipico ([39]), realizzato impiegando tutta la popolazione della filiera vivaistica “Monte Baldo”, che non viene mostrato per motivi di spazio, non ha evidenziato eventuali relazioni tra piante delle sotto-popolazioni di origine usate per la raccolta del seme ed eventuali possibili discendenze. Questo lo interpretiamo come indizio di un certo scambio di materiale genetico all’interno della popolazione di Monte Baldo, da porre in relazione alla biologia della specie, che obbliga alla fecondazione incrociata. L’impollinazione entomofila, che copre in genere distanze di alcune centinaia di metri ([21]), fa in parte superare i limiti legati al numero ridotto di piante madri, al loro isolamento in quota ed alle condizioni ecologiche in cui si sviluppano, favorendo così una certa dinamica nella popolazione. Tutto ciò contribuisce in generale a ridurre i livelli di inbreeding nelle piantine prodotte in vivaio. Nonostante rimanga elevato rispetto a S1 T1, l’F stimato per S1 T2 è comunque inferiore a quello della probabile popolazione di origine (Monte Baldo B).
Poiché i trapianti di un anno sembrano costituire una popolazione relativamente più vicina all’equilibrio rispetto agli stadi successivi, è da arguire che qualche fattore determini pressione selettiva sui lotti di piantine. Sarebbe perciò auspicabile operare cercando di ridurre i vari fattori che possono entrare in gioco nel determinarla. Il più evidente di questi sembrerebbe la selezione fenotipica effettuata in vivaio al momento della distribuzione; essa è in alcuni casi inevitabile, come per i materiali destinati ad arboricoltura da legno, ma per altri scopi è possibile limitarne l’effetto, distribuendo piantine di qualità morfometrica variata. Infine, per favorire la germinazione del maggior numero di genotipi presenti nel lotto di seme, potrebbe risultare utile disporre di più aiuole per la semina poste in zone diverse del vivaio, o in vivai ad altitudini diverse. Il postime ottenuto verrà poi mescolato al momento della messa a dimora.
Organizzare i materiali di base da destinare alla filiera vivaistica del ciliegio
P. avium sembra caratterizzata da bassa differenziazione tra le popolazioni e da maggior variabilità individuale, come mostrano anche i risultati di precedenti lavori ([11]; [10]), confermati anche a livello fenotipico e fenologico ([8], [15]). I valori medi di GST (0.051) riscontrati da Hamrick et al. ([26]) per le Angiosperme sono in genere inferiori a quelli riscontrati per il ciliegio italiano, francese e caucasico (Santi et al., com. pers.), come anche in altre Rosaceae a distribuzione sparsa ([37], [6]).
Oltre a questa caratteristica, l’intensa antropizzazione del territorio italiano potrebbe aver favorito, insieme ad alterazioni della struttura genetica determinate dalle attività colturali ([10]), anche l’introgressione di materiale genetico di varietà da frutto nelle popolazioni di ciliegio selvatico. Il ciliegio dolce è, infatti, coltivato e diffuso da secoli in prossimità delle formazioni forestali e può aver contribuito ad alterare, almeno parzialmente, la struttura genetica di P. avium. Essa è probabilmente influenzata anche dall’isolamento dovuto a barriere geografiche naturali o all’interruzione per lunghi tratti della copertura forestale.
Queste considerazioni generali interessano i criteri di gestione delle risorse genetiche destinate alla filiera vivaistica al punto che in Francia, probabilmente a causa della sua scarsa differenziazione, il sistema di classificazione dei materiali forestali di base indica per P. avium una sola grande regione di provenienza ([2]). Questo non sembra possibile in Italia, dove è necessario tener conto della probabile maggior diversità adattativa delle popolazioni, in relazione alla grande quantità di ambienti e del maggior grado di differenziazione genetica tra provenienze ([8], [11]).
Trattandosi di una specie di elevato valore economico, la diversità genetica (componente individuale) può essere usata con profitto per produrre materiale di qualità. Per questo motivo sia in Francia ([42]) che nel nostro paese ([15]) si è data notevole importanza alla selezione clonale. Il metodo consente, infatti, di catturare e valorizzare quasi per intero e per caratteri vantaggiosi quella parte di variabilità (verificata anche per caratteri fenotipici) contenuta nei singoli individui della specie. È perciò possibile, attraverso valutazioni sperimentali, selezionare non solo singoli cloni ([14]), ma anche impiegarne un certo numero per realizzare arboreti da seme ([43]).
Prendendo come esempio la popolazione del Monte Baldo, sembrerebbe che essa sia parte di un gruppo di popolazioni geneticamente affini, probabilmente originato da materiali della Val Padana, che hanno risalito le vallate prealpine formando una popolazione più ampia, che include Bosco Fontana (MN), la Valvestino, le Valli Giudicarie (BS e TN) e la Valtellina (SO). A livello adattativo questi materiali sembrerebbero differenziati principalmente in funzione dell’altitudine di origine, come mostrano i risultati di test fenologici ([14]). Anche altri caratteri, non adattativi ma morfologici, legati alla forma delle foglie, hanno consentito di distinguere abbastanza chiaramente questa grande area di provenienza ([8]).
Le raccolte di seme potrebbero quindi prendere in considerazione, per il futuro, l’intera area con il vantaggio di avere a disposizione una base genetica più ampia.
I risultati suggerirebbero di organizzare l’approvvigionamento di seme in Monte Baldo principalmente dalla popolazione di minor quota, inserendo una certa percentuale di piante madri (5-10) del gruppo B, al fine di consentire il più ampio campionamento possibile di variabilità. Per garantire questo aspetto, nonostante le difficoltà che si possono incontrare in bosco e la ciclicità della produzione (influenzata anche dalla diversa altitudine delle due sottopopolazioni), si dovrebbe raccogliere seme dal maggior numero di piante possibile, magari in quantità ridotta.
Resta ancora aperto in Italia il capitolo della realizzazione di arboreti da seme che, nel caso di specie a distribuzione sparsa come il ciliegio, potrebbero contribuire a produrre materiali di moltiplicazione (semi e piantine) caratterizzati da più elevati livelli di diversità. Queste piantagioni, formate da un numero adeguato di cloni o famiglie, garantiscono raccolti frequenti, abbondanti, facili e a minor costo, consentendo di integrare la buona qualità del materiale selezionato con idonei livelli di variabilità.
Note al lavoro
Questa ricerca si inserisce tra le attività del Programma Finalizzato MiPAF “Riselvitalia”, sottoprogetto 1.1 - “Biodiversità e produzione di materiale forestale di propagazione”. Essa si integra con analoghe ricerche, condotte nell’ambito dello stesso sottoprogetto, su P. silvestris ([29]), con l’obiettivo di fornire modelli di riferimento alla filiera vivaistica per specie caratterizzate da biologia diversa.
References
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar