Using the Resistograph®to distinguish different types of wood rot on living silver fir in Molise (Italy)
Forest@ - Journal of Silviculture and Forest Ecology, Volume 7, Pages 190-198 (2010)
doi: https://doi.org/10.3832/efor0638-007
Published: Oct 13, 2010 - Copyright © 2010 SISEF
Research Articles
Guest Editors: 7° SISEF Congress (Pesche, IS - 2007)
« Development, adaptation, naturality and conservation »
Collection/Special Issue: Marco Marchetti, Roberto Tognetti
Abstract
he study was performed in two silver-fir forests (Abies alba Mill.) located in Alto Molise, Province of Isernia: Collemeluccio, near Pescolanciano and Abeti Soprani near Capracotta. The aim of this work was to distinguish different types of wood rot on living silver fir individuals by using the Resistograph® (IML-RESI E400), a device that allows to estimate the variation of wood density by measuring the resistance to micro-perforation. The occurrence of different types of wood rot (white rot and brown rot) in living trees was pointed out and discriminated by the device. In the detected deteriorated zones, fungal pathogens and decomposers were isolated and identified, causing either white (Phellinus hartigii, Ganoderma adspersum, Heterobasidion abietinum and Armillaria ostoyae) or brown rot (Fomitopsis pinicola).
Keywords
Abies alba Mill., wood density, rot, Resistograph®, drilling resistance, Ganoderma adspersum
Introduzione
Il legno è soggetto alla degradazione operata da diversi agenti fra cui i principali sono i funghi ([1]). L’attività di questi organismi può minare la stabilità delle piante indebolendone la struttura meccanica, può compromettere i processi fisiologici della pianta nel caso in cui l’alterazione si estenda all’alburno e alla corteccia e porta ad una riduzione della qualità delle caratteristiche tecnologiche del legno ([26]), che può indurre anche danni economici molto elevati ([13], [16], [19]).
In generale, sia su piante in piedi, sia su piante a terra sono riconosciuti tre tipi di carie del legno: la carie bianca, la carie bruna e quella soffice, differenziate in base ai diversi componenti chimici della parete cellulare interessati dalla degradazione ([21]).
Nella carie bianca (o distruttiva), causata principalmente da Basidiomiceti ([4]), si ha una rimozione più o meno selettiva della lignina e solo successivamente della cellulosa. Il risultato è che i tessuti danneggiati assumono una colorazione chiara. Alcune delle specie fungine che causano questo tipo di alterazione afferiscono ai generi: Armillaria, Ganoderma, Heterobasidion e Phellinus.
Nella carie bruna (o cubica), altre specie di Basidiomiceti ([4]) sono in grado di decomporre la cellulosa e le emicellulose, lasciando quasi intatta la lignina. Il legno colpito assume una colorazione bruna, perde resistenza alla compressione e alla flessione, e aumenta la permeabilità. Tra i generi fungini agenti di carie cubica è possibile annoverare Fomitopsis e Phaeolus.
Nel caso di carie soffice, invece, si tratta di una degradazione causata da numerosi Ascomiceti che si manifesta con l’imbrunimento di strati esterni del legno che diventano molli ed elastici.
Un ulteriore aspetto da considerare nello studio delle carie e degli organismi che le causano è la loro posizione preferenziale all’interno dell’albero, anche in base alle caratteristiche della specie ospite, tanto da assumere un diverso significato in relazione alla stabilità o alla sopravvivenza stessa dell’esemplare ([2]).
Il Resistograph® è uno strumento che permette una stima del profilo di densità del legno attraverso la misurazione della resistenza alla micro-perforazione ([25]). Questo strumento può essere utilizzato in ambiti molto diversi tra loro. Su legname in opera è possibile la stima della resistenza meccanica delle travi in legno durante interventi di restauro conservativo ([3]) e la verifica nel tempo dello stato di conservazione delle opere in legno nelle sistemazioni idraulico-forestali ([8]). Può consentire di distinguere i diversi stadi di decadimento del legno morto ([15]) e di relazionare le diverse densità ai contenuti di carbonio ed azoto presenti ([7]). Infine, su piante vive, consente di determinarne la densità del legno ([14]), di valutare le caratteristiche delle cerchie annuali del legno ([25] su Taiwania cryptomerioides), tanto da permettere, talvolta, di determinare l’età delle piante ([18] su tiglio), di stimare l’estensione delle carie ed altre anomalie del fusto in soggetti in ambiente urbano ([20]), di evidenziare precocemente la presenza di alterazioni interne anche quando non sono evidenti sintomi esterni ([6]).
Nel presente studio si è indagato sulla possibilità di utilizzare il Resistograph® per individuare le alterazioni in piante vive di abete bianco (Abies alba Mill.) e le loro caratteristiche, argomento innovativo non trattato in alcun precedente lavoro.
Materiali e metodi
L’indagine è stata condotta in due abetine naturali nell’Alto Molise: Collemeluccio (Pietrabbondante - IS; quota 790 - 1065 m s.l.m.; temperatura media annua 11.9°C; precipitazione media annua 1018.55 mm) ed Abeti Soprani (Pescopennataro e Capracotta - IS; quota 1200 - 1600 m s.l.m.; temperatura media annua 8.2°C; precipitazione media annua 1070.02 mm). L’abete bianco presenta un legno biancastro opaco, con anelli di accrescimento chiaramente individuabili e transizione tra la zona primaverile e la zona tardiva piuttosto brusca. Gli anelli hanno un andamento regolare anche se il loro spessore non è costante. L’abete bianco ha la particolarità, tra le conifere, di non presentare canali resiniferi nel legno ma di avere una corteccia molto ricca di resina ([10]).
Strumento utilizzato
Nel presente studio è stato utilizzato il Resistograph® IML-RESI E400 che utilizza una punta con diametro di 2 mm e lunghezza di 40 cm, dotata di un movimento sia di rotazione che di avanzamento a velocità regolabili. La misura della resistenza alla micro-perforazione viene registrata ogni decimo di millimetro ed i dati vengono memorizzati dalla centralina elettronica che consente anche di trasferire su carta i grafici dei profili di resistenza riscontrati permettendo una prima valutazione in campo dei tracciati. La velocità di avanzamento adottata è stata di 40 cm/min, poiché l’abete bianco è considerato una specie a “legno tenero” e per tali specie sono consigliate velocità comprese tra i 20 ed i 45 cm/min.
Protocollo di rilevamento
In ognuna delle due aree è stato individuato un transetto lungo la massima pendenza (max 10%), con l’ausilio di uno strumento GPS (Trimble GEO XT). Ogni transetto ha una lunghezza di 150 metri ed una larghezza di 15 metri e sono state campionate tutte le piante di abete bianco, ricadenti nel transetto, con diametro a petto d’uomo superiore a 25 cm.
In totale sono state considerate 70 piante nell’abetina di Collemeluccio e 75 in quella di Abeti Soprani. Il numero totale dei profili raccolti è stato di 291: per ogni pianta sono state realizzate due misurazioni con il Resistograph®, una al colletto B ed una a circa 1.30 m di altezza A; solo per la pianta Pf4 sono stati raccolti due profili a petto d’uomo. Inoltre, per ogni esemplare sono stati misurati i relativi diametri.
Infine, a seguito delle prime osservazioni sui profili, in corrispondenza di quelli che presentavano alterazioni nel tracciato, l’indagine è proseguita effettuando dei prelievi di tessuto legnoso con la trivella di Pressler da cui tentare l’isolamento degli eventuali agenti di carie del legno.
Indagini di laboratorio
Per permettere l’isolamento di eventuali miceti agenti di carie, i campioni di legno prelevati sono stati incubati sul substrato di Kuhlman & Hendrix ([17]). I miceli ottenuti sono stati trasferiti su PDA (Potato Dextrose Agar) e MA (Malt Agar) per ottenere le colture in purezza.
L’identificazione dei miceli così isolati è stata effettuata mediante l’osservazione delle caratteristiche microscopiche e macroscopiche del micelio in vitro ([24]). Per i miceti dubbi si è proceduto all’estrazione del DNA ([5]) e successiva amplificazione della regione nucleare ribosomale ITS (Internal Trascribed Spacer) con gli oligonucleotidi ITS4 (TCCTCCGCTTATTGATATGC) e ITS5 (GGAAGTAAAAGTCGTAACAAGG - [27]). L’amplificazione è stata effettuata secondo le seguenti condizioni: 5 min a 95 °C; 33 cicli di 40 sec a 95 °C; 45 sec a 53 °C; 1 min a 72 °C con un estensione finale a 72 °C per 7 min. Successivamente, per tutte le sequenze ottenute è stata effettuata l’analisi BLAST (Basic Local Alignment Search Tool). Per quanto concerne l’identificazione degli isolati del genere Heterobasidion, in cui la dimensione dell’introne mitocondriale permette di discriminare Heterobasidion annosum (0.2 kb) da H. abietinum (1.5 kb - [9]), si è proceduto all’amplificazione del DNA mitocondriale con gli oligonucleotidi Mito7-Mito8 ([11]). L’amplificazione è stata effettuata secondo le seguenti condizioni: iniziale denaturazione di 3 min a 94 °C seguita da 35 cicli di amplificazione con 30 sec di denaturazione a 94 °C, 45 sec a 53 °C e 2 min a 72 °C seguiti da una estensione finale di 7 min a 72 °C.
Analisi statistiche
Tutte le misurazioni effettuate in campo e memorizzate dallo strumento sono state salvate su computer ed elaborate con il programma E-Tools Pro che consente di convertire i tracciati in file di testo per le successive elaborazioni.
Per ciascuna delle due aree, è stata effettuata una cluster analysis (software PAST) dei profili, con il metodo “paired group” e la misura di similarità Euclidea che permette di raggruppare i profili con caratteristiche simili. Dei 291 profili saggiati è stato deciso di utilizzare solo quelli che presentavano una lunghezza almeno pari a 30 cm e per i quali è stato possibile effettuare la cluster analysis elaborando i dati solo per i primi 30 cm. In totale sono stati considerati nello studio 200 profili, 92 per Collemeluccio e 108 per Abeti Soprani.
Risultati
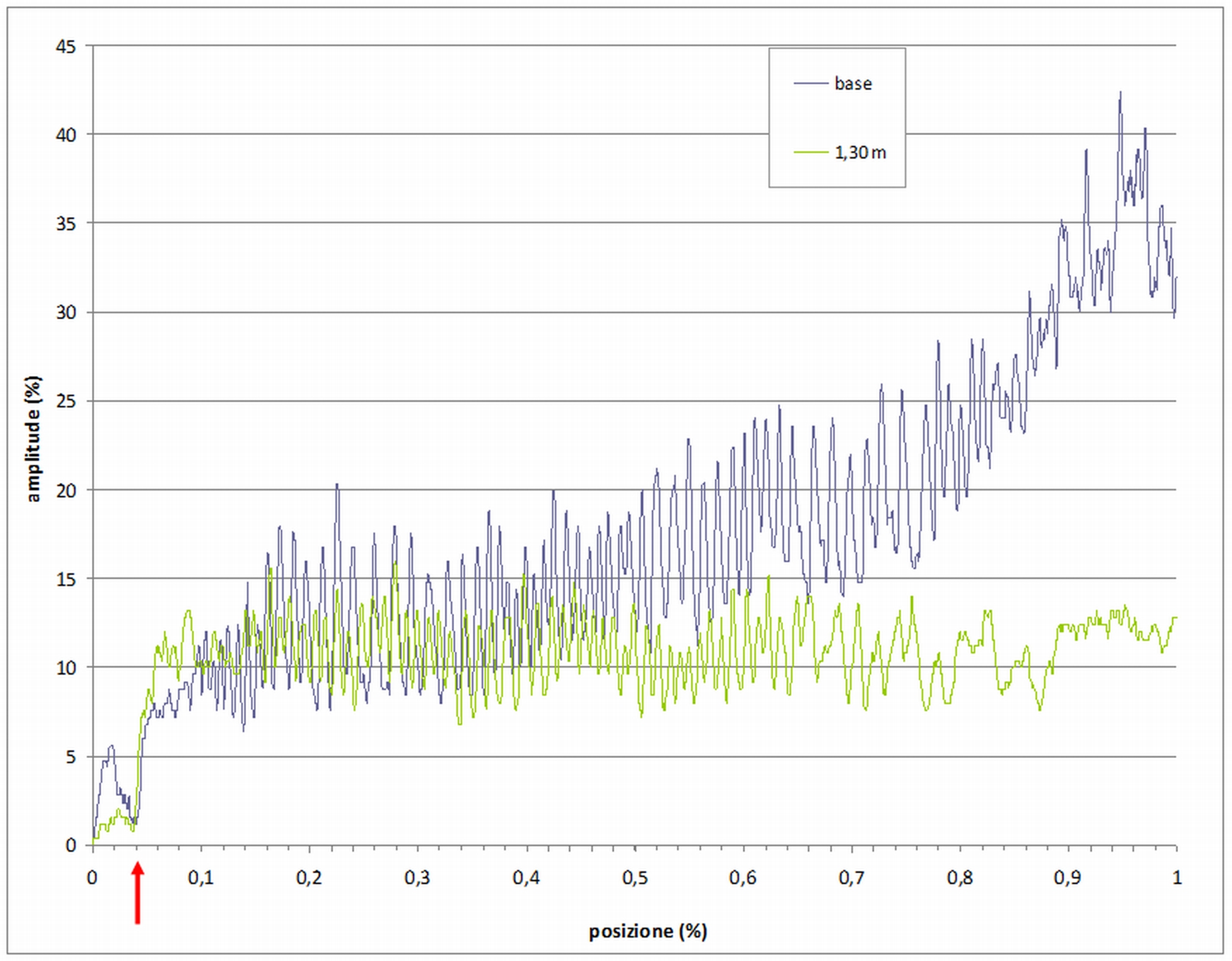
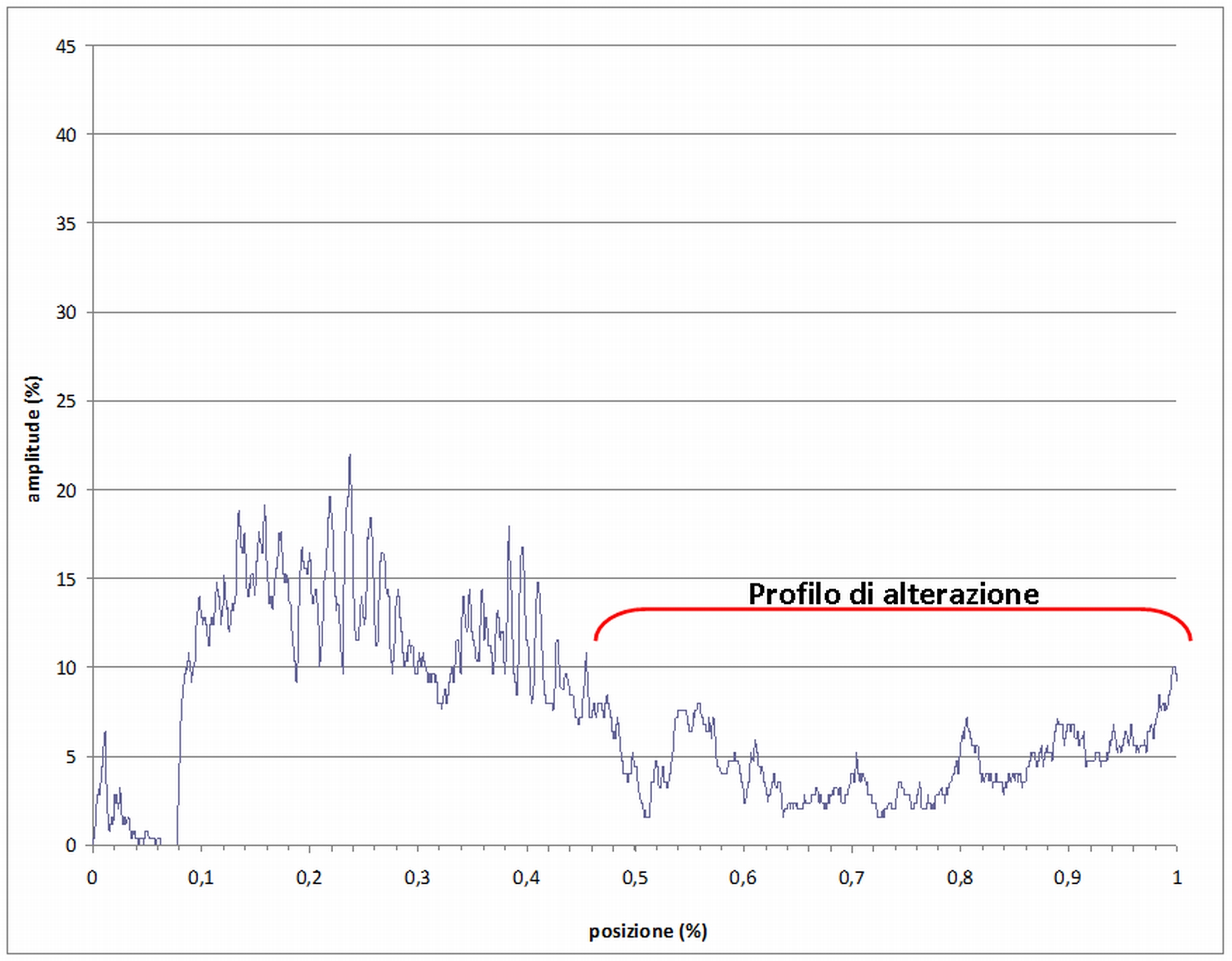
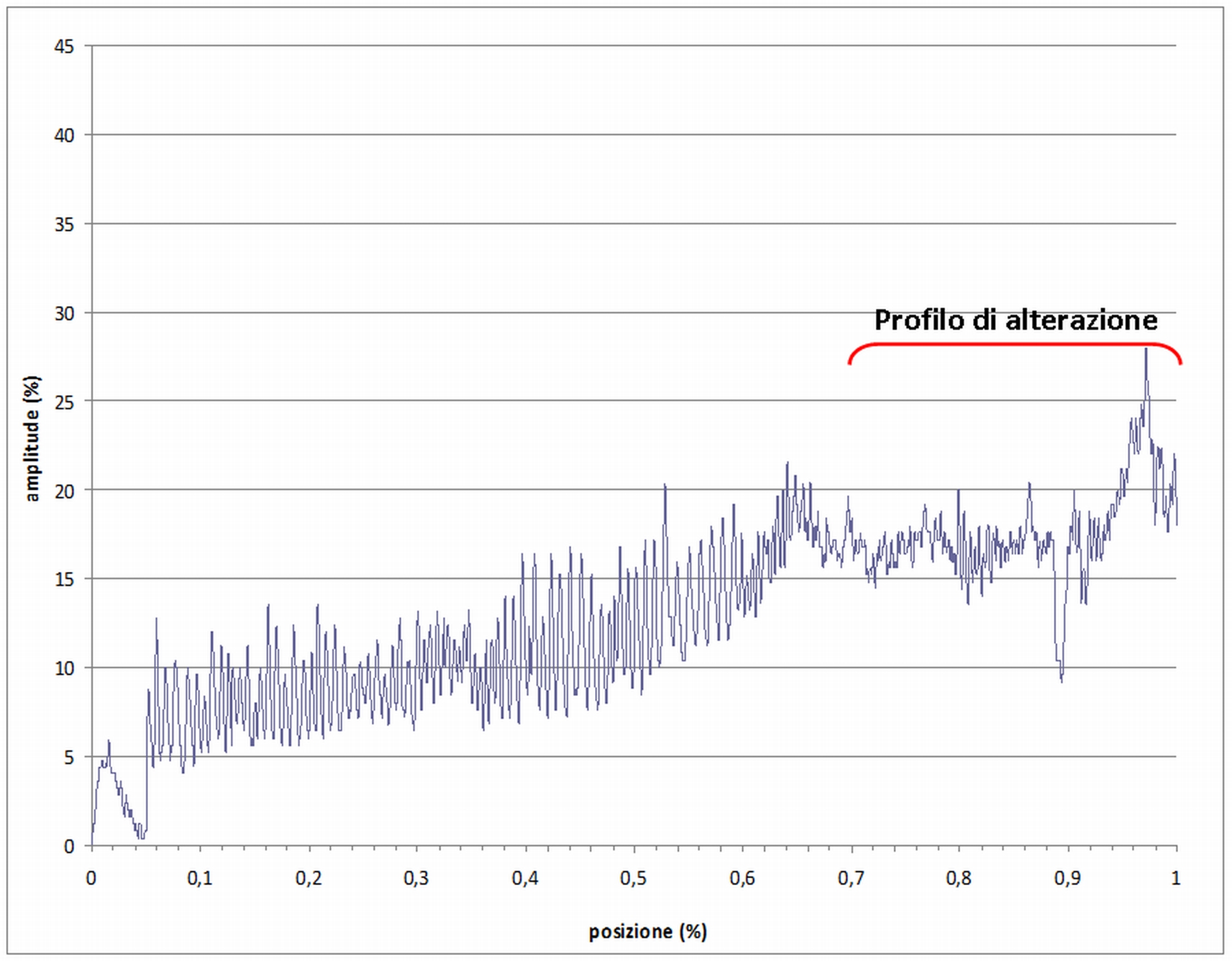
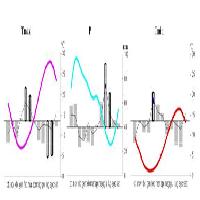
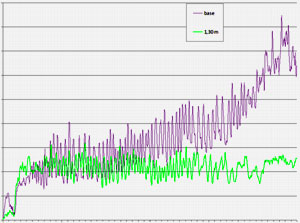
Un primo risultato deriva dalla osservazione dei tracciati che permette di discriminare i profili delle piante sane da quelli con alterazioni. In Fig. 1 si riportano due profili riferibili ad una pianta sana, in quanto evidenziano l’integrità dei tessuti analizzati alla base ed a 1.3 metri di altezza rispettivamente. Le oscillazioni nette che rappresentano l’alternanza di legno primaverile e tardivo degli anelli risultano ben visibili e regolari, quindi prive di alterazioni. Per il profilo realizzato a 1.3 m di altezza, si nota come, una volta superata la corteccia (freccia rossa), le suddette oscillazioni avvengono intorno ad un valore medio pressoché costante (circa 11% di amplitude), mentre per il profilo alla base il valore medio aumenta fortemente in vicinanza del midollo. In Fig. 2 è rappresentato un tracciato rilevato ad 1.30 m con chiara alterazione nel profilo. Infatti, per buona parte del raggio (55%) gli anelli non sono più ben distinguibili a causa del processo di carie del legno che risulta ad uno stadio abbastanza avanzato. Infine, in Fig. 3, il profilo rilevato al colletto presenta alterazioni per circa il 30% del raggio nella parte più interna della pianta. In questo caso, nonostante l’alterazione, nel profilo è ancora possibile riconoscere i picchi che denotano la distinzione tra legno primaverile e legno estivo.
Fig. 1 - Profili di pianta sana (2A - 2B, Abeti Soprani). La scala delle ordinate rappresenta la resistenza alla penetrazione (amplitude) espressa in percentuale. Per rendere più leggibile il grafico sulle ascisse la lunghezza del profilo è stata presentata in percentuale.
Fig. 2 - Profilo (1.30 m) di pianta con evidente alterazione del tracciato (PgA2, Collemeluccio). La scala delle ordinate rappresenta la resistenza alla penetrazione (amplitude) espressa in percentuale. Per rendere più leggibile il grafico sulle ascisse la lunghezza del profilo è stata presentata in percentuale.
Fig. 3 - Profilo (al colletto) di pianta con alterazione del tracciato (22B, Abeti Soprani). La scala delle ordinate rappresenta la resistenza alla penetrazione (amplitude) espressa in percentuale. Per rendere più leggibile il grafico sulle ascisse la lunghezza del profilo è stata presentata in percentuale.
Per l’abetina di Collemeluccio l’11% dei profili, riferibili ad un totale di 8 piante, mostravano alterazioni del tracciato; ad Abeti Soprani le alterazioni erano presenti nel 14% dei casi, riferibili a 12 piante.
I risultati dello studio micologico per i due siti sono riassunti in Tab. 1. Le indagini basate solo sull’identificazione delle caratteristiche morfologiche del micelio hanno permesso di identificare con certezza gli individui afferenti alla specie Fomitopsis pinicola e quelli riferibili al genere Heterobasidion. Le indagini effettuate a livello di DNA mitocondriale hanno permesso di identificare questi ultimi a livello specifico, attribuendoli alla specie H. abietinum. Infine, le analisi effettuate a livello di DNA nucleare hanno consentito di identificare, mediante analisi BLAST: Armillaria ostoyae (99% di identità con sovrapposizione (covery del 99% con FJ664601.1); Ganoderma adspersum (99% di covery e 99% di identità con AY884184.1 e 97% di covery e 99% di identità con AM906057.1) ed Phellinus hartigii (100% di identità con percentuale di covery del 95% con AY558621.1).
Tab. 1 - Risultati dell’indagine micologica suddivisi per sito.
| Località | Piante infette |
Specie fungina identificata |
Metodo di identificazione |
Tipo di carie |
|---|---|---|---|---|
| Collemeluccio | PgB1 | Ganoderma adspersum | rDNA nucleare | Carie bianca |
| PgA2 | Ganoderma adspersum | rDNA nucleare | ||
| 32B | Phellinus hartigii | rDNA nucleare | ||
| 51B | Ganoderma adspersum | rDNA nucleare | ||
| 63B | Heterobasidion abietinum | rDNA mitocondriale | ||
| 24A24B | Heterobasidion abietinum | rDNA mitocondriale | ||
| 27A27B | Armillaria ostoyae | rDNA nucleare | ||
| 69B | Armillaria ostoyae | rDNA nucleare | ||
| Abeti Soprani | 22B | Fomitopsis pinicola | Morfologia del micelio | Carie bruna |
| Pf5APf5B | Fomitopsis pinicola | Morfologia del micelio | ||
| Pf2A | Fomitopsis pinicola | Morfologia del micelio | ||
| Pf4APf4A+Pf4B | Fomitopsis pinicola | Morfologia del micelio | ||
| Pf6APf6B | Fomitopsis pinicola | Morfologia del micelio | ||
| 51A | Phellinus hartigii | rDNA nucleare | Carie bianca | |
| 14B | Ganoderma adspersum | rDNA nucleare | ||
| 71B | Armillaria ostoyae | rDNA nucleare | ||
| 65B | Heterobasidion abietinum | rDNA mitocondriale | ||
| 70B | Heterobasidion abietinum | rDNA mitocondriale | ||
| 9B | Heterobasidion abietinum | rDNA mitocondriale | ||
| 32A | Armillaria ostoyae | rDNA nucleare |
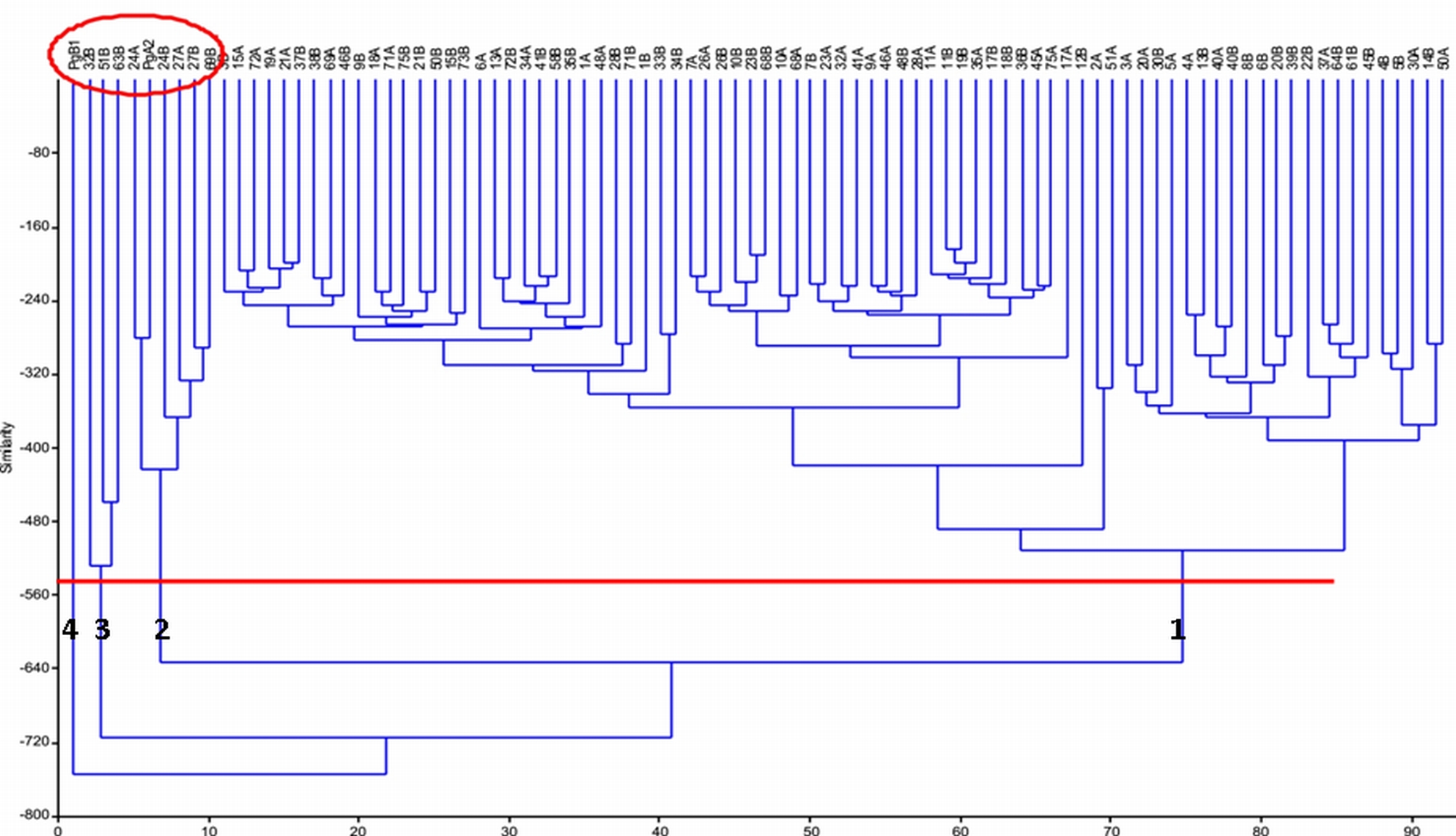
La cluster analysis, applicata ai dati rilevati con il Resistograph® ha, poi, consentito la divisione in diversi gruppi in base alle caratteristiche dei profili. Per Collemeluccio, l’analisi statistica ha permesso di distinguere 4 gruppi (Fig. 4): il gruppo 1 riunisce quei tracciati (82) in cui sono assenti alterazioni, mentre negli altri tre gruppi i profili di densità misurati mostrano diverse “tipologie” di alterazione lungo il tracciato, sia per la posizione che per l’estensione della carie, come esemplificato in Fig. 6. Nonostante le differenze evidenziate, i profili sono accomunati dal fatto che le alterazioni sono tutte causate da agenti di carie bianca (Fig. 4, cerchio rosso, Tab. 1).
Fig. 4 - Cluster analysis effettuata sulle misurazioni raccolte a Collemeluccio. La linea rossa permette di distinguere 4 gruppi (per le spiegazioni si rimanda al testo). Il cerchio rosso indica i profili dove le indagini micologiche hanno permesso di evidenziare la presenza di funghi agenti di carie bianca.
Fig. 6 - Esempi di profili appartenenti a diversi gruppi individuati a Collemeluccio con la cluster analysis. (profilo PgA2: gruppo 2; profilo 32B: gruppo 3; profilo PgB1: gruppo 4) Tutti e tre i profili mostrano delle alterazioni, indicate dalle frecce rosse, in differenti posizioni del tracciato, ma sono il risultato dell’attività di Ganoderma adspersum e Phellinus hartigii, miceti agenti di carie bianca.
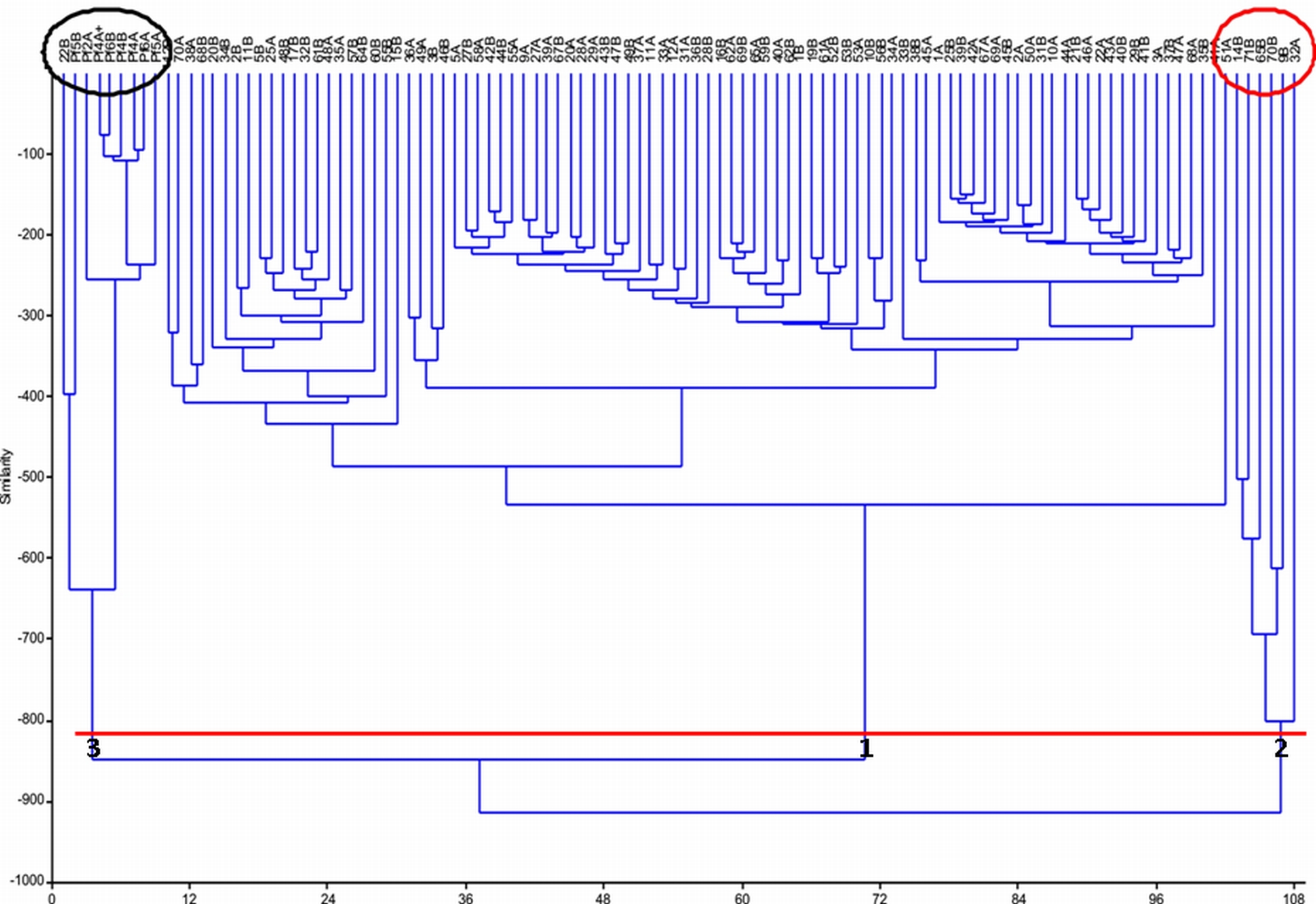
Ad Abeti Soprani, invece, l’elaborazione statistica ha messo in luce la presenza di tre diversi gruppi, evidenziati in Fig. 5. Il gruppo 1 riunisce tutti i profili in cui sono assenti alterazioni (92); il gruppo 2 (cerchio rosso) corrisponde perfettamente alle piante in cui l’indagine micologica ha messo in evidenza l’azione di miceti agenti di carie bianca; infine, il gruppo 3, evidenziato da un cerchio nero, corrisponde alle piante interessate dagli agenti di carie bruna. Una nota particolare riguarda il profilo 51A che afferisce al gruppo 1 pur appartenendo ad un soggetto con carie bianca causata da P. hartigii: si tratta di un’alterazione limitata all’area circostante un nodo, comportamento caratteristico della specie fungina rilevata. Le osservazioni riferite alle diverse alterazioni individuate sono esemplificate in Fig. 7.
Fig. 5 - Cluster analysis effettuata sulle misurazioni realizzate ad Abeti Soprani. La linea rossa permette di distinguere 3 gruppi (per le spiegazioni si rimanda al testo). Il cerchio rosso indica i profili dove le indagini micologiche hanno permesso di evidenziare la presenza di funghi agenti di carie bianca, quello nero, invece, i funghi agenti di carie cubica.
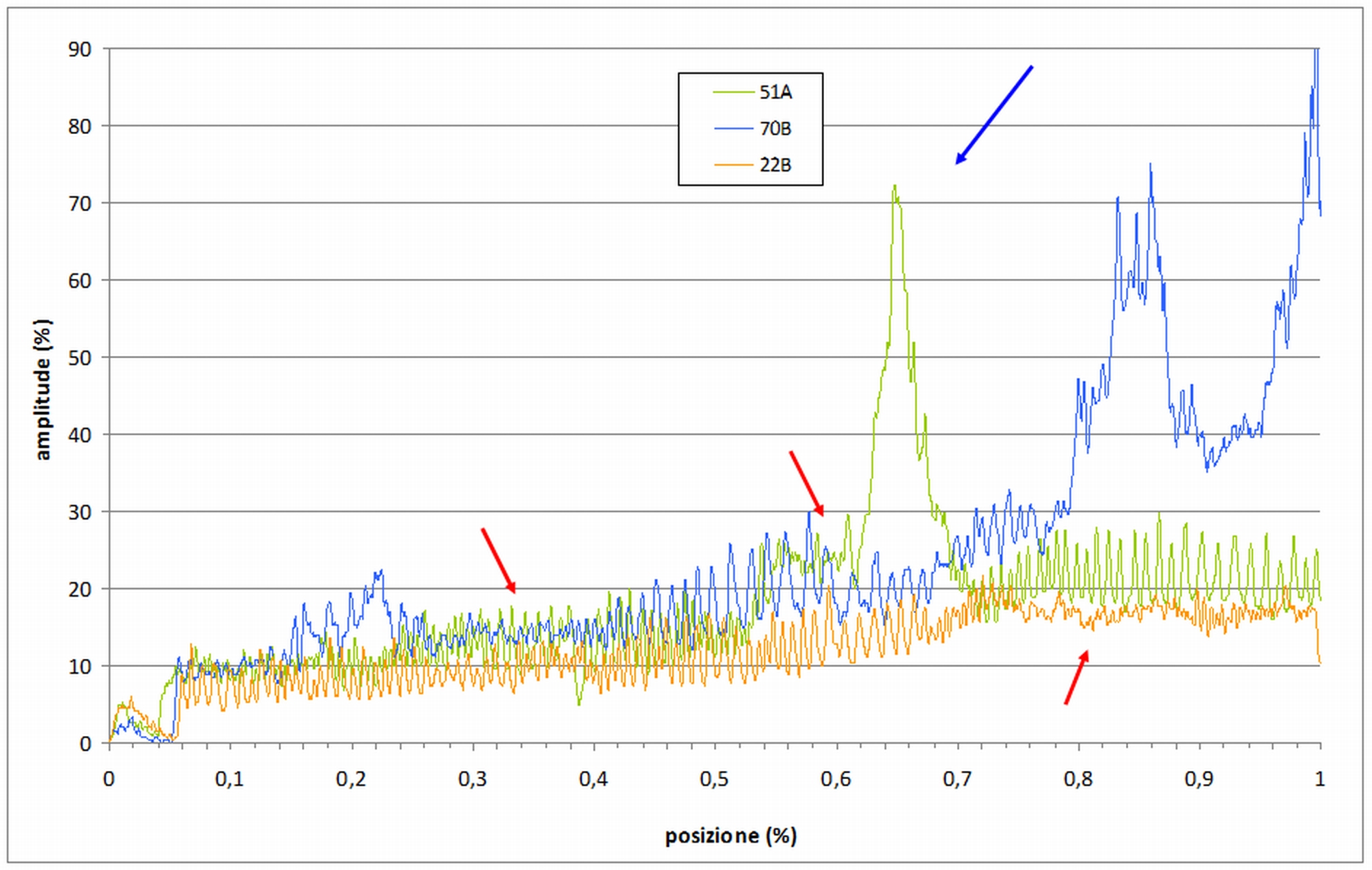
Fig. 7 - Esempi di profili appartenenti a diversi gruppi individuati ad Abeti Soprani con la cluster analysis (profilo 51A: gruppo 1; profilo 70B: gruppo 2; profilo 22B: gruppo 3). Il profilo 51A che afferisce al gruppo 1 appartiene ad un soggetto con carie bianca causata da Phellinus hartigii, ma si tratta di un’alterazione (freccia rossa) limitata all’area circostante un nodo (freccia blu). Il profilo 70B presenta un’alterazione (freccia rossa) causata da Heterobasidion abietinum, il 22B da Fomitopsis pinicola.
Discussione
Tra i pochi lavori scientifici che indagano sulla corrispondenza tra le anomalie nei profili misurati con il Resistograph® e le alterazioni del legno dovute a carie in piante vive, quali quelli di Costello & Quarles ([6]) e di Isik & Li ([14]), non risultano indagini effettuate su abete bianco. Il presente lavoro è da considerarsi, quindi, preliminare, ma i risultati sin qui raccolti permettono di avanzare alcune considerazioni.
Nel sito di Collemeluccio, i profili alterati, tutti da riferirsi all’attività di funghi di carie bianca, sono ben distinguibili da quelli che non presentano alterazioni. Inoltre, è da notare come vi sia una ulteriore diversificazione tra i profili dovuta, non solo all’estensione dell’alterazione, ma anche alla sua posizione all’interno della pianta. Nel sito di Abeti Soprani, invece, sebbene il campione saggiato sia di piccole dimensioni, le analisi effettuate hanno consentito una chiara distinzione dei profili di soggetti interessati da carie bianca da quelli con carie cubica, entrambi presenti nel sito. Lo strumento, quindi, risulta valido per caratterizzare i tipi di carie del legno di abete bianco. Non altrettanto si può dire sull’eventualità di riuscire a distinguere i singoli generi fungini coinvolti. In particolare, nei nostri siti erano presenti diversi agenti di carie bianca: in nessun caso l’analisi statistica ha consentito di differenziare i tracciati in base al fungo presente. Questo potrebbe essere dovuto sia ad una limitata sensibilità dello strumento, che non permette di rilevare le diverse sfumature prodotte dall’attività dei differenti agenti di carie, sia alla limitatezza del campione, non sufficiente ad ottenere dati statisticamente significativi.
Tra gli agenti di carie bianca evidenziati dallo studio micologico, le quattro specie identificate sono state rinvenute, con diversa frequenza, in entrambi i siti. Al contrario, F. pinicola, l’unico agente di carie cubica isolato, è presente esclusivamente nel sito di Abeti Soprani (Tab. 1). Infine, il rinvenimento di G. adspersum su abete bianco vivo è da considerare un elemento di particolare interesse micologico in quanto rappresenta una novità. G. adspersum infatti viene riportato in letteratura come specie normalmente presente solo su latifoglia ([22], [23], [2]). L’unica segnalazione su conifera rintracciata in bibliografia è lo studio di Gottlieb et al. ([12]) che, caratterizzando numerosi isolati con gli isoenzimi, ne inseriscono uno rinvenuto su Pinus taeda L..
In conclusione, in questo studio su abete bianco, l’utilizzo del Resistograph® ha permesso sinora di distinguere solo i due tipi di carie presenti. Un maggiore numero di osservazioni, da elaborare con analisi statistiche più stringenti, permetterà di ottenere informazioni più approfondite, con utili risvolti tecnici per valutare, in piante vive, l’importanza delle carie, in relazione non solo alla loro estensione, ma anche al tipo ed alla posizione nella pianta.
References
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar