Floristic diversity analysis along a fragmentation gradients: a case study of beech forests in the Molisean Appenines (southern Italy)
Forest@ - Journal of Silviculture and Forest Ecology, Volume 8, Pages 137-148 (2011)
doi: https://doi.org/10.3832/efor0677-008
Published: Nov 02, 2011 - Copyright © 2011 SISEF
Research Articles
Abstract
The process of fragmentation of natural habitats is increasing exponentially worldwide and represents one of the foremost threats to biological diversity. Forest fragmentation is considered to heavily affect the demographic and genetic structure of forest plant populations. Habitat fragmentation is a landscape process occurring when areas of continuous habitat are broken into smaller and discontinuous patches. In this paper we analyzed the effects of fragmentation on vascular plant diversity of Fagus sylvatica forest in central Italy (habitat of Community interest -92/43/ECC- “Appenine beech forests with Taxus and Ilex” - cod. 9210*). First, by integrating five parameters that describe beech forest patches structure (patch area, perimeter, shape index, corea area, euclidean nearest neighbor) we identified three levels of fragmentation: high, medium and absent. Then the vascular plants of each level of fragmentation were sampled following a random stratified design. The diversity of vascular plant species was analyzed considering two species groups: all sampled species and “diagnostic” species of the habitat 9210* (sensu Directive 92/43/ECC). We compared the biodiversity patterns of the different fragmentation levels by using rarefaction curves and Rényi’s profiles. We also tested the significance of the founded differences by a bootstrapping procedure. The diversity pattern of the two species groups (diagnostics and all species) showed two opposite trends. As the diversity of the entire pool of species increased on fragmented beech forests the diversity of the diagnostic group decreased. The differences between diversity values of high and low fragmentation levels resulted significant. Our results emphasize the existence of two diagnostic species: Cardamine kitaibelii and Paris quadrifolia that are indicators of not fragmented beech forests. Additionally the diversity pattern of the diagnostics species allow us to propose them as “focal species”, thus it represent a concrete indicator of the conservation status of the Fagus sylvatica with Taxus and Ilex forest.
Keywords
Rarefaction curves, Habitat Directive (92/43/ECC), Vascular flora, Spatial pattern, Rényi diversity profiles, Diagnostic species
Introduzione
La frammentazione dei paesaggi naturali costituisce una delle principali minacce alla diversità biologica a livello planetario ([82], [84], [20], [39], [6]). La frammentazione è un processo che avviene a scala di paesaggio mediante il quale un habitat naturale o seminaturale, che occupa con continuità un’ampia porzione di territorio, viene suddiviso in patch di dimensioni minori ([31], [70], [62], [27]). Tale processo (naturale e/o antropico) interviene sull’eterogeneità naturale del territorio determinando un mosaico di ecosistemi, di tipo naturale, seminaturale e artificiale con strutture e funzioni ben differenziate ([6]). La frammentazione di un paesaggio viene comunemente misurata come variazione in estensione e configurazione spaziale degli habitat naturali e seminaturali, aspetti che possono essere entrambi estrapolati dalla cartografia digitale ([36]). In particolare la frammentazione degli habitat forestali può essere valutata attraverso il calcolo di alcuni parametri di paesaggio, spesso analizzati singolarmente ([65]), come la dimensione delle patches ([66]), la distanza dal vicino più prossimo ([23]), la lunghezza dei bordi (perimetro) e l’estensione della core area ([64]). La frammentazione infatti determina la riduzione dell’estensione delle macchie di bosco, incrementa la distanza tra i lembi relitti che, piccoli ed isolati, sono soggetti a fenomeni di estinzione locale ([34], [27]) e provoca l’aumento dell’habitat di margine ([32]). Queste modifiche del pattern spaziale danno luogo a consistenti modifiche delle condizioni ecologiche e strutturali delle foreste, quali il ritardo nelle dinamiche successionali ([72], [78], [77]), il cambiamento della struttura demografica e genetica dei popolamenti forestali ([68]), la riduzione degli spostamenti delle specie animali ([38]), l’innesco del fenomeno della deriva genetica e della depressione da inbreeding ([51], [43]) e l’ingresso di specie aliene ([12]). Inoltre, lungo i margini forestali neoformati, si innescano una serie di processi ecologici conosciuti nel loro complesso come “effetto margine” ([79], [37]), quali la trasformazione della struttura orizzontale e verticale della vegetazione, le variazioni dei valori di diversità vegetale ed animale ([50], [69]), l’incremento della mortalità degli alberi e l’ingresso di specie ruderali ([52], [45], [49]).
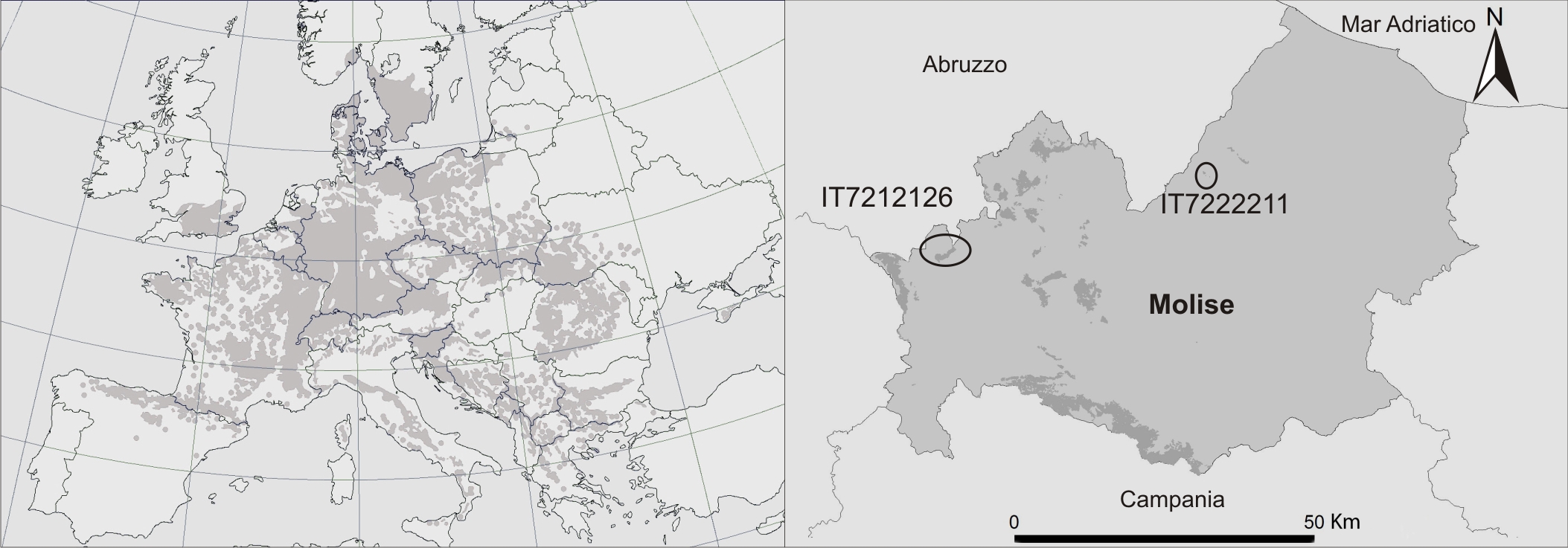
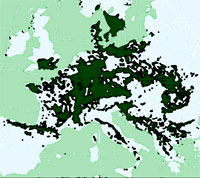
Una tipologia forestale ampiamente diffusa nei paesaggi montanti italiani ed europei è la faggeta ([9] - Fig. 1A). Tuttavia, lo sfruttamento a cui sono state soggette le faggete in Italia ha comportato una diminuzione delle superfici di questi boschi ed ha portato alla scomparsa quasi completa di Fagus sylvatica negli ambienti sotto-ottimali ([9]). In particolare i tagli non adeguati, gli incendi ed il sovrapascolo hanno degradato queste foreste ([8]) e determinato una semplificazione della struttura e composizione dello strato arboreo con una conseguente riduzione della biodiversità. Il grande valore naturalistico dei boschi di faggio e la presenza di fattori antropici che li minacciano hanno portato all’inserimento della maggior parte delle faggete europee nella direttiva Habitat (92/43/EEC - [21]), che rappresenta uno degli strumenti europei più efficaci in materia di tutela della biodiversità. La suddetta direttiva mira alla conservazione degli habitat di interesse, individuati e caratterizzati sulla base di un elenco di specie caratteristiche ([26]) e diagnostiche ([11]) le quali sono delle componenti chiave nella pianificazione e conservazione della biodiversità e richiedono una particolare attenzione, dato il loro ruolo strutturale e funzionale nelle formazioni vegetali; la loro presenza è la sola garanzia dell’esistenza dell’habitat che identificano.
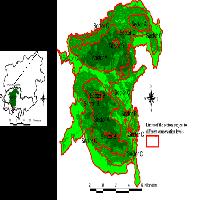
Fig. 1 - (A) Areale di distribuzione delle faggete in Europa ([25], modificato). (B) Area studio e localizzazione delle faggete in Regione Molise (dal Piano Forestale Regione Molise 2002, modificato). Codici SIC: (IT7222287) La Gallinola-Monte Miletto-M. del Matese; (IT7212126) Pantano della Zittola-Feudo Valcocchiara; (IT7222211) Monte Mauro-Selva di Monte falcone.
Ciononostante sono quasi del tutto assenti studi che mettono in relazione il processo della frammentazione alla biodiversità floristica di questi boschi. Per questo motivo, tali aspetti sono stati analizzati nel presente lavoro, relativamente all’habitat forestale di interesse comunitario: “Faggeti degli Appennini con Taxus e Ilex” (9210* sensu Direttiva 92/43/ECC). La nostra ipotesi preliminare è che le specie caratteristiche e le diagnostiche, date le loro peculiarità, siano particolarmente sensibili al fenomeno della frammentazione rispetto a ciò che si può osservare considerando l’intero insieme di specie. Per verificare questa ipotesi sono stati confrontati i valori di diversità tassonomica relativi all’intero pool di specie e alle sole specie diagnostiche dell’habitat 9210* tra i diversi livelli di frammentazione che caratterizzano tale habitat. Per analizzare in modo adeguato il grado di frammentazione delle faggete indagate, si è reso necessario integrare una serie di parametri strutturali ([56], [76], [65]) che ne descrivono l’estensione e la configurazione spaziale.
Materiali e metodi
Area di studio
Lo studio è stato condotto sulle faggete dell’Italia centromeridionale ricadenti in tre siti SIC (Siti d’Importanza Comunitaria) molisani (Fig. 1B - La Gallinola-Monte Miletto-M. del Matese - IT7222287, Pantano della Zittola-Feudo Valcocchiara - IT7212126, Monte Mauro-Selva di Monte falcone - IT7222211). Le faggete indagate appartengono a due associazioni vegetali: l’Aquifolio-Fagetum ([33]) e, limitatamente alle quote più elevate, il Polysticho-Fagetum ([30]). Tali consorzi forestali sono caratterizzati da uno strato arboreo dominato da Fagus sylvatica, e da uno strato erbaceo ricco di specie sciafile legate specificamente al faggio ([61]).
Analisi della frammentazione
Al fine di valutare il processo di frammentazione, aspetto di fondamentale importanza è stato quello di verificare l’estensione effettiva e la disposizione delle varie tessere del mosaico sul territorio. Si è quindi reso necessario esaminare la cartografia relativa all’habitat 9210*. A questo scopo sono state integrate ed aggiornate in ambiente GIS (ASDVJFX 3.2 - [24]) alcune cartografie preesistenti, in particolare la Carta degli Habitat di Direttiva Regione Molise ([1], [2], [3]) e la Carta Forestale su basi Tipologiche della Regione Molise in scala 1:10000 ([4]). L’aggiornamento è stato svolto attraverso fotointerpretazione a video di ortofoto digitali ad alta risoluzione (1 pixel = 1 metro) relative all’anno 2007. Una successiva valutazione della accuratezza cartografica è stata attuata attraverso verifica in campo di una serie di 50 punti casuali. Dal confronto tra la carta dell’habitat e le rilevazioni a terra su punti casuali, è stato costruito un vettore di errore E ([16]). Il vettore contiene un unico rigo nc (tutti i plot attribuiti sulla carta all’habitat) e due colonne ntf (plot riscontrati a terra appartenenti all’habitat) ed ntnf (plot cartograficamente attribuiti all’habitat ma che a terra non lo sono). L’accuratezza totale è stata calcolata come rapporto tra il totale dei plot correttamente classificati e il numero totale di plot, ed è risultata pari allo 0.86. Sulla cartografia aggiornata, sono stati scelte 10 patches di faggeta distribuite su tutto il territorio indagato e rappresentativi dell’eterogeneità spaziale presente, che coprono in totale circa 7200 ha di territorio (94% dell’estensione totale dell’habitat). Per ciascuno di queste patches sono stati calcolati i seguenti parametri strutturali di frammentazione ([54], [63], [55]) utilizzando il software Fragstats 3.3 ([55]): Patch Area, Perimeter, Shape Index (come suggerito da [54]), Euclidean Nearest Neighbor, Core Area (area centrale, in ettari). Per il calcolo di quest’ultimo parametro, è stata utilizzata una distanza dal margine o area buffer di 20 m. Infatti nelle foreste temperate, molti autori ([57], [53], [83], [42]) riportano una zona di transizione tra il margine forestale e la core area compresa tra 20 e 50 metri.
I livelli di frammentazione sono stati individuati attraverso l’analisi di una matrice patch di faggeta x indici strutturali, mediante tecniche di analisi multivariate di classificazione e ordinamento. Il metodo di classificazione applicato, di tipo gerarchico, sfrutta una matrice di similarità (distanza euclidea) fra gli oggetti (patch) come base di aggregazione di quest’ultimi. Per la definizione dei gruppi e la successiva costruzione del dendrogramma si è seguito il criterio della varianza minima (Ward’s method) che si basa sul minimo aumento di varianza interna ai gruppi per ogni fusione ([81]). I risultati sono stati rappresentati in un dendrogramma che sintetizza le distanze tra le singole macchie e tra i gruppi. Successivamente, i gruppi individuati sono stati proiettati nello spazio di ordinamento (Analisi delle Componenti Principali - PCA analysis) in modo da evidenziare la presenza di eventuali gradienti strutturali e di ordinare i gruppi in “livelli di frammentazione”. Entrambe le analisi sono state eseguite mediante l’impiego del software PAST ([44]).
Campionamento floristico
Il campionamento floristico si è svolto secondo uno schema di tipo random stratificato, utilizzando come strati di indagine i diversi livelli frammentazione precedentemente definiti. Sulla carta aggiornata dell’habitat 9210*, è stata sovrapposta, in ambiente GIS, una griglia numerata a maglia quadrata (quadrati 50 x 50). Successivamente si sono estratte delle unità campionarie, per un totale di 37 (quadrati), distribuite nei diversi livelli di frammentazione. Sono stati esclusi i quadrati di bordo, che includevano oltre alla faggeta altre tipologie di uso del suolo contigue. Al centro di ogni quadrato è stato tracciato in campo un plot di 10 m di lato (suddiviso a sua volta in 4 quadranti), all’interno del quale è stata rilevata la flora vascolare. Ad ogni specie censita è stato attribuito un valore di abbondanza variabile tra 1 (presente in un solo quadrante) a 4 (presente nei 4 quadranti). Il riconoscimento dei campioni è stato effettuato utilizzando le chiavi dicotomiche presenti nella “Flora d’Italia” ([61]) mentre la nomenclatura segue quanto riportato nella “Checklist della Flora Italiana” ([18]).
Analisi della diversità
Le analisi effettuate per lo studio delle relazioni esistenti tra diversità tassonomica e livelli di frammentazione si sono svolte considerando l’intero elenco floristico e l’elenco delle specie caratteristiche e diagnostiche dell’habitat 9210*, come descritte rispettivamente nell’Interpretation Manual of European Union Habitats ([26]) e nell’Italian Interpretation Manual of the 92/43/EEC ([11]). Tenendo conto che tutte le specie caratteristiche sono incluse nel più vasto elenco di specie diagnostiche, di seguito si fa riferimento a quest’ultime.
Per ogni livello di frammentazione sono state costruite delle curve di rarefazione (EstimateS v. 8.2 - [15]) relativamente ai due set di specie considerati. La significatività delle differenze tra i livelli di frammentazione è stata valutata considerando gli intervalli di confidenza al 95% delle curve di rarefazione a dimensione campionaria standardizzata (SMaoTao - [15]). Inoltre, è stato calcolato il rapporto tra la curva di rarefazione ottenuta per la ricchezza totale e la curva risultante dalle sole specie diagnostiche ([14], [75]). Da tale rapporto è stato possibile confrontare i due pattern di accumulazione.
Sono state inoltre calcolate le funzioni generalizzate di Rényi ([40], [80]) sui valori di abbondanza specifica per ciascun livello di frammentazione. La funzione generalizzata di Rényi permette di descrivere in un’unica curva, chiamata “profilo di diversità”, i diversi aspetti della biodiversità quali ricchezza, equipartizione e dominanza.
Dato un vettore di probabilità p = (p1, p2, p3, ..., pN), Rényi ([67]) ha proposto un’estensione parametrica dell’indice di Shannon detta entropia generalizzata di ordine a (eqn. 1):
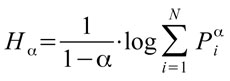
dove 0 ≤ α ≤ ∞ e pi denota l’abbondanza relativa dell’i-esimo elemento del vettore p (i=1, 2, …, N), tale che 0 ≤ pi ≤ ∞, e (eqn. 2):
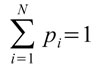
Hill ([40]) ha dimostrato che numerosi indici di diversità ampiamente utilizzati in ecologia sono casi particolari dell’entropia generalizzata Hα. Ad esempio, per α = 0, Hα= logN, dove N è il numero di elementi costituenti il sistema; per α = 1, H1 è pari all’indice di Shannon ([71]); per α = 2, H2= log(1/D), dove D è l’indice di dominanza di Simpson ([73]), e per α = ∞, Hα = log(1/d) = 1/pmax, dove d è l’indice di Berger-Parker ([7]) e pmax è l’abbondanza relativa dell’elemento più abbondante del sistema. Quindi mentre gli indici tradizionali forniscono una descrizione puntuale della struttura del sistema, seguendo la formulazione di Rényi, si ottiene un continuum di misure di diversità che pesano in maniera differenziata la presenza di elementi più o meno abbondanti in funzione del valore assunto dal parametro α ([58], [59]). Per un sistema biologico, come ad esempio una formazione forestale, Hα è una funzione decrescente di α. In altre parole, variando il valore di α, è possibile ottenere una descrizione vettoriale della struttura floristica del bosco che può essere rappresentata attraverso il suo profilo di diversità Hα vs. α.
Per confrontare i livelli di frammentazione sono stati calcolati e rappresentati graficamente i profili di diversità di Rényi per valori di α che variano da 0 a 4. Quando due profili non si sovrappongono vengono considerati confrontabili. Inoltre è stata calcolata la significatività delle differenze tra i valori di diversità (Ricchezza, Shannon, Simpson e Berger-Parker), nei differenti livelli di frammentazione utilizzando la procedura di ricampionamento numerico con rimpiazzo (bootstrapping - [22]).
Risultati
Analisi della frammentazione
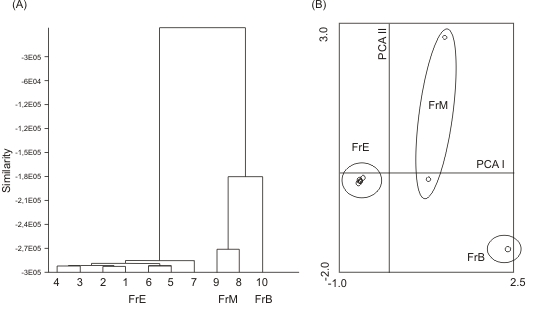
L’analisi degli indici strutturali delle patches di faggeta attraverso classificazione e ordinamento multivariato (PCA) ha messo in evidenza la presenza di tre gruppi (Fig. 2, Tab. 1) riconducibili a tre livelli di frammentazione: elevato (FrE), medio (FrM) e nullo (FrN - Tab. 2). Il livello di frammentazione elevato è costituito da patches piccole, con forme regolari, distanti tra loro e con core area di estensione modesta; il livello di frammentazione medio, è caratterizzato da patches di dimensioni medie, relativamente vicine tra loro e con una core area di dimensioni intermedie; il livello di frammentazione nullo è rappresentato da una patch molto estesa, di forma irregolare, con una core area molto grande e che dista molto poco da un’altra patch di faggeta (Tab. 2). Per ogni livello di frammentazione il campionamento è stato distribuito nel seguente modo: 15 campioni per il livello nullo, 12 campioni per il livello medio e 10 campioni per il livello elevato.
Fig. 2 - Risultato della classificazione attraverso cluster analysis gerarchico (A) e dell’analisi di ordinamento PCA (Principal Components Analysis). La percentuale di varianza spiegata dai primi due assi della PCA corrisponde al 83.54 % per il primo (PCA I) e al 11.14 % per il secondo (PCA II). (B) delle patch in base ai loro indici di struttura. Il taglio del dendrogramma ad un livello di dissimilarity pari a 2 permette di individuare tre livelli di frammentazione: (FrE) frammentazione elevata; (FrM) frammentazione media; (FrN) frammentazione nulla.
Tab. 1 - Valori di correlazione tra i parametri strutturali ed i primi due assi di PCA (PCA I e PCA II). PA: Patch Area (Ha); P: Perimetro (m); SI: Shape Index; CA: Core Area (m); ENN: Euclidean Nearest Neighbor (m).
| Parametro | PCA I | PCA II |
|---|---|---|
| PA | 0.956 | 0.252 |
| P | 0.99 | 0.094 |
| SI | 0.898 | -0.133 |
| CA | 0.946 | 0.268 |
| ENN | -0.755 | 0.62 |
Tab. 2 - Valori medi degli indici strutturali calcolati per le patches di faggeta indagate. PA: Patch Area (ha); P: Perimetro (m); SI: Shape Index; ENN: Euclidean Nearest Neighbor (m); CA: Core Area (m); ES: errore standard.
| Classe | N patches | PA | P | SI | ENN | CA | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Media | ES | Media | ES | Media | ES | Media | ES | Media | ES | ||
| Elevato | 7 | 23 | 10.27 | 3260 | 1142 | 1.83 | 0.19 | 18.29 | 8.79 | 259.41 | 53.27 |
| Medio | 2 | 1364 | 358.12 | 149290 | 15550 | 10.52 | 2.46 | 1160.73 | 379.12 | 23.46 | 16.11 |
| Nullo | 1 | 4249 | - | 284740 | - | 10.92 | - | 3865.6 | - | 7.46 | - |
Frammentazione e diversità floristica
Il campionamento floristico ha permesso di rilevare 158 taxa che rappresentano circa l’80% della flora vascolare descritta per le faggete dell’Italia centromeridionale ([10], [5]). Le specie diagnostiche rinvenute sono 33 (Tab. 3) e rappresentano il 21% della flora vascolare totale. Tra le specie diagnostiche 19 sono presenti in tutti i livelli di frammentazione e alcune di loro con valori di frequenza elevati: Fagus sylvatica, Viola reichenbachiana, Cardamine bulbifera, Sanicula europaea, Rubus hirtus, Galium odoratum, Aremonia agrimonioides, Mycelis muralis, mentre altre, quali Cardamine kitaibelii, Paris quadrifolia e Potentilla micrantha sono esclusive del livello di frammentazione nullo, mentre non esiste alcuna specie focale esclusiva del livello di frammentazione elevato (Tab. 3). E’ da notare che Taxus baccata, la cui distribuzione nelle faggete meridionali risulta essere molto ridotta e discontinua ([74]), è assente nelle faggete molto frammentate. Ilex aquifolium, che caratterizza oltre alle faggete molte altre foreste come i boschi montani di leccio e di latifoglie decidue ([19]), risulta presente in tutte le categorie di frammentazione con una tendenza ad incrementare nelle faggete frammentate.
Tab. 3 - Distribuzione delle specie diagnostiche nei tre livelli di frammentazione (FrN: frammentazione nulla; FrM: frammentazione media; FrE: Frammentazione elevata). I valori sono espressi come percentuale dei quadranti campionati. Tra parentesi viene riportato il numero di quadranti per classe di frammentazione. (*): specie comuni nei tre livelli di frammnetazione; (**): specie esclusive del livello di frammentazione nullo.
| Specie | FrN (60) | FrM (48) | FrE (40) | Specie | FrN (60) | FrM (48) | FrE (40) |
|---|---|---|---|---|---|---|---|
| Abies alba | 13.30 | 0.00 | 5.00 | * Galium odoratum | 55.00 | 54.17 | 12.50 |
| Acer platanoides | 0.00 | 2.10 | 0.00 | Ilex aquifolium | 1.67 | 14.58 | 17.50 |
| Acer pseudoplatanus | 3.30 | 2.10 | 7.50 | Lathyrus venetus | 0.00 | 10.42 | 0.00 |
| Actaea spicata | 5.00 | 4.20 | 0.00 | Lathyrus vernus | 16.67 | 16.67 | 7.50 |
| Anemone apennina | 20.00 | 22.90 | 20.00 | Melica uniflora | 11.67 | 14.58 | 32.50 |
| Anemone nemorosa | 5.00 | 0.00 | 17.00 | * Mycelis muralis | 40.00 | 41.67 | 27.50 |
| * Aremonia agrimonoides | 46.70 | 52.10 | 27.50 | Oxalis acetosella | 23.33 | 8.33 | 0.00 |
| * Cardamine bulbifera | 70.00 | 39.60 | 67.50 | ** Paris quadrifolia | 3.33 | 0.00 | 0.00 |
| Cardamine chelidonia | 1.70 | 2.10 | 2.50 | Polygonatum multiflorum | 10.00 | 14.58 | 15.00 |
| ** Cardamine kitaibelii | 30.00 | 0.00 | 0.00 | Polystichum aculeatum | 6.67 | 8.33 | 0.00 |
| Cephalanthera damasonium | 18.30 | 47.92 | 20.00 | ** Potentilla micrantha | 1.67 | 0.00 | 0.00 |
| Corydalis cava | 6.70 | 0.00 | 5.00 | Ranunculus lanuginosus | 40.00 | 10.42 | 20.00 |
| Doronicum orientale | 6.70 | 10.42 | 0.00 | * Rubus hirtus | 56.67 | 68.75 | 75.00 |
| Dryopteris filix-mas | 6.70 | 10.42 | 12.50 | * Sanicula europaea | 58.33 | 33.33 | 20.00 |
| Euphorbia amygdaloides | 23.30 | 10.42 | 17.50 | Taxus baccata | 5.00 | 2.08 | 0.00 |
| * Fagus sylvatica | 91.70 | 95.83 | 87.50 | * Viola reichenbachiana | 86.67 | 70.83 | 55.00 |
| Galanthus nivalis | 0.00 | 2.08 | 5.00 | - | - | - | - |
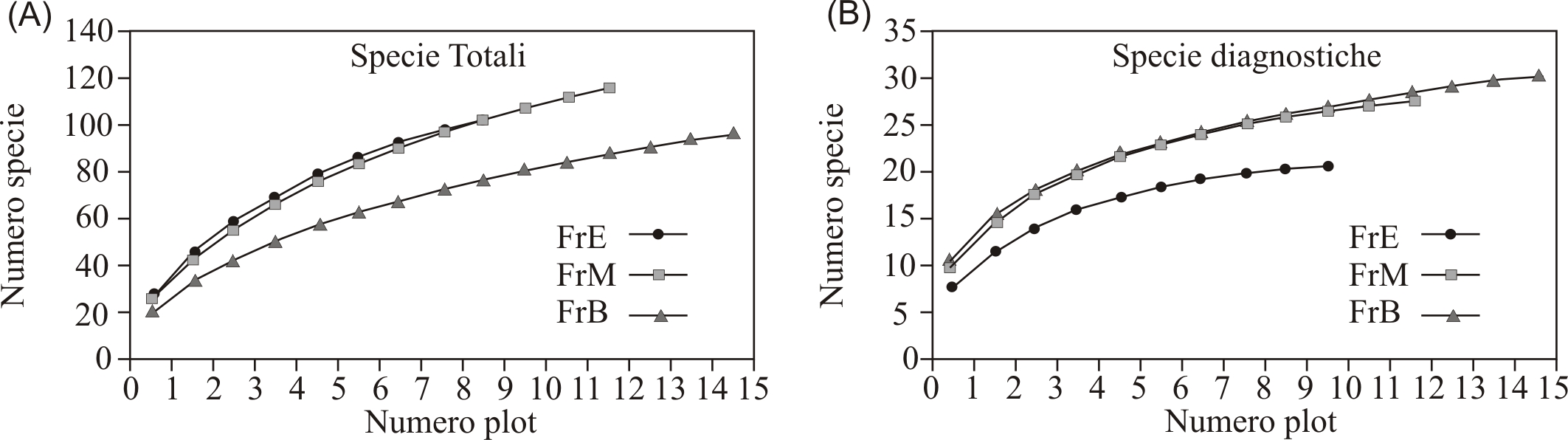
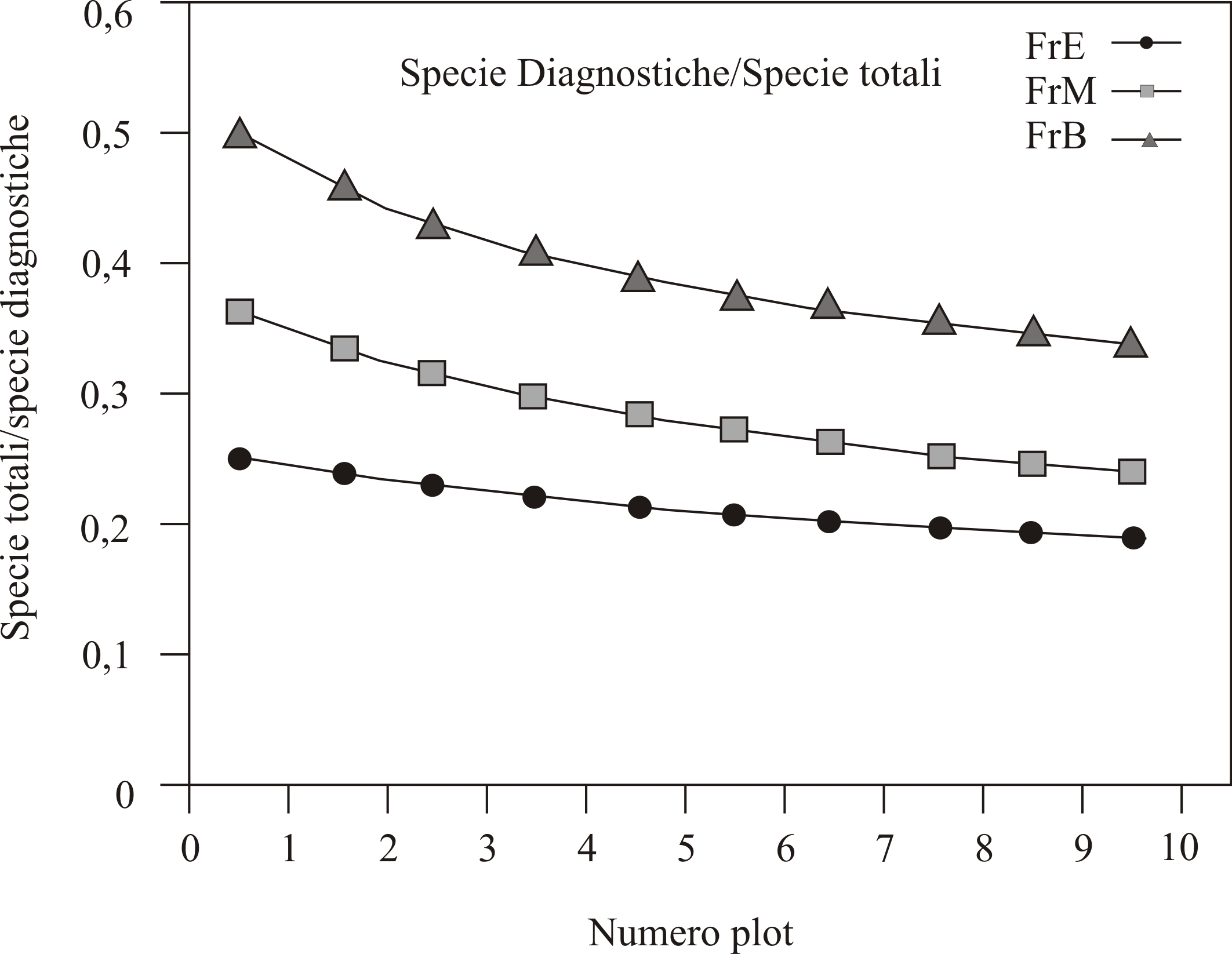
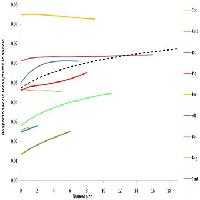
L’analisi delle curve di accumulazione ha messo in evidenza dei pattern di diversità distinti nei tre livelli di frammentazione (alto, medio e nullo - Fig. 3). Il confronto delle curve di rarefazione per l’intero pool di specie (Fig. 3A) mostra valori di diversità maggiori nelle faggete a frammentazione elevata e media rispetto alle faggete poco frammentate. Le curve di rarefazione calcolate sulle specie diagnostiche (Fig. 3B) invece, presentano un pattern di accumulazione opposto a quello delle specie totali. Infatti, le curve dei livelli di frammentazione medio e nullo sono al di sopra (più ricche in specie diagnostiche) della curva del livello di frammentazione elevato. Di conseguenza, il rapporto tra le curve di rarefazione delle specie diagnostiche e delle specie totali (Fig. 4) ha messo in evidenza un contributo delle specie diagnostiche, sull’intero pool di specie, più cospicuo nel livello di frammentazione nullo ed invece minore nei livello di frammentazione elevato. In particolare osservando la pendenza della curva del livello di frammentazione elevato (FrE foc/tot) emerge che le specie diagnostiche mostrano sostanzialmente lo stesso tasso di accumulazione delle specie totali, quindi il loro contributo alla diversità specifica è costante. Al contrario, l’elevata pendenza della curva relativa al livello di frammentazione nullo (FrN foc/tot) denota che le specie diagnostiche all’interno dei plot sono molto comuni e che sono sufficienti pochi rilievi per intercettarne la maggior parte.
Fig. 3 - Curve di rarefazione generate tramite il software EstimateS 9.2 costruita sulle specie totali (A) e sulle specie diagnostiche (B). (FrE): livello di frammentazione elevato; (FrM): livello di frammentazione medio; (FrN): livello di frammentazione nullo.
Fig. 4 - Rapporto tra le curve di rarefazione costruite per le specie diagnostiche e per le specie totali, nei tre livelli di frammentazione.(FrE): livello di frammentazione elevato; (FrM): livello di frammentazione medio; (FrN): livello di frammentazione nullo.
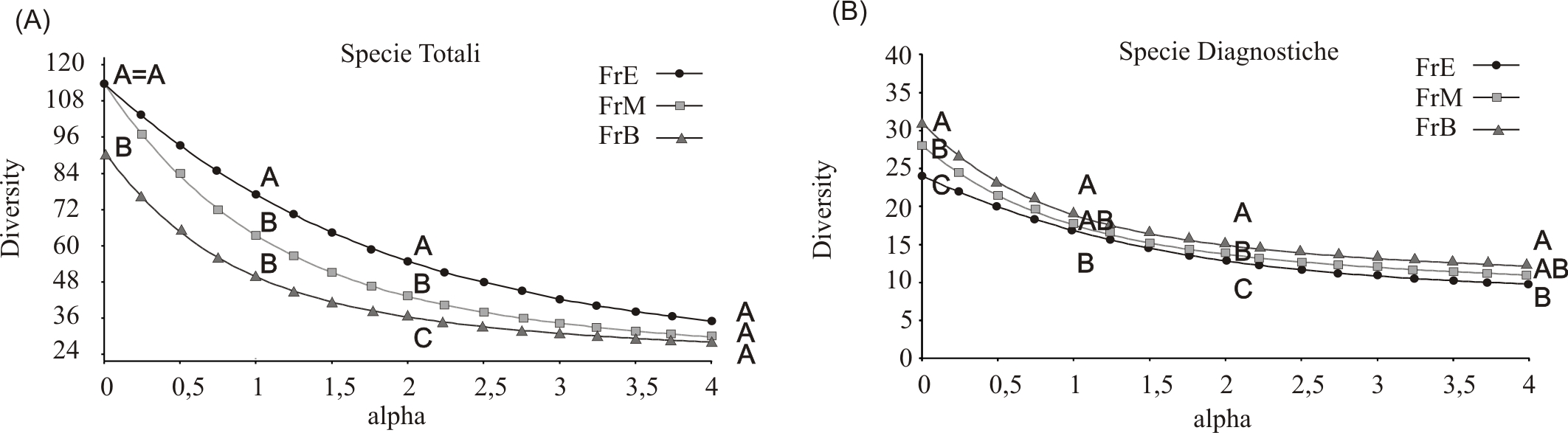
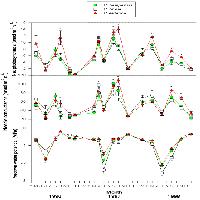
Esaminando i profili di diversità floristica di Rényi (Fig. 5) risulta che le curve sono confrontabili, non essendoci sovrapposizioni tra le stesse. I profili di Rényi in contesti più frammentati confermano la co-presenza di elevati valori di diversità totale e di bassi valori di diversità di specie diagnostiche. Al contrario, le medesime curve relative alle faggete a frammentazione bassa, evidenziano una maggiore diversità di specie diagnostiche e una minore diversità di specie totali. Per quanto riguarda le specie totali (Fig. 5A), si osservano differenze significative (p<0.05) tra i profili relativi ai livelli di frammentazione elevato e nullo per α=0 (ricchezza), per α=1 (indice di Simpson) e α=2 (indice di Shannon), mentre non si riscontrano differenze significative (p>0.05) per α=4 (indice di Berger-Parker). Tra i livelli di frammentazione elevato e medio sono emerse differenze significative (p<0.05) per gli indici di Simpson e di Shannon, mentre differenze non significative (p>0.05) sono state registrate per la ricchezza e per l’indice di Berger-Parker. Stessi valori di significatività sono stati riscontrati tra frammentazione media e frammentazione bassa. Confrontando le sole specie diagnostiche (Fig. 5B) tra frammentazione elevata e bassa, sono emerse differenze significative per tutti gli indici di diversità considerati (p<0.05). Le differenze negli indici di diversità relative alle specie diagnostiche tra livelli di frammentazione elevato e medio e tra medio e nullo risultano solo parzialmente significative. Tra il livello elevato e medio le differenze sono significative per la ricchezza e per l’indice di Simpson mentre tra medio e nullo lo sono per Shannon e Simpson.
Fig. 5 - Profili di diversità di Rényi costruiti per le specie totali (A) e per le specie diagnostiche (B), nei tre livelli di frammentazione: FrE = livello di frammentazione elevata; FrM = livello di frammentazione media; FrN = livello di frammentazione nullo. Indici di diversità: alpha) = 0: ricchezza; = 1: Indice di Simpson; = 2: Indice di Shannon; = 4: Indice di Berger-Parker. Le lettere A, B, C all’interno dei diagrammi indicano differenze significative (: p<0.05).
Discussione e conclusioni
L’analisi della diversità floristica totale e delle specie diagnostiche dell’habitat nei diversi livelli di frammentazione ha messo in evidenza consistenti differenze ecologico-funzionali associate a questo gradiente di disturbo.
La distribuzione delle specie diagnostiche nei campioni relativi ai diversi livelli di frammentazione non è omogenea. Tra queste esiste un gruppo di specie sempre presenti, tipiche di faggeta come Fagus sylvatica, Viola reichenbachiana, Cardamine bulbifera, Sanicula europaea, Rubus hirtus, Galium odoratum, Aremonia agrimonioides, Mycelis muralis ([61]). La fedeltà di questo gruppo di specie permette di confermare l’identità dell’habitat “Faggeti degli Appennini con Taxus e Ilex” (sensu Direttiva 92/43/EEC). Esiste inoltre un insieme di specie diagnostiche presenti esclusivamente nei boschi a bassa frammentazione tra cui Cardamine kitaibelii, Paris quadrifolia e Potentilla micrantha. Questi risultati sono in linea con quanto riportato da Honnay & Hermy ([41]) che definiscono Paris quadrifolia come una specie indicatrice dei boschi temperati maturi (true forest species) e con Pignatti ([61]) che descrive questa specie insieme a Cardamine kitaibelii come caratteristica delle faggete centromeridionali ben strutturate e mature. Alla luce di tali considerazioni e dei risultati ottenuti possiamo proporre queste due specie come indicatrici di faggete integre e con un livello di frammentazione nullo.
L’analisi delle curve di rarefazione e dei profili di Rényi relative alle specie diagnostiche ha messo in evidenza una significativa riduzione dei valori di diversità all’aumentare della frammentazione. Queste tendenze, che risultano opposte a quelle riscontrate nell’intero pool di specie, sottolineano l’importate ruolo della diversità delle specie diagnostiche come bioindicatore di disturbo dell’habitat. Le caratteristiche ecologiche di alcune specie diagnostiche, quali Cardamine kitaibelii, Paris quadrifolia, e la loro sensibilità al disturbo, ci permettono di proporle come specie “focali” (focal species), concetto ampiamente utilizzato ed applicato in ecologia della conservazione della fauna ([48], [13]), ma ancora poco diffuso in ecologia vegetale e forestale ([14]).
L’analisi della diversità floristica attraverso le curve di rarefazione ([35]) ha messo in evidenza una ricchezza totale superiore nelle aree maggiormente frammentate (SMAO-TAO per n=1 e per n=10). Questa tendenza dell’intero pool di specie viene confermata dall’analisi dei profili di diversità di Rényi, dove le situazioni molto frammentate presentano valori di diversità significativamente maggiori rispetto a quelle non frammentate. Questi risultati confermano, come riportato da Kerr et al. ([46]) e Fairbanks & McGwire ([28]), che la frammentazione, porta ad un aumento della ricchezza specifica. L’incremento della diversità tassonomica all’interno del bosco frammentato potrebbe essere in parte interpretato alla luce della teoria del disturbo intermedio ([17]), la quale postula l’esistenza di valori di diversità floristica massimi negli ambienti moderatamente perturbati. E’ tuttavia da sottolineare che i risultati ottenuti non concordano con alcuni lavori precedenti che descrivono una diminuzione della diversità floristica in foreste molto frammentate ([47], [60], [66]) Le discordanze riscontrate sono da ricondurre principalmente alla differente modalità adoperata in questi lavori per definire i livelli di frammentazione. I lavori sopracitati descrivono la frammentazione solo in base all’estensione delle macchie (patches) ed alla distanza tra di loro. Secondo questo schema le macchie grandi ospitano una maggiore biodiversità dovuta alla loro elevata eterogeneità di condizioni pedologiche e geomorfologiche, la maggiore diversificazione della struttura arborea e la maggiore disponibilità di microambienti ([43]). Inoltre, nelle patches lontane ed isolate si verifica una probabilità di estinzione locale maggiore. A differenza dei lavori appena descritti, i livelli di frammentazione da noi definiti tengono conto anche dei parametri di estensione dei contatti, forma e core area. In questo modo abbiamo aggiunto ai due aspetti importanti della frammentazione come l’estensione e l’isolamento un terzo elemento altrettanto importante come l’effetto margine. L’introduzione di nuovi bordi nelle faggete, ha dato luogo a valori di biodiversità complessiva elevati dovuti in parte all’ingresso di specie che colonizzano nuovi microambienti e in parte a condizioni microclimatiche particolari ([32], [52], [45], [49], [29]).
Ringraziamenti
Si ringraziano i due revisori anonimi della rivista che con i loro preziosi suggerimenti hanno contribuito a migliorare la prima versione del manoscritto. Un ringraziamento speciale al Dott. Celestino Rigoletti ed alla Dott.ssa Carmen Giancola per il loro prezioso contributo nel lavoro di campo e nella identificazione dei campioni di flora.
References
Online | Google Scholar
Online | Google Scholar
Online | Google Scholar
Online | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Online | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar