A bio-indicator for the evaluation of quality forestry and landscape fragmentation
Forest@ - Journal of Silviculture and Forest Ecology, Volume 10, Pages 94-102 (2013)
doi: https://doi.org/10.3832/efor1040-010
Published: Nov 05, 2013 - Copyright © 2013 SISEF
Technical Advances
Abstract
A bio-indicator for the evaluation of quality forestry and landscape fragmentation. Intensive agricultural practices, as well as tourism development, summer fires, urbanization and air pollution represent a serious threat for many woodlands in Mediterranean Europe. Tawny owls, Strix aluco, is a valuable indicator of habitat quality and shows high sensitivity to wood fragmentation. Assessing the association between Tawny owls and their habitat may provide useful tools for conservation and management of forested habitats. Populations of woodland birds are influenced by forest characteristics, wood proportion being a key factor explaining breeding density and regularity in nest spacing. Populations of the Tawny Owl reach their highest densities in old deciduous forests. The distribution of territories remains almost constant for many years, and the period during which any particular wood maintains suitable conditions for nesting depends on factors like tree species and management, especially on the timing and extent of thinning. To assure the maintenance of good habitat quality in most woodlands, regulation of water diversion, prevention of summer fires, and a general reduction of human activities inside forests seem to be useful conservation tools.
Keywords
Introduzione
La frammentazione ambientale è un processo dinamico dovuto a cause antropiche e conduce ad una suddivisione della copertura boschiva in frammenti più o meno separati e progressivamente isolati. La frammentazione interviene così sull’eterogeneità del paesaggio portando all’accostamento più o meno marcato di ecosistemi naturali, seminaturali e artificiali con conseguenze a tutti i livelli di organizzazione ecologica ([12], [18]). La frammentazione degli ambienti naturali costituisce una grave minaccia per la diversità biologica. Essa influisce su popolazioni animali e vegetali, influenzando gli spostamenti degli individui e la loro presenza, abbondanza e persistenza con conseguenze a livello di comunità e di ecosistema ([71], [66]). Gli effetti della frammentazione sono riscontrabili a scale geografiche differenti. Alla scala di paesaggio la frammentazione porta alla strutturazione di “eco-mosaici” nei quali è possibile distinguere una matrice antropica, formata per la scomparsa o alterazione di preesistenti tipologie vegetazionali, all’interno della quale sono collocati i frammenti residui ([19]).
La matrice non si amplia casualmente, infatti sono le aree più favorevoli alle attività umane che vengono trasformate più rapidamente ([64], [66]). I frammenti di grandi dimensioni hanno una maggiore ricchezza di habitat, quindi una maggiore disponibilità di risorse può supportare popolazioni più numerose rispetto a frammenti di dimensioni minori. Unità relitte, soprattutto se di piccole dimensioni, possono andare incontro ad alterazioni micro-climatiche e mutamenti dei parametri abiotici con conseguenze sulla componente biotica. Un’area di ridotte dimensioni è, infatti, maggiormente soggetta a luminosità, variazioni di umidità, regime dei venti, sbalzi di temperature rispetto ad unità ecosistemiche dello stesso tipo di più ampie dimensioni. In aree relitte di dimensioni contenute, quindi, si verifica una riduzione fisica degli habitat disponibili, con un conseguente aumento della probabilità di estinzione di specie, poiché la superficie può essere insufficiente a mantenere una popolazione vitale ([2]).
Gli effetti della frammentazione ambientale sono specie-specifici ([9]), e la frammentazione influenza, a livello individuale, il comportamento e i movimenti di molte specie animali ([22]). La capacità di persistenza delle specie animali in ambienti frammentati dipende così sia dalle caratteristiche eco-etologiche di ciascuna specie sia da fattori e processi ambientali estrinseci oltre che dal tipo, grado, modalità, scala e fase temporale del processo di frammentazione ([64], [8], [16], [12]).
Tra le caratteristiche intrinseche alle specie necessarie a valutare la sensibilità di ciascuna al processo di frammentazione si possono considerare: l’ampiezza di nicchia, le dimensioni dell’home-range, l’uso dei frammenti del mosaico ambientale, la predisposizione a disperdersi ([8], [16]).
Le specie con popolazioni poco numerose, che hanno bisogno di aree di rilevante estensione, che sono soggette a fluttuazioni demografiche, che hanno un basso potenziale riproduttivo e una capacità dispersiva limitata, oltre che una elevata specializzazione, possono rientrare tra le specie intrinsecamente più sensibili al processo di frammentazione ([2]). Le specie possono essere distinte in tipi ecologicamente differenti sulla base del loro legame a condizioni presenti nei frammenti e alla loro sensibilità all’effetto margine ([71]). Molti rapaci forestali, legati anche ad ambienti aperti, sono relativamente abili a disperdersi in paesaggi con un certo grado di frammentazione, incorporando più frammenti all’interno del loro home-range e compensando così la perdita di habitat idoneo dovuta a frammentazione ([42]). Capita infatti che individui di queste specie possano essere trovati in piccoli frammenti utilizzati come stepping-stones per le loro dinamiche a più ampia scala di paesaggio ([13]). Le stepping stones sono frammenti di habitat ottimale che possono fungere da aree di sosta e rifugio per determinate specie altamente vagili. Tra queste ritroviamo specie abili ad effettuare movimenti a medio o breve raggio attraverso ambienti non idonei, ma anche specie che compiono spostamenti a lungo raggio.
Alcune specie legate ad ecosistemi forestali maturi mostrano una accentuata sensibilità alla variabile superficie del frammento. Tra queste vi sono alcuni grandi predatori, piciformi, ed anche alcuni passeriformi relativamente diffusi ([26]). La qualità ambientale può incidere sulla riduzione dell’idoneità ecologica di frammenti residui di habitat per determinate specie. Gli incendi e la ceduazione in aree forestali, gli stress ecologici dovuti all’abbassamento della falda freatica o a oscillazioni improvvise del livello delle acque in aree umide sono tra i disturbi di origine antropica che possono provocare effetti disastrosi in ecosistemi residui presenti in paesaggi frammentati ([2]).
La mitigazione degli effetti della frammentazione su popolazioni e comunità può essere ottenuta con il mantenimento di una continuità fisico-territoriale ed ecologico-funzionale fra gli ambienti residui ([36], [4]). La connettività deve essere funzionale ad ogni specie, infatti in uno stesso paesaggio ogni specie può percepirla a differenti livelli. Anche l’aspetto temporale è importante: l’efficacia di un’area di connessione può variare a seconda del periodo dell’anno o delle fasi del ciclo vitale di una specie ([15]).
Le formazioni forestali del Mediterraneo
L’area del Mediterraneo è una regione biogeografica ben definita ([14]) ad elevata biodiversità ([17]). Essa infatti ospita circa 25 000 specie di piante mentre nell’Europa centrale e settentrionale, una regione quattro volte più grande, si possono trovare solo 6 000 specie tra angiosperme e felci ([65]). Il cinquanta per cento della flora mediterranea è endemico della regione e si è evoluto in un intervallo di tempo molto variabile e sotto diverse condizioni climatiche.
Le formazioni forestali rappresentano una componente importante della flora mediterranea ([65]). La distribuzione delle foreste nella regione Mediterranea è piuttosto irregolare: il 65% della superficie forestale si trova sulla costa settentrionale, mentre la restante superficie è quasi equamente divisa tra Africa settentrionale e vicino Medio-Oriente. La percentuale di copertura forestale in relazione alla superficie totale della zona è molto diversa tra sub-regioni del Mediterraneo: essa varia dal 20 al 30% nei Paesi del Nord del bacino, all’1-8% e 5-10% rispettivamente nel Sud e nei Paesi dell’Est ([65]). Si deve tuttavia sottolineare che le foreste di tipo Mediterraneo (estese per circa 81 milioni di ettari) sono ecosistemi piuttosto unici che costituiscono l’1.5% delle foreste del pianeta ([46]). Circa l’80% di queste foreste è concentrata nella regione mediterranea, il resto è diviso in piccole aree tra Australia, Sud Africa, California e Cile.
La vegetazione naturale della regione Mediterranea è strettamente legata alle caratteristiche tipiche del clima, ma dipende anche dal fattore altitudinale. La persistenza nei secoli di diverse forme di eccessivo sfruttamento da parte dell’uomo ha causato la notevole riduzione di buona parte dei tipi forestali climax della regione mediterranea ([56]). Le rimanenti foreste sono boschi alterati in modo più o meno intensivo da parte dell’uomo che spesso corrispondono a diversi stadi di successione regressiva della foresta originaria.
L’aumento progressivo delle attività agricole negli ultimi secoli ha portato ad una forte riduzione della superficie forestale. Attualmente, tessere residue di paesaggio forestale si ritrovano soprattutto nelle zone collinari. Fanno eccezione alcune zone in quota dove una copertura forestale continua è ancora presente con una struttura non derivata dall’intervento dell’uomo ([50]).
Sclerofille e foreste mesofile nel paesaggio Mediterraneo rappresentano l’unico esempio di habitat boschivo continuo contenente un’abbondante diversità specifica, animale e vegetale, esemplificata dal gran numero di specie arboree rispetto alle foreste nordiche ([65]).
Pratiche di agricoltura intensiva, così come lo sviluppo del turismo, incendi estivi, l’inquinamento dell’aria e l’urbanizzazione rappresentano una seria minaccia per molti boschi nell’Europa Mediterranea ([65]).
La trasformazione della vegetazione naturale in un complesso mosaico di patches tra la matrice coltivata che forma un sistema in “quasi-equilibrio”, è pure un grave problema per la regione Mediterranea. Ciò ha contribuito alla perdita di diversità specifica e variabilità genetica di specie forestali ([30]). Il recupero di paesaggi frammentati dovrebbe essere basato sul riconoscimento che “i diversi patches e l’uso del suolo in un paesaggio sono strettamente interconnessi ecologicamente e che la loro gestione deve essere integrata nell’intero paesaggio, piuttosto che essere relativa a segmenti di paesaggio isolato” ([29]). Questa esigenza è particolarmente evidente nel bacino del Mediterraneo, dove alcune regioni sono quasi completamente prive di vegetazione forestale o con frammenti boschivi completamente isolati la cui conservazione insieme alla gestione delle specie selvatiche è compromessa.
Un bioindicatore della qualità forestale
La distribuzione e le dimensioni dei frammenti di habitat idonei sono state considerate le variabili chiave che influenzano la comparsa ([49], [3], [27]), la persistenza nel territorio ([21], [3]), la densità di popolazione ([69], [40]), la dimensione dell’home range ([21], [60]), il successo riproduttivo ([47], [39]), le abitudini alimentari ([37]), la sopravvivenza ([40]), e la dispersione ([41]) di molte specie di uccelli. La dimensione della superficie boscata è un fattore chiave per spiegare il successo riproduttivo e la regolarità nella spaziatura tra i nidi ([48], [28], [55], [60]). Inoltre molte specie ornitiche sono influenzate dalle caratteristiche fisiografiche della foresta ([48], [54], [20], [52]). I cambiamenti nella struttura dell’habitat possono causare cambiamenti nella composizione delle comunità ornitiche e nell’abbondanza di molte specie ([70], [34]). La diversità e la ricchezza specifica, il numero di specie nidificanti in cavità degli alberi e il numero di specie interiori aumentano con l’età delle foreste, sottolineando l’importanza di ecosistemi forestali maturi ([33], [45], [24]). L’età delle foreste è positivamente correlata con il volume degli alberi, e a sua volta con la produttività dell’area boschiva, quindi il suo effetto sulle comunità ornitiche può essere molto forte ([31]).
Al livello di popolazione o di specie la sensibilità per la frammentazione degli habitat idonei e per il rapporto perimetro/area è stata registrata soprattutto nelle specie legate al bosco fitto ([71]) così come in specie stenoecie, dotate di scarsa vagilità, in specie sedentarie o in quelle con densità di popolazione naturalmente basse ([32]). Tra queste specie sensibili alcune possono essere scelte come indicatori e svolgere così un ruolo nella elaborazione di strategie di pianificazione per la conservazione delle foreste ([25]).
Queste specie, definite come target ([67]), possono riflettere lo stato di un sistema ecologico e fornire informazioni sugli effetti della frammentazione in diversi contesti geografici ([66]). Tali specie sono scelte per rappresentare un gran numero di specie ecologicamente affini (ruolo di indicatore). Inoltre, in questo senso, un buon indicatore dovrebbe essere relativamente diffuso nella zona di studio e valutabile facilmente per la sua abbondanza e il suo modello di distribuzione locale ([51]).
L’individuazione di indicatori ed il loro monitoraggio per verificarne l’efficacia sono passaggi essenziali nel settore della biologia della conservazione, per evitare che le ipotesi di pianificazione formulate non restino solo speculative e inutili ai fini del raggiungimento degli obiettivi prefissati ([61]). Come evidenziato da Dobson et al. ([15]) le specie candidate a svolgere una funzione target per attuare strategie di monitoraggio della connettività sono quelle con necessità di ampiezza dell’area core. Quando si lavora a scala di paesaggio o regionale, le specie idonee a tal fine possono essere, inoltre, quelle che necessitano del mantenimento di vaste aree per compiere il processo di dispersione o che siano presenti con basse densità (tra queste, i grandi carnivori e le specie di ambienti maturi e delle ultime fasi delle successioni).
In relazione alle esigenze ecologiche e all’ampiezza di nicchia potranno anche essere selezionate specie che, benché relativamente diffuse e abbondanti (quindi non rientranti nelle liste rosse), possono mostrare una vulnerabilità intrinseca alla frammentazione ambientale. La scelta di specie non appartenenti a specifiche categorie di minaccia può essere necessaria in contesti antropizzati (ad esempio, pianura padana, aree costiere, sistemi urbani e suburbani - [38]).
In tali contesti è, infatti, altamente improbabile la presenza di specie minacciate a scala regionale/nazionale che possono svolgere il ruolo di indicatori del processo, e quindi può risultare difficile, se non impossibile, definirne i pattern di distribuzione ed abbondanza sui quali lavorare per individuare ipotesi di pianificazione. Alcune specie, ancora relativamente diffuse, possono essere quindi selezionate al pari di quelle minacciate perché possono rivelarsi intrinsecamente sensibili al processo di frammentazione e svolgere un ruolo chiave nella funzionalità dei sistemi ecologici. In tal senso le specie target, così selezionate, possono essere assimilate a specie focali che mostrano una sensibilità a quei fattori (area, isolamento, qualità ambientale) individuati come le componenti del processo di frammentazione ([35]).
Le specie più promettenti che servono come indicatori delle condizioni ambientali sono quelle più facilmente contattabili e monitorate e le cui relazioni funzionali ai cambiamenti di habitat sono chiaramente comprensibili. Alcune specie sono buoni indicatori della qualità delle foreste perché sono specialiste e particolarmente sensibili ai cambiamenti di habitat. Il controllo della risposta della loro popolazione alla gestione permetterà di utilizzarle come indicatori. Altre specie, tuttavia, possono essere buoni indicatori perché le caratteristiche del loro habitat coprono le esigenze di molti altri animali e piante. Il loro valore è particolarmente grande per la pianificazione e analisi su vasta scala.
Diverse caratteristiche fanno dell’allocco (Strix aluco Linneo 1758) una specie interessante da studiare soprattutto sotto il punto di vista della dinamica di popolazione. E’ una specie completamente sedentaria, gli adulti, una volta stabilito il territorio, vi rimangono per il resto della loro vita, mentre i giovani si disperdono allontanandosi solo di poco dal territorio di nascita (22.5 km è la distanza di dispersione maggiore misurata per un giovane marcato in Inghilterra - [68]). L’allocco, è un rapace notturno di medie dimensioni appartenente alla famiglia degli Strigidi (Strigiformes). L’adulto arriva a misurare in altezza circa 38 cm, con un’apertura alare che si aggira intorno ai 99 cm ed un peso variabile dai 345 ai 600 g.
L’areale dell’allocco corrisponde alla regione Paleartica occidentale, e si estende fino alla parte sud- occidentale dell’Asia ([68]), arrivando in Europa centrale a popolare regioni sino ai 1600 m sul livello del mare ([10], [11], [43]).
Normalmente l’habitat dell’allocco è costituito da ambienti boscosi alternati a spazi aperti, aree rocciose con una copertura boschiva o arbustiva relativamente ampia, ma anche giardini e parchi se ci sono esemplari di vecchi alberi ([57], [63]). La specie evita le zone umide, le pianure prive di alberi e i territori caratterizzati da climi gelidi o aridi. L’habitat di elezione sono le formazioni di alto fusto, ma colonizza ugualmente i cedui composti e i cedui semplici, o riconvertiti, con densità proporzionalmente ridotte in base alla struttura del bosco. L’allocco, infatti, dipende dalla presenza di alberi usati come posatoi per cacciare e per nidificare ([43], [11]). Esso però può sopravvivere anche in ambienti frammentati costituiti da piccoli boschi circondati da paesaggi aperti con alberi sparsi, cosicché la matrice che circonda il bosco contenga numerosi posatoi ([28], [23]). Il modello di idoneità ambientale ([6]) mostra le aree di distribuzione potenziale della specie in Italia, che comprendono l’intero territorio nazionale con esclusione della Sardegna e della Puglia, regioni con habitat meno idonei per questa specie.
La nidificazione può avvenire nelle cavità degli alberi, ma anche sui dirupi o nelle costruzioni abbandonate. Presentano una forte fedeltà al sito di nidificazione che abbandonano solo in caso di deterioramento o di disturbo irreversibile. L’utilizzo di cassette-nido fornite nel territorio di nidificazione aiuta lo studio dell’incidenza e del successo riproduttivo ([68]). L’allocco è una specie con ampio repertorio canoro; il richiamo territoriale dell’adulto consente di effettuare un censimento acustico, ed il richiamo di richiesta del cibo dei pulcini permette di contare i giovani nati con facilità. Lo studio di Redpath ([59]), ad esempio, ha indicato che il 94% degli allocchi rispondevano al playback entro i primi 30 minuti e gli allocchi che hanno colonizzato piccoli frammenti tendevano a rispondere più velocemente e in modo più aggressivo. Prevale un sistema territoriale molto rigido e ciò aiuta nella pratica il lavoro di censimento che è estremamente rapida e standardizzabile.
L’allocco come indicatore di qualità forestale e frammentazione del paesaggio
La stabilità delle popolazioni di allocco aumenta da nord a sud nel suo areale, probabilmente a causa delle condizioni di clima più mite e della riduzione delle fluttuazioni dei piccoli mammiferi ([63]). È interessante notare che questi fattori stabilizzano anche il successo riproduttivo della specie nel bacino del Mediterraneo ([21], [58]).
E’ stato provato che la dipendenza del numero dei territori di allocco dalla superficie boschiva è strettamente lineare ([63]). La densità dei territori varia in maniera significativa rispetto al tipo di habitat, in particolare la quantità di area boschiva per territorio di un allocco è stata eccezionalmente stabile tra gli habitat. La densità dei territori risulta dunque correlata positivamente alla percentuale di boschi e negativamente alla percentuale di aree antropizzate, e non correlata con la percentuale di terreni agricoli e con la distanza dalle aree urbane ([57]), confermando questa specie come una delle più idonee nel monitoraggio della qualità forestale. Le dimensioni dell’home-range degli allocchi sono inoltre influenzate dalla perdita e dalla frammentazione dei boschi che influenzano la selezione dell’habitat, il comportamento territoriale, il successo riproduttivo e il turnover.
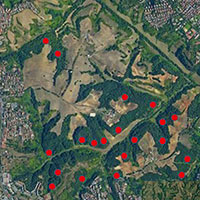
Dallo studio di Redpath ([60]) è emerso che l’allocco è presente in tutti i boschi continui di oltre 4 ettari e fino al 35% dei boschi inferiori ad un ettaro. In aree frammentate l’habitat boschivo incluso nell’home-range ha una superficie ridotta rispetto alle dimensioni totali dell’home-range, infatti gli esemplari che vivono in queste zone tendono a fare in modo di aumentare le dimensioni del loro territorio per comprendere un certo numero di questi frammenti boschivi ([60]). Gli home-range sono maggiori dove i boschi sono piccoli e isolati. Altri studi su allocchi in boschi continui hanno mostrato dimensioni del territorio comprese tra 12 e 24 ettari ([68], [28]), suggerendo che siano queste le misure di home-range tipiche per la specie. Anche se l’home-range minimo registrato in un bosco continuo è stato 9.2 ettari, allocchi in una zona aperta sono stati in grado di sopravvivere con appena 0.7 ettari di bosco nel loro home-range ([60]).
Il turnover all’interno dei territori, misurato come numero di anni in cui ogni territorio è stato occupato da un allocco (non necessariamente lo stesso individuo), è stato misurato da Redpath ([60]). Il turnover era più alto nei boschi più piccoli. Nei boschi inferiori ad un ettaro solo uno di otto territori era stato occupato per 3 anni interi, rispetto all’81% dei territori occupati nei boschi di dimensioni maggiori a 4 ettari. I cambiamenti nella dimensione della popolazione in relazione alla frammentazione degli habitat sono correlati linearmente alla variazione percentuale di habitat idonei nel paesaggio.
Attraverso la correlazione tra copertura forestale e la distribuzione della specie o la densità di popolazione si possono ottenere informazioni concernenti l’idoneità di habitat quando vengono confrontate differenti categorie di bosco ([1], [44]).
Salvati & Ranazzi ([62]) hanno effettuato uno studio in tal senso determinando la dipendenza della densità di popolazione e della dimensione del territorio dalla copertura forestale, ed hanno calcolato la quantità di area boschiva nel territorio di un allocco in quattro tipi di bosco in Italia centrale lungo un gradiente altitudinale, a partire da querce sclerofille lungo la costa a faggete di montagna nel Lazio e in Abruzzo.
Tale studio appare illuminante al fine del monitoraggio della frammentazione e qualità forestale in quanto effettuato in svariate condizioni ambientali: l’altitudine delle foreste prese in esame varia da 10 m fino a 1500 m s.l.m. Le dimensioni della maggior parte delle foreste variano tra 100 e 500 ettari, con solo poche foreste più grandi di 2000 ettari. Tutti i tipi vegetazionali dominanti sono stati valutati come pure il differente governo del bosco, individuando differenze importanti nella densità della specie tra formazioni di alto fusto e cedui.
Salvati & Ranazzi ([62]) hanno anche dimostrato che vi è una correlazione tra densità di popolazione e tipo di copertura forestale. La più bassa densità di popolazione è stata registrata in media nei boschi urbani e in quelli gestiti a ceduo semplice, e la più alta in boschi di querce sclerofille non gestite. Gli autori hanno usato il metodo della distanza dal territorio più vicino ([57]) per stimare la densità di popolazione. La spaziatura è stata valutata utilizzando il centro di territori occupati. Questo metodo è stato scelto per ottenere stime comparabili di densità e per correlarle quantitativamente con la copertura forestale.
Dalla regressione lineare risultante dai loro studi si ottiene, inoltre, che la dimensione minima dell’home-range è di 7.2 ettari per i boschi di querce sclerofille, 10 ettari per i boschi di querce mesofile, 12.7 ettari per il bosco misto urbano, e di 18.1 ettari per i boschi di faggio di montagna.
In un altro studio, Salvati et al. ([63]) hanno ottenuto che la superficie delle aree boschive presenti nel territorio di un allocco è positivamente correlata con l’altitudine alla quale si trovano le foreste.
L’area boschiva è stata utilizzata come descrittore della quantità di habitat adatto all’allocco per la nidificazione. La densità di popolazione dell’allocco non risulta però correlata all’altitudine ([63]).
La più alta densità di popolazione registrata nei boschi di querce sclerofille riflette le loro caratteristiche peculiari, tra cui la produttività elevata di prede, ridotta frammentazione del bosco, la diversità della vegetazione alta, bassa pressione antropica, e un numero eccezionalmente elevato di siti di nidificazione dovuto alla presenza di molti alberi monumentali ([52], [5], [63]), indicando elementi di elevata qualità e bassa frammentazione di tali formazioni. Diversi tipi di paesaggio perciò possono influenzare la probabilità di colonizzazione di un frammento di habitat ([44]). Le differenze di densità di popolazione degli allocchi suggeriscono che la qualità delle foreste incide sulla densità e regola la difesa territoriale ([21], [60]).
Conclusioni
I rapaci forestali mostrano un’elevata sensibilità alla frammentazione del bosco ([7], [53], [52]), e sono preziosi indicatori della qualità degli habitat ([7]). I cambiamenti nella densità di popolazione a livello di habitat ci portano ad affermare che l’allocco può essere utilizzato come indicatore per valutare le differenze di qualità delle foreste. Inoltre l’allocco risente degli effetti della frammentazione del territorio e pertanto può essere utilizzato per monitorare il grado di diversità ambientale e predisporre misure di gestione al fine di aumentare il grado di connettività del paesaggio.
La struttura, la composizione specifica ed il governo del bosco sono importanti predittori delle caratteristiche delle comunità ornitiche, non ultimo l’allocco ([63]). Perciò valutare l’associazione tra rapaci e i loro habitat può fornire strumenti utili per la conservazione e la gestione degli habitat forestali. I risultati presentati suggeriscono inoltre come i bio-indicatori animali possano fornire utili indicazioni agli interventi di miglioramento della funzionalità dell’ecosistema bosco, e più in generale alla pianificazione forestale. Mediante monitoraggi non invasivi e particolarmente semplici per quanto attiene allo sforzo di campagna, la diversa distribuzione e densità dell’allocco nelle formazioni forestali studiate possono suggerire le aree di intervento volte ad un aumento della complessità strutturale e alla protezione della biodiversità.
References
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar