Bark necrosis by Brenneria nigrifluens and other bacteria on walnut plantations in Piedmont: analysis of the disease evolution in the field and isolate characterization by rep-PCR
Forest@ - Journal of Silviculture and Forest Ecology, Volume 11, Pages 180-188 (2014)
doi: https://doi.org/10.3832/efor1335-011
Published: Nov 20, 2014 - Copyright © 2014 SISEF
Research Articles
Abstract
Owing to its increasing incidence, a study was performed on walnut bacterial bark canker by Brenneria nigrifluens, a disease native to California but spreading over Europe since about twenty years. B. nigrifluens may compromise wood quality and, in some cases, impair plant survival due to extensive cankers and bark necroses. Bacterial isolates obtained from bark tissue fragments, typed by rep-PCR analysis after multiplication on proper selective growing media, confirmed the diagnosis of the causal agent, despite the presence of other bacterial species. B. nigrifluens was detected in 28% of common walnut arboricultural stands located in Piedmont plains and hills, especially those located in the Vercelli province and in some areas of the Alessandria province. Based on the results of the cluster analysis carried out on PCR amplicons, none of the other bacterial isolates showed any genotypic similarity with the related B. rubrifaciens, the agent of the deep bark canker of walnut, which has not been detected in Europe yet. The application of the three rep-PCR variants, including BOX-PCR applied for the first time to B. nigrifluens, gave similar results, but with different cluster structures. In two pilot plantations, trees already presenting necroses did not necessarily develop new necroses or enlarge the pre-existing cankers in the following years. The disease apparently does not spread according to a climate factor, whereas it may be affected by plant genotype that possibly promotes the transition of B. nigrifluens, probably already present in tissues in an asymptomatic endophytic phase, to the pathogenic phase.
Keywords
English Walnut, Brenneria nigrifluens, Shallow Bark Canker, Rep-PCR, Wood Arboriculture
Introduzione
In occasione di un monitoraggio fitopatologico svolto per quattro anni consecutivi su numerose piantagioni di arboricoltura da legno costituite con latifoglie di pregio, Juglans regia L. (noce europeo) e Prunus avium L. (ciliegio comune) in particolare, sono state osservate necrosi corticali su numerose piante di noce che, per aspetto, potevano essere del tutto assimilate a quelle descritte in letteratura come indotte dal batterio Brenneria nigrifluens (Wilson et al.) Hauben et al. Esse all’inizio consistono in piccole lesioni necrotiche essudanti un caratteristico fluido brunastro, localizzate possibilmente dalla base fino alla sommità del tronco, spesso limitrofe a lesioni cancerose più estese e già disseccate (Fig. 1). I tessuti necrotizzati tendono poi a interessare l’intera circonferenza del tronco per arrivare a uno stadio finale in cui esso risulta ingrossato per le estese reazioni cicatriziali che comunque non riescono a circoscrivere il cancro stesso (Fig. 2). Con tutta evidenza, il legno interessato dall’alterazione risulta inutilizzabile al momento del taglio finale e i cancri più estesi mettono a repentaglio la stabilità meccanica della pianta, la quale è esposta a rotture da vento o da neve, nonché alla colonizzazione da parte di funghi agenti di carie. Il patogeno non è nuovo in Italia: descritto per la prima volta su noce nero americano in California ([18]) e segnalato a metà degli anni ’90 in Spagna su noce europeo ([5]), fu poi osservato nel nostro Paese proprio in Piemonte ([11]) e quasi contemporaneamente in Veneto ([14]), quindi in Lazio ([15]) e in Campania ([1]). Comparso poco più tardi in Francia ([8]) e da ultimo in Serbia ([12]), le segnalazioni del batterio sono andate intensificandosi nel nostro Paese soprattutto nell’ultimo lustro. Conosciuto in letteratura anglosassone come agente di cancro corticale superficiale (Shallow Bark Canker, SBC) per contrapporlo a Brenneria rubrifaciens (Wilson et al.) Hauben et al., agente di cancro corticale profondo (Deep Bark Canker, DBC) allo stato attuale non ancora diffuso in Europa se non in un distretto spagnolo ([4]), B. nigrifluens rappresenta una minaccia potenziale per la conduzione degli impianti di noce misti e soprattutto in purezza, viste anche le scarse conoscenze sulle condizioni predisponenti alla sindrome e più in generale sulla sua epidemiologia in Italia.
Fig. 1 - Emissione di essudato brunastro da necrosi corticale su noce europeo causata da Brenneria nigrifluens.
Nel corso del monitoraggio di cui sopra è stata dunque assegnata una crescente attenzione al rilievo puntuale di sintomi ascrivibili a batteriosi da Brenneria, in particolare in due piantagioni pure di noce di una medesima località in cui essi apparivano oltremodo frequenti, in vista di trarre elementi di previsione per gli anni a venire. A ciò si è accompagnato un consistente campionamento di tessuti corticali sintomatici per l’isolamento delle entità batteriche da identificare.
Materiali e metodi
Rilievi in campo e isolamenti in laboratorio
Piante con sintomi di infezioni batteriche sono state registrate, ove presenti, in 25 piantagioni di noce europeo in purezza o misto con altre latifoglie nobili (per lo più Prunus avium L.) ubicate in vari distretti piemontesi a varie altitudini (Tab. 1). Sono stati condotti rilievi ad hoc sulla totalità delle piante, negli anni 2009, 2010 e 2011, in due piantagioni di noce in purezza di Borgo San Martino (AL), di seguito denominati come “impianto A” (516 piante) e “impianto B” (254 piante), nelle quali le necrosi corticali erano particolarmente diffuse, avendo cura di distinguere piante con vecchie necrosi ormai seccate e/o cicatrizzate, piante con necrosi vecchie e nuove dell’anno e infine piante interessate soltanto da necrosi nuove. Sono stati prelevati tasselli corticali mediante scalpelli a fustella (3 cm di diametro, in numero variabile per pianta secondo il numero e la disposizione delle necrosi) da piante sintomatiche, in modo da arrivare fino ai primi strati legnosi, zona fino alla quale si spingono gli imbrunimenti connessi alla sindrome e da cui è più probabile l’isolamento di batteri non saprofiti. I prelievi sono stati sempre praticati in corrispondenza di lesioni ancora limitate, di fresca formazione, da cui fosse evidente la secrezione di fluidi brunastri.
Tab. 1 - Località e composizione specifica delle piantagioni di arboricoltura da legno piemontesi monitorate per la batteriosi corticale causata da B. nigrifluens. (§): pianura; (§§): fondovalle; (‡): versante; (‡‡): collina.
| Provincia | Località | Annod’impianto | Altit. (m) | Specie | Sesto d’impianto (m) |
|---|---|---|---|---|---|
| Alessandria | Casalnoceto§ | 1994 | 160 | P. avium, J. regia | 6.5 × 2.0 |
| Pozzolo Formigaro§ | 1996 | 160 | P. avium, J. regia | 8.0 × 8.0 | |
| Montaldeo§§ | 1994 | 230 | P. avium, J. regia | 8.0 × 4.0 | |
| Coniolo‡ | 1994 | 110 | P. avium, J. regia | 6.0 × 6.0 | |
| Fubine‡ | 1994 | 100 | P. avium, J. regia, F. excelsior | 8.0 × 8.0 | |
| Serralunga di Crea‡ | 1996 | 250 | P. avium, J. regia | 6.0 × 6.0 | |
| Sezzadio§ | 1995 | 110 | P. avium, J. regia | 4.0 × 14.0 | |
| Sezzadio§ | 1995 | 110 | P. avium, J. regia e accessorie | 4.0 × 14.0 | |
| Borgo S. Martino (2)§ | 1996 | 103 | J. regia puro | 7.0 × 7.0 | |
| Asti | Montiglio Monferrato‡ | 1997 | 240 | P. avium, J. regia, F. excelsior | 4.5 × 4.5 |
| Cuneo | Montanera§ | 1994 | 400 | P. avium, J. regia | 5.0 × 5.0 |
| Dogliani‡ | 1996 | 400 | P. avium, J. regia | 6.0 × 6.0 | |
| Ceva§ | 1994 | 500 | P. avium, J. regia | 3.0 × 6.0 | |
| Bergolo‡ | 1996 | 500 | P. avium, J. regia | 3.0 × 4.0 | |
| Benevagenna§ | 1995 | 347 | J. regia e accessorie | 5.0 × 4.0 | |
| Torino | Chivasso§ | 1997 | 180 | J. regia | 8.0 × 8.0 |
| Riva di Chieri§ | 1996 | 250 | J. regia | 6.0 × 6.0 | |
| Pinerolo§ | 1996 | 360 | J. regia | 8.0 × 8.0 | |
| Venaria§ | 1994 | 310 | P. avium, J. regia | vari | |
| Novara, Vercelli | Cigliano (VC)§ | 1994 | 210 | J. regia | 7.0 × 5.5 |
| Borgo d’Ale (VC)§ | 1996 | 250 | J.regia | 3.0 × 3.0 | |
| Alice Castello (VC)§ | 1996 | 250 | J. regia | 7.0 × 8.0 | |
| Novara (NO)§ | 1995 | 130 | P. avium, J. regia e altre | 3.0 × 4.0 | |
| Novara (NO)§ | 1995 | 130 | P. avium, J. regia e altre | 3.0 × 4.0 | |
| Cigliano (VC)§ | 1995 | 220 | J. regia | 8.0 × 8.0 |
In laboratorio sono state isolate le entità batteriche sterilizzando in superficie ciascun tassello, immergendolo in etanolo al 70% e passandolo a becco Bunsen, con successiva asportazione in sterilità da ciascuno di essi uno o più frammenti di circa 5-6 mm3 in corrispondenza soprattutto del margine di passaggio dal tessuto imbrunito e/o alterato a quello sano, ma in diversi casi anche da quest’ultimo. Ogni frammento è stato poi sminuzzato con pestello sterilizzato in 2 ml di acqua sterile e la sospensione risultante distribuita con ansa batteriologica in capsula Petri sterile contenente Miller-Schroth agar (MS agar - [9]), substrato specifico selettivo per la crescita di colonie di batteri anaerobi facoltativi assimilabili al gruppo Erwinia (genere cui afferiva in precedenza anche B. nigrifluens), le quali vi assumono una caratteristica colorazione arancione virante poi al verde in seguito a invecchiamento.
Le capsule Petri così inoculate sono state poste a incubare capovolte in termostato per 2-3 giorni a 28 °C, temperatura ritenuta favorevole alla crescita delle colonie di diverse entità del gruppo Erwinia. Gli isolati, le cui colonie presentavano i caratteri morfologici tipici del gruppo Erwinia su tale substrato, sono state trasferiti su nuove capsule Petri contenenti Nutrient Agar (NA - Oxoid®, pH 7.4) e mantenuti in purezza.
Fingerprinting di isolati batterici
Per l’identificazione degli isolati ottenuti dai vari campionamenti è stata adottata la metodica di reazione a catena della polimerasi nota come rep-PCR ([16], [17], [13]), principalmente nella variante REP-PCR. In alcune analisi, tuttavia, si è fatto ricorso anche alle varianti ERIC-PCR e BOX-PCR, sottoponendo uno stesso insieme di isolati batterici separatamente alle tre varianti di analisi al fine di poterne confrontare analogie e differenze. Si ricorda qui che la metodica rep-PCR sfrutta la naturale presenza di sequenze ripetute e altamente conservate nel DNA genomico della maggior parte dei batteri gram-negativi e di molti gram-positivi. Tali sequenze intergeniche, ricorrenti in copie multiple e ubicate in posizioni distinte e precise del genoma, sono riconducibili a tre gruppi, denominati come Repetitive Extragenic Palindromic (REP) Sequence, Enterobacterial Repetitive Intergenic Consensus (ERIC) Sequence e BOX Element.
Ovviamente, l’amplificazione molecolare basata su ciascuna delle predette sequenze ha comportato il ricorso a primer differenti, le cui sequenze sono in dettaglio:
- REP 1R (5’-IIIICgICgICATCIggC-3’) e REP 2I (5’-ICgICTTATCIggCCTAC-3’) per la REP-PCR;
- ERIC 1R (5’-ATgTAAgCTCCTggggATTCAC-3’) ed ERIC 2 (5’-AAgTAAgTgACT-ggggTgAgCg-3’) per la ERIC-PCR;
- BOX A1R (5’-CTACggCAAggCgACgCTgACg-3’) per la BOX-PCR.
È stato applicato, con alcune lievi modifiche, il protocollo proposto da Rademaker & DeBruijn ([13]), secondo il quale è possibile eseguire l’amplificazione sulle sospensioni batteriche senza la preventiva estrazione del DNA genomico. È stata saggiata l’amplificazione da colture cellulari axeniche cresciute su NA di circa una settimana.
Una soluzione tampone, Gitschier Buffer 5×, è stata preparata con 16.6 ml di (NH4)2SO4 1 M, 67 ml di Tris-HCl 1 M (pH 8.8), 6.7 ml di MgCl2 1 M, 1.3 ml di EDTA 0.5 M (pH 8.8) diluito 1:100 e 106 ml di acqua sterile, distribuita in aliquote da 1 ml e conservata a -20 °C. Il campione da sottoporre a PCR è stata preparato, per ciascun isolato batterico, a partire da 1 µl di sospensione cellulare ottenuta sciogliendo 10 mg di colonia in 5 ml di acqua sterile. A detta aliquota è stata aggiunta una miscela (master mix) composta da 5 µl di Gitschier Buffer 5×, 2.5 µl di DMSO 100%, 12.85 µl di acqua sterile, 1.25 µl di una soluzione di dNTPs 25 mM (ATP:TTP:GTP:CTP = 1:1:1:1), 0.4 µl di una soluzione di Taq DNA Polymerase (5 U/l), 1 µl di soluzione di ciascun primer (0.3 µg/µl). Tranne l’acqua sterile, conservata a temperatura ambiente, gli altri componenti della miscela erano stati conservati a -20 °C. Ciascuna provetta conteneva pertanto 25 µl di materiale da sottoporre a PCR. Il materiale è stato introdotto in termociclatore (mod. 9800 Fast, Applied Biosystems®) ed è stato sottoposto a 35 cicli termici, ciascuno dei quali dato da 1’ a 94 °C, 1’ a 40 °C e 8’ a 65 °C, preceduti da un periodo di incubazione di 7’ a 95 °C e seguiti da un’estensione di 16’ a 65 °C. È quindi subentrata una temperatura di conservazione a 4 °C. Gli ampliconi sono stati sottoposti a elettroforesi in gel di agarosio all’1.5%, cui sono stati aggiunti 2 µl di bromuro di etidio per la visualizzazione dei profili elettroforetici sotto raggi UV. La corsa elettroforetica è stata impostata a 60 mV di potenziale per 45 minuti. I profili così ottenuti sono stati evidenziati sotto raggi UV in un trans-illuminatore (mod. Gel Doc™ XR 170-8171, Biorad®) e le immagini immediatamente registrate su supporto informatico.
Le impronte elettroforetiche sono state comparate registrando le bande corrispondenti ai frammenti di DNA di vari pesi molecolari, assegnando il valore 1 laddove presenti e il valore 0 laddove assenti. Le matrici binarie così ottenute sono state sottoposte ad analisi dei cluster basata sul coefficiente di Dice ([2]), facendo ricorso al software Statistica v. 8 (Statsoft Inc., Tulsa OK, USA).
Sono stati messi a confronto vari gruppi di isolati. Per la rappresentatività, vengono qui presentati due di tali gruppi (Tab. 2).
Tab. 2 - Due gruppi esemplificativi di isolati batterici sottoposti ad analisi elettroforetica mediante rep-PCR. (*): Isolati forniti e certificati dal Deutsche Sammlung von Mikroorganismen und Zellkulturen (Braunschweig).
| gruppo A(REP-PCR) | gruppo B(REP-PCR, ERIC-PCR e BOX-PCR) | ||
|---|---|---|---|
| numero di riferimentonel profilo elettroforetico | località o ceppo certificato | numero di riferimentonel profilo elettroforetico | località o ceppo certificato |
| I | Borgo San Martino (AL) | I’ | Borgo San Martino (AL) |
| II | II’ | ||
| III | Sezzadio (AL) | III’ | Sezzadio (AL) |
| IV | IV’ | Montanera (CN) | |
| V | V’ | Pozzolo Formigaro (AL) | |
| VI | VI’ | ||
| VII | Alice Castello (VC) | VII’ | Montanera (CN) |
| VIII | VIII’ | ||
| IX | Cigliano (VC) | IX’ | Pozzolo Formigaro (AL) |
| X | Brenneria nigrifluens* | X’ | Montaldeo (AL) |
| XI | Brenneria salicis* | XI’ | Brenneria nigrifluens* |
| XII | Pantoea agglomerans* | XII’ | Brenneria rubrifaciens* |
Risultati
Rilievi in campo
Sul totale delle 25 piantagioni monitorate con presenza di noce europeo, 7 (28%) sono risultate affette dalla sindrome batterica corticale, con incidenza molto variabile (dal 1% fino al 22% circa delle piante presenti), con la sola eccezione degli impianti-studio di Borgo San Martino dove si raggiungevano valori ben maggiori.
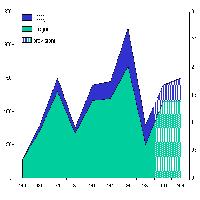
In questi ultimi, nel 2010 il decorso delle manifestazioni necrotiche aveva ricalcato quello del 2009, coprendo una frazione di stagione vegetativa che va dalla mezza estate alla fine di settembre. Le nuove necrosi, con essudato bruno fresco, erano tuttavia state osservate in misura assai contenuta rispetto a quella dell’anno precedente (Tab. 3). Mentre nel 2009 le nuove necrosi avevano interessato il 17.8% e l’11% del totale delle piante presenti rispettivamente nell’impianto A e in quello B, nel 2010 esse erano comparse soltanto su poco oltre il 3% in ambedue gli impianti, portando gli individui interessati da segni di necrosi, freschi o pregressi, al 35% e 30% circa. Gli individui recanti segni di vecchie necrosi che avessero sviluppato nuove necrosi erano una percentuale esigua sia nell’impianto A che nel B (15.3% e 14.9%, non in tabella). Per quanto concerne la distribuzione delle necrosi, l’insorgenza di quelle nuove dell’anno non aveva modificato la sostanziale distribuzione casuale nell’impianto B, mentre nell’impianto A si osservava un addensamento delle necrosi nelle porzioni marginali dello stesso; in effetti, nessuna necrosi fresca del 2010 era stata osservata nella zona centrale del campo.
Tab. 3 - Distribuzione delle necrosi corticali da B. nigrifluens nei due impianti-studio di noce di Borgo San Martino (AL).
| Impianto | Anno di rilievo | 2009 | 2010 | 2011 |
|---|---|---|---|---|
| impianto A (516 pp. iniziali) |
piante con necrosi (%) | 31.6 | 34.7 | 55.4 |
| piante con necrosi dell’anno (%) | 17.8 | 3.1 | 23.1 | |
| piante abbattute (%) | 0.0 | 0.0 | 3.5 | |
| impianto B (254 pp. iniziali) |
piante con necrosi (%) | 26.8 | 29.6 | 34.9 |
| piante con necrosi dell’anno (%) | 11.0 | 3.2 | 11.8 | |
| piante abbattute (%) | 0.0 | 0.4 | 9.5 |
Nel corso dell’ultima annata vegetativa analizzata (2011), l’incidenza della batteriosi aveva fatto registrare una notevole accelerazione, con oltre il 23% di nuove necrosi nell’impianto A e quasi il 12% nel B, a fronte di poco più del 3% del 2010. Il totale delle piante con sintomi si era quindi attestato ad oltre la metà (55% circa) di quelle presenti nell’impianto A e a quasi il 35% nel B, comunque senza ripercussioni apparenti, almeno alla stato attuale, sulla produttività complessiva data la contenuta estensione delle necrosi stesse. Nell’impianto A, la comparsa dei sintomi si era estesa anche alla porzione centrale dello stesso, in contrapposizione a quanto osservato negli anni precedenti.
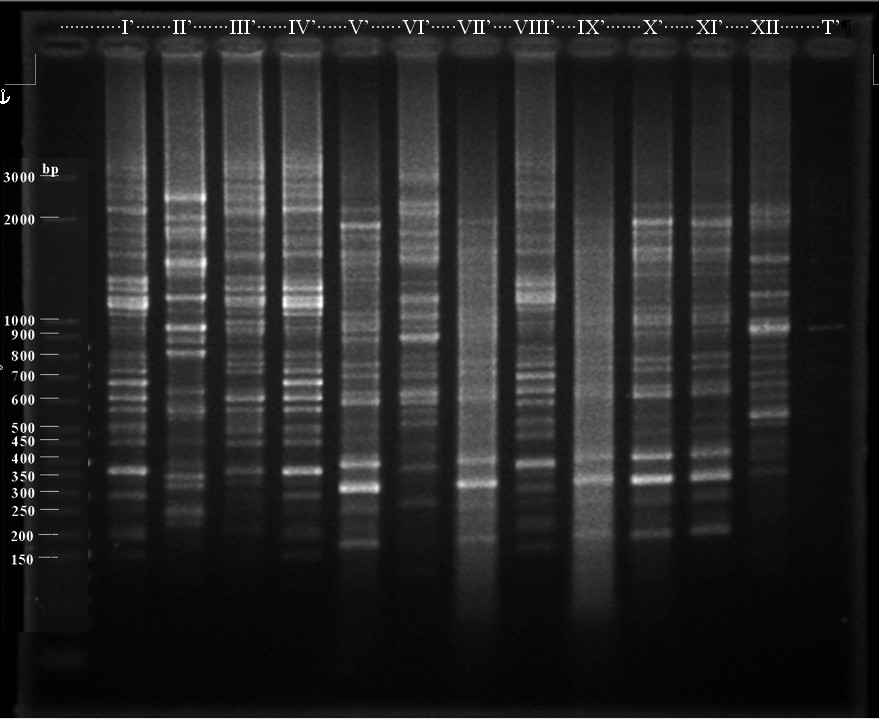
Per tutti i profili elettroforetici ottenuti da rep-PCR, le bande componenti sono risultate comprese fra 150 e 3000 bp (Fig. 3 relativa alla BOX-PCR a titolo esemplificativo).
Fig. 3 - Fingerprint in gel di agarosio (1.5%) di amplificati di DNA genomico di isolati batterici provenienti da imbrunimenti corticali su noce europeo, ottenuti secondo tecnica BOX-PCR. (I-X: isolati da imbrunimenti corticali su noce - I’ e II’: da Borgo San Martino, III’: da Sezzadio, IV’ e VII’ e VIII’: da Montanera, V’ e VI’ e IX’: da Pozzolo, X’: da Montaldeo; XI’: Brenneria nigrifluens DSMZ 30175; XII’: B.rubrifaciens DSMZ 4483; T: testimone amplificato di master mix e acqua sterile).
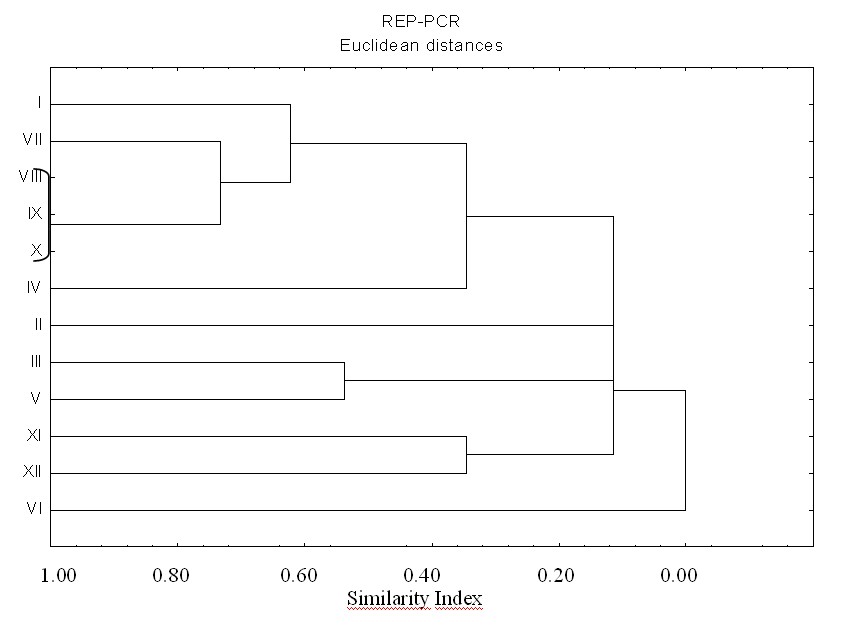
Per quanto concerne la REP-PCR, i risultati dell’analisi per cluster hanno evidenziato una perfetta identità degli isolati VIII, IX e X, ossia di quelli di Alice Castello e Cigliano con il ceppo certificato di B. nigrifluens (Fig. 4). Anche l’isolato VII di Alice Castello aveva una differenza ridotta da B. nigrifluens (similarity index pari a circa 0.72), mentre l’isolato I di Borgo San Martino si attestava su un valore di SI di 0.62 con B. nigrifluens. Dei restanti isolati, il VI di Sezzadio e gli XI (B. salicis) e XII (Pantoea agglomerans) sono risultati i più dissimili dal patogeno di interesse.
Fig. 4 - Dendrogramma ottenuto dall’analisi dei cluster di impronte elettroforetiche ottenute mediante REP-PCR di isolati batterici estratti da noce europeo. (I-IX: isolati da imbrunimenti corticali su noce - I e II: da Borgo San Martino, III-VI: da Sezzadio, VII e VIII: da Alice Castello, IX: da Cigliano; X: Brenneria nigrifluens DSMZ 30175; XI: B. salicis DSMZ 30166; XII: Pantoea agglomerans DSMZ 4609).
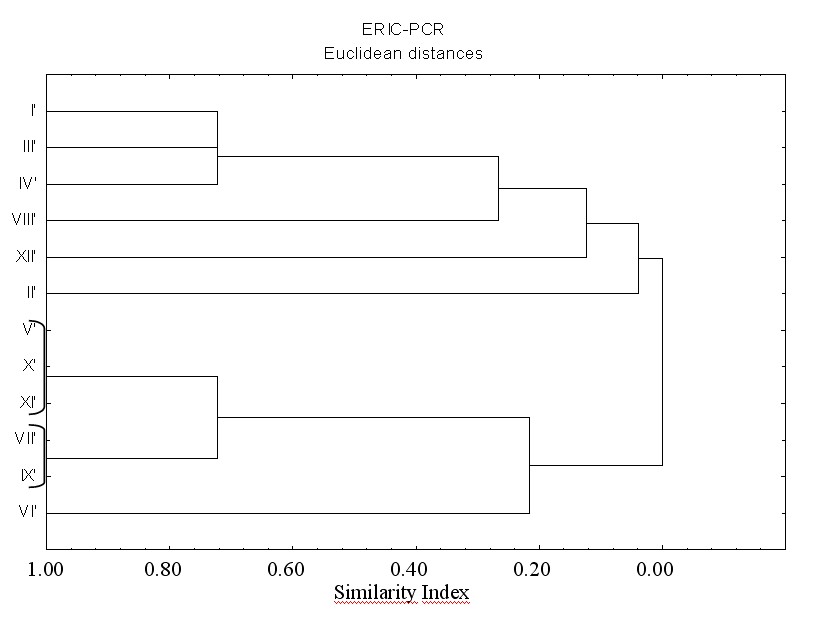
Nella ERIC-PCR (Fig. 5), gli isolati V’ (da Pozzolo Formigaro) e X’ (da Montaldeo) sono risultati identici a B. nigrifluens (XI’), mentre gli isolati VII’ e IX’ (rispettivamente da Montanera e P. Formigaro) sono risultati anch’essi identici e con un SI di 0.72 con B. nigrifluens; si sono discostati l’altro isolato VI’ da P. Formigaro (SI circa 0.22) e in misura ancora maggiore gli isolati I’, II’, III’, IV’, VIII’ e XII’, i quali sembravano costituire un gruppo del tutto differenziato. B. rubrufaciens (XII’) si annovera fra questi (fra cui gli isolati di Borgo San Martino I’ e II’, assai distanti nel cluster), ma nessuno degli isolati menzionati poteva essere assimilato a tale specie.
Fig. 5 - Dendrogramma ottenuto dall’analisi dei cluster di impronte elettroforetiche ottenute mediante ERIC-PCR di isolati batterici estratti da noce europeo.(I-X: isolati da imbrunimenti corticali su noce - I’ e II’: da Borgo San Martino, III’: da Sezzadio, IV’ e VII’ e VIII’: da Montanera, V’ e VI’ e IX’: da Pozzolo, X’: da Montaldeo; XI’: Brenneria nigrifluens DSMZ 30175; XII’: B.rubrifaciens DSMZ 4483).
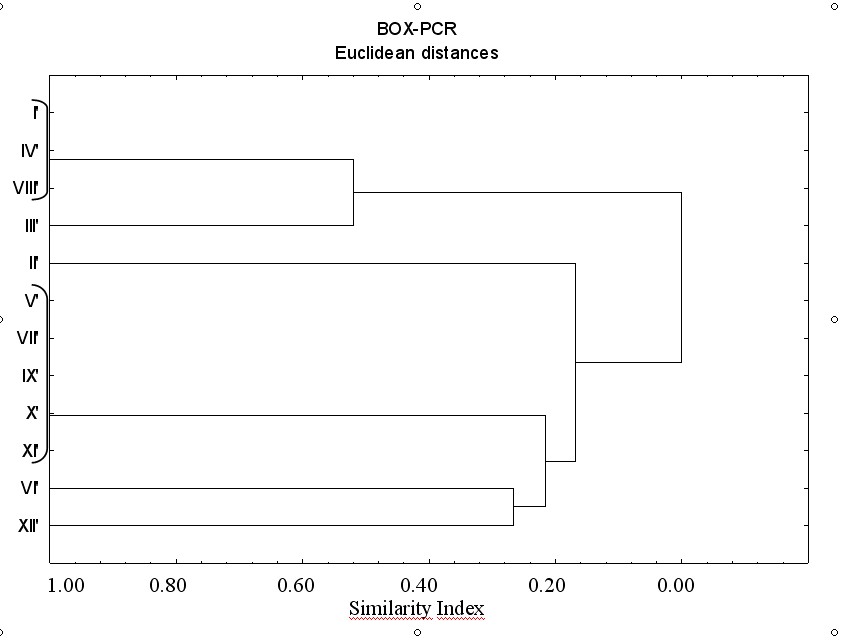
Nella BOX-PCR (Fig. 6), gli stessi isolati si sono distribuiti secondo cluster abbastanza differenti da quelli della ERIC-PCR. Oltre agli isolati V’ e X’, anche il VII’ e il IX’ sono risultati identici a B. nigrifluens (XI’). B. rubrifaciens era piuttosto distante dal precedente cluster (SI circa 0.26) così come, in misura ancora maggiore, i restanti isolati.
Fig. 6 - Dendrogramma ottenuto dall’analisi dei cluster di impronte elettroforetiche ottenute mediante BOX-PCR di isolati batterici estratti da noce europeo.(I-X: isolati da imbrunimenti corticali su noce - I’ e II’: da Borgo San Martino, III’: da Sezzadio, IV’ e VII’ e VIII’: da Montanera, V’ e VI’ e IX’: da Pozzolo, X’: da Montaldeo; XI’: Brenneria nigrifluens DSMZ 30175; XII’: B.rubrifaciens DSMZ 4483).
Discussione
Il fingerprinting molecolare attraverso rep-PCR con fini di identificazione di Brenneria è già stato impiegato con successo sia nella variante REP-PCR ([10]) sia nella variante ERIC-PCR ([6]); per quanto ci risulta, la variante BOX-PCR è stata da noi impiegata per la prima volta su questi patogeni con esiti analoghi a quelli delle altre due. Diversi altri metodi di caratterizzazione molecolare sono comunque riportati in letteratura per l’identificazione o il rilevamento di Brenneria da tessuti sintomatici, facenti capo a protocolli sia di PCR convenzionale che di real-time PCR ([7]).
I dendrogrammi relativi alle impronte elettroforetiche di ERIC-PCR e BOX-PCR suggeriscono in primo luogo che B. rubrifaciens, agente di DBC, non è stata riscontrata nelle piantagioni piemontesi indagate; in seconda istanza, che nessuna delle entità batteriche isolate con B. nigrifluens gli è geneticamente affine. Questa apparente assenza, che andrebbe comunque verificata a distanza di alcuni anni sulla base di quanto asserito da González et al. ([4]), potrebbe essere spiegata con un clima troppo rigido per B. rubrifaciens il quale, nello stesso areale di prima segnalazione, la California, è più incidente nei distretti centrali che non nelle più fresche zone costiere ([3]).
I confronti dei profili elettroforetici degli isolati raccolti nelle piantagioni con quello di B. nigrifluens suggeriscono che l’agente di SBC è diffuso in Piemonte, sebbene non desti ad oggi particolari preoccupazioni epidemiologiche. Assenti dagli impianti del Torinese e da larga parte di quelli del Cuneese (ma con l’importante eccezione di Montanera), i sintomi di B. nigrifluens sono ben presenti nelle piantagioni indagate del Vercellese e di larghi distretti dell’Alessandrino. Dalla nostra indagine è emerso che gli individui già colpiti non necessariamente sviluppano nuove necrosi nelle annate seguenti né i cancri preesistenti si estendono; pertanto, il danno sembra riguardare più la qualità del legname che la sopravvivenza delle piante stesse, con importanti ripercussioni sull’economia di un’attività sostenuta in prevalenza da sovvenzioni pubbliche. L’incidenza elevata della sindrome nei due impianti di Borgo San Martino, invero incongrua rispetto agli altri noceti oggetto di studio della presente indagine, porterebbe ad escludere un ruolo della componente climatica quale fattore scatenante della batteriosi, mentre prende corpo la possibilità che detta affezione possa essere legata a caratteri genetici del materiale di impianto che possano favorire il passaggio del batterio, probabilmente già presente nei tessuti in forma endofitica asintomatica, alla fase patogenetica. Per potere suffragare questa ipotesi sarebbe necessario disporre della composizione genetica della totalità dei noceti, utile a definire le interazioni fra ospite e patogeno. Del resto, i risultati delle analisi di rep-PCR non offrono la certezza che nello stesso campo di Borgo San Martino B. nigrifluens sia presente, dunque le necrosi riscontrate possono avere altra eziologia non necessariamente biotica.
La possibilità di B. nigrifluens come componente abituale della microflora infeudata nei tessuti cribro-vascolari è suggerita anche da Morone et al. ([11]) e Moretti et al. ([10]), ma che le sole condizioni di stress siano sufficienti a innescarne la patogenicità risulta non corroborato dai dati qui presentati.
Ringraziamenti
Le sperimentazioni sono state condotte nell’ambito del Progetto “Arbo.San - Situazione sanitaria degli impianti di arboricoltura da legno in Piemonte: connessioni con le condizioni ecologiche e con i caratteri della produzione legnosa”, finanziato su fondi della Regione Piemonte.
References
Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
Online | Google Scholar