How much different are conifer forests? Comparison of Lepidoptera community in silver fir and black pine stands in Calabria (southern Italy)
Forest@ - Journal of Silviculture and Forest Ecology, Volume 14, Pages 49-59 (2017)
doi: https://doi.org/10.3832/efor2241-013
Published: Feb 27, 2017 - Copyright © 2017 SISEF
Research Articles
Guest Editors: ALForLab Project (PON03PE_00024_1 - PON R&C- PAC 2007-2013)
« Public-private lab for the application of innovative technologies with high environmental sustainability in the forest-wood-energy chain »
Collection/Special Issue: Alessandro Paletto (CREA, Trento), Giorgio Matteucci & Mauro Maesano (CNR-ISAFOM)
Abstract
The main coniferous forests of Calabria (Italy) are certainly the Calabrian black pine (Pinus nigra calabrica) forests of the Sila massif and the silver fir (Abies alba) forests of the Serre Vibonesi. Despite these woodlands are of great importance both economically and from a conservationist point of view, biodiversity of moth has been investigated in a non occasional way only for the Sila Calabrian black pine forests, while the silver fir woods of the Serre have been only recently the subject of studies. Apart from increasing the knowledge on the biodiversity of the nocturnal Lepidoptera hosted by Calabrian coniferous forests, the aim of this study was to compare the sampled communities to find out the main differences and their causes. The sampling was conducted in 9 sites for each forest type, distributed so as to cover the different development stages of ecological succession, from open areas to mature woodlands. A light trap was monthly placed at each site from May to November 2015, for a total of 126 nights/trap. The two communities showed low similarity indices (Classic Jaccard = 0.396; Sorensen Classic = 0.568), due both to the component trophically linked to the dominant forest species and to the component linked to the herbaceous layer. In fact, the dominant species in the Calabrian black pine wood and in the silver fir wood (Thera firmata and Macaria liturata, respectively) are absent or only occasionally present in the other forest type, and the community linked to the herbaceous layer is much better represented in the Calabrian black pine forest (29.7% of the total) than in the silver fir forest (14.9%). The arrangement of the Sila landscape, where Calabrian black pine forests alternate with pastures, shrubs and cultivated fields, seems to be the cause of the increased presence of species related to non-forest vegetation layer, while the micro-climatic conditions of the silver fir forest, more humid and temperate, favor the presence of a limited share of species trophically associated with herbaceous plants, which, however, have a high bio-geographical interest.
Keywords
Introduzione
La Calabria è una delle regioni italiane con maggiore copertura forestale. I boschi rappresentano, infatti, più del 40% del territorio regionale (612.931 ha) rispetto a una media nazionale del 34.7% ([16]). Fra le varie tipologie boschive le conifere rivestono una grande importanza, sia per l’industria boschiva, sia dal punto di vista ambientale e paesaggistico. In particolare ci si riferisce ai boschi di pino nero di Calabria (Pinus nigra calabrica (Loud.) Cesca & Peruzzi) e di abete bianco (Abies alba Mill.) che caratterizzano habitat considerati prioritari negli elenchi della Rete Natura 2000 (9220*: Faggete degli Appennini con Abies alba e faggete con Abies nebrodensis; 9510*: Foreste sud-appenniniche di Abies alba; 9530* : Pinete (sub) mediterranee di pini neri endemici). La gestione forestale di questi habitat deve, quindi, porre una grande attenzione alla conservazione della biodiversità e alle complesse interazioni ecologiche di questi ecosistemi ([11], [17]).
Il pino nero di Calabria, la cui posizione tassonomica è ancora oggetto di dibattito, è diffuso in Sicilia e Calabria, ma è in quest’ultima regione e precisamente nell’altipiano della Sila che i boschi mostrano la maggiore estensione (74.625 ha), quasi un terzo della superficie italiana. L’abete bianco è una specie che preferisce le zone montane con alta piovosità e umidità atmosferica. È presente prevalentemente in Europa centrale (Balcani, Carpazi, Germania centro-meridionale e regioni Alpine), ma vi sono altre popolazioni sui Pirenei e lungo l’Appennino, seppure con molta discontinuità. Pur non avendo grandi estensioni (4.851 ha) le abetine in Calabria sono molto interessanti in quanto al loro limite meridionale di distribuzione. In questa regione l’abete bianco è presente con popolazioni isolate, spesso in associazione al faggio, su Pollino, Catena Costiera, Sila, Aspromonte e Serre Vibonesi. Pinete e abetine differiscono nella struttura, nel tipo di associazione vegetale, per le condizioni abiotiche in cui si sviluppano e per le tipologie di trattamento selvicolturale a cui vengono sottoposte.
La domanda che ci poniamo in questo lavoro è quanto queste differenze influenzino la biodiversità animale ospitata. Per cercare di rispondere al quesito, si è scelto di monitorare le comunità di Lepidotteri notturni in entrambe le tipologie forestali e confrontarne i risultati. I Lepidotteri notturni, infatti, sono comunemente considerati degli ottimi indicatori biologici e sono stati spesso utilizzati a questo scopo in vari studi sulla biodiversità e l’ecologia forestale a tutte le latitudini ([2], [31], [30], [7], [25], [13]). Inoltre, soprattutto per gli stadi larvali, c’è un diretto legame trofico con la vegetazione e molte specie hanno nelle conifere la loro principale pianta alimentare.
I dati disponibili in letteratura relativamente alle comunità di Lepidotteri notturni delle conifere dell’Italia peninsulare sono scarni e, con poche eccezioni, sono stati raccolti in modo piuttosto occasionale. Le pinete a pino nero di Calabria sono state indagate con continuità da Russo ([24]) presso la Fossiata (Sila) e da Scalercio ([27]) presso Monte Cocuzzo (Catena Costiera). Tuttavia i dati del primo sono stati pubblicati solo in parte ([18], [19]), e i risultati del secondo sono relativi ad un nucleo di rimboschimento in una area in cui la specie non cresce spontaneamente ed è frammista a latifoglie e abeti. Più consistenti sono le informazioni che riguardano Lepidotteri defogliatori come la Processionaria del Pino (Thaumetopoea pityocampa Denis et Schiffermuller 1775), particolarmente dannosa per le pinete ([6]). Le abetine invece sono state ben indagate in Appennino centro-meridionale ([23], [29]) e solo recentemente in un’area del meridione ([15]). Nel complesso, queste comunità sembrano conservare buoni livelli di funzionalità, essendo presenti molte specie legate troficamente alle specie forestali, alcune delle quali con popolazioni molto disgiunte dall’areale principale.
L’intersecarsi in queste tipologie forestali di interessi economici e conservazionistici rendono particolarmente importante l’approfondimento delle conoscenze sulla biodiversità ospitata in modo che possano essere programmati interventi selvicolturali sempre più consapevoli ed eco-compatibili.
Aree di studio
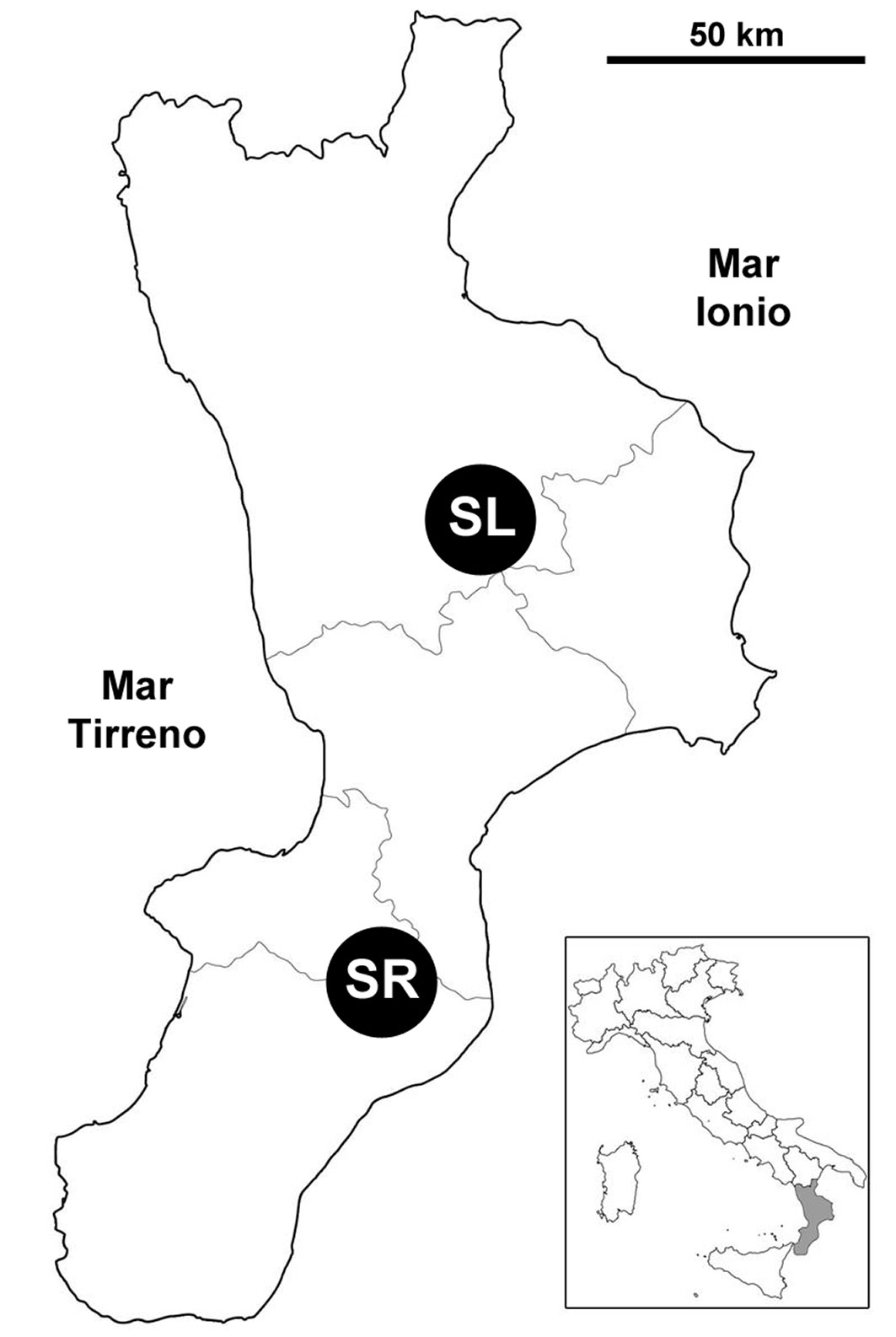
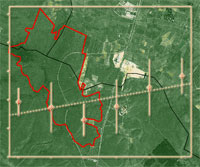
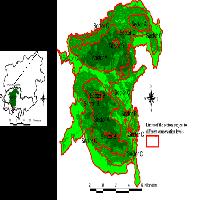
Il campionamento ha interessato le pinete della Sila e le abetine delle Serre Vibonesi (Fig. 1). Le pinete silane si sviluppano su un suolo generato quasi totalmente da rocce di natura cristallina. La superficie sommitale dell’altipiano mostra i caratteri di una vasta spianata continentale con morbide dorsali ([12]). Il clima è di tipo temperato-freddo. La temperatura media annua è di 9 °C con forti escursioni termiche, con picchi di oltre 30 °C in estate e -10 °C in inverno. Le precipitazioni sono sempre elevate, fra 1.200 e 1.600 mm annui, concentrati soprattutto tra settembre e maggio, spesso a carattere nevoso fra dicembre e marzo ([9]).
Fig. 1 - Inquadramento geografico delle aree di studio. SL è il codice identificativo delle pinete della Sila e SR quello delle abetine delle Serre Vibonesi.
Nelle aree interessate dai campionamenti, estese foreste si alternano a pascoli e campi coltivati. Le pinete a pino nero di Calabria rappresentano in alcune aree lo stadio di transizione verso la vegetazione climax della faggeta e occupano solitamente i suoli con la frazione sabbiosa più elevata. Le pinete calabre non possiedono un sottobosco caratteristico ([4]), anche se da qualche autore vengono riferite all’associazione Hypochoerido-Pinetum calabricae ([8]). Nelle pinete fitte, per via della poca luce filtrante e del folto strato di aghi che copre il suolo, il sottobosco è povero. Dove le pinete raggiungono una maggiore maturità e si fanno più rade si possono trovare soprattutto Pteridium aquilinum (L.) Kuhn, Buglossoides calabra (Ten.) I.M. Johnst., arbusti quali Salix caprea L., Prunus spp. e varie specie di ginestre ([4]).
Le Serre vibonesi si trovano nel sud della Calabria, in continuità con il massiccio dell’Aspromonte. L’area di studio è quasi completamente compresa nel comune di Serra San Bruno (VV). Geologicamente le montagne delle Serre sono di natura cristallina. Morfologicamente si identificano due brevi creste montuose parallele a questo tratto appenninico e i terreni hanno una tessitura sabbioso-argillosa ([20]). Il clima cambia con l’altitudine e l’esposizione. L’area valliva centrale, tra gli 800 e i 1000 metri, è caratterizzato da inverni freddi e piovosi ed estati calde ma non secche, con una temperatura media annua di 10.8 °C, mentre in alto il clima è più freddo, con nebbia e piogge frequenti. Le precipitazioni sono molto abbondanti, con una media annua di 1848 mm a Serra San Bruno ([9]). Le foreste di abete bianco sono quasi interamente incluse nel Parco Naturale Regionale delle Serre, tra gli 800 e i 1420 metri di altitudine, con i siti ad altitudini più elevate in associazione al faggio (4800 ha in totale). Gran parte dei boschi sono il risultato dei rimboschimenti degli anni ’60-’70, ma non è difficile trovare aree con esemplari ultracentenari. Oltre a faggio e abete bianco sono presenti anche altre latifoglie, arbusti e piante erbacee, tutti elementi dell’associazione Aquifolio-Fagetum, tipico delle montagne del Sud Italia ([1]).
Materiali e metodi
Le comunità dei Lepidotteri notturni sono state campionate tramite l’utilizzo di trappole luminose. Tali trappole sono composte da un recipiente nel quale viene posto un esalatore di acetato di etile. Sul recipiente è inserito un coperchio a imbuto sovrastato da alette verticali in plexiglas e un tetto orizzontale in materiale plastico. La fonte luminosa è data da un nastro di LED con picco di emissione a 395 nm (15 W), avvolto intorno a un tubo posto fra le alette in plexiglas, alimentato da una batteria a 12V. Le trappole sono state collocate su supporti metallici in modo che la trappola resti sollevata a circa 1.30 m dal terreno, sia per limitare possibili danneggiamenti da parte di animali, sia per rendere la trappola più visibile ai Lepidotteri notturni ponendola al di sopra della vegetazione erbacea e arbustiva.
In ogni area sono state individuate 9 stazioni, per un totale di 18 siti. Le stazioni sono state scelte in modo da coprire la più ampia variabilità possibile degli ecosistemi campionati includendo 3 boschi maturi (boschi radi con piante di età superiore agli 80 anni), 3 boschi giovani (boschi più fitti con piante di età compresa tra i 20 e i 40 anni) e tre stadi iniziali della successione ecologica (radure, prati o zone sottoposte a tagli recenti). Per ogni stazione di campionamento, vengono riportati i nomi delle località, i codici alfanumerici delle stazioni, le coordinate UTM, la quota e una sintetica descrizione della tipologia di trattamento (Tab. 1).
Tab. 1 - Descrizione sintetica dei siti di campionamento: vengono riportati i nomi delle località, i codici alfanumerici assegnati a ogni stazioni, le coordinate UTM, la quota e una sintetica descrizione della tipologia di trattamento
| Località | Codice | Coord. UTM | Quota (m s.l.m.) |
Tipologia trattamento | |
|---|---|---|---|---|---|
| E | N | ||||
| Montagna Grande | SL_A1 | 638895 | 4348709 | 1380 | Pineta - fustaia matura disetanea |
| Montagna Grande | SL_A2 | 639198 | 4349346 | 1294 | Pineta - rimboschimento 2x2 non diradato |
| Montagna Grande | SL_A3 | 638566 | 4348166 | 1352 | Radura pascolata |
| Torre Scarda | SL_B1 | 630586 | 4344332 | 1310 | Pineta - fustaia disetanea matura ~80 anni |
| Quaresima | SL_B2 | 625635 | 4341417 | 1382 | Pineta - rimboschimento diradato |
| Quaresima | SL_B3 | 630208 | 4343972 | 1300 | Radura pascolata |
| Colle Macchie | SL_C1 | 631754 | 4346636 | 1436 | Pineta - fustaia matura disetanea |
| Vallivone | SL_C2 | 632070 | 4346713 | 1453 | Pineta - rimboschimento diradato ~25 anni |
| Colle Macchie | SL_C3 | 631592 | 4346649 | 1433 | Radura pascolata |
| S. Maria | SR_A1 | 614535 | 4268065 | 847 | Abetina - fustaia matura ~150 anni |
| Palmento | SR_A2 | 614557 | 4269042 | 840 | Abetina - fustaia giovane ~30-40 anni |
| Palmento | SR_A3 | 614593 | 4269034 | 827 | Abetina - taglio con matricine e rinnovamento con latifoglie |
| Cattarinella | SR_B1 | 614989 | 4267584 | 940 | Abetina - fustaia matura ~100 anni |
| Cattarinella | SR_B2 | 615110 | 4267307 | 970 | Abetina - rimboschimento 2x2 non diradato |
| Cattarinella | SR_B3 | 615262 | 4266271 | 1039 | Radura a prevalenza di P. aquilinum |
| Sietto dello Caricatore | SR_C1 | 617087 | 4267949 | 1120 | Abetina - fustaia matura ~150 anni |
| Pietra del Signore | SR_C2 | 615992 | 4266586 | 1080 | Abetina mista a faggio con rinnovazione |
| Sietto dello Caricatore | SR_C3 | 616907 | 4267754 | 1110 | Abetina mista a faggio diradata selettivamente |
Le stazioni sono state scelte in modo che ci fosse omogeneità nella copertura vegetale in un raggio di almeno 30 m, coincidente approssimativamente con il raggio di azione delle trappole ([3]). Inoltre, le trappole sono state collocate ad una distanza minima fra esse di 150 metri. Il campionamento ha avuto cadenza mensile fra maggio e novembre 2015, per un totale di 126 notti/trappola. Le 9 trappole collocate nella stessa tipologia vegetale sono state attivate contemporaneamente.
I dati di raccolta sono stati organizzati in una tabella zoosociologica (matrice specie/stazioni) in cui è stato riportato il numero di individui raccolti durante l’arco della ricerca (vedi Appendice 1 e Appendice 2).
La tabella zoosociologica è stata sottoposta ad analisi statistiche multivariate che hanno permesso di ordinare e classificare le comunità rilevate. Come tecnica di ordinamento è stata utilizzata la Detrended Correspondence Analysis (DCA). Il primo (DCA1) ed il secondo asse (DCA2) rappresentano la maggior parte della variabilità fra gli oggetti e il loro peso relativo è misurato come eigenvalue. Come tecnica di classificazione è stata utilizzata la Cluster Analysis scegliendo l’algoritmo (paired group) e la misura di similarità (Morisita’s index for abundance data) più adatti ad una matrice di dati composta da misure di abbondanza delle specie. I dati sono stati sottoposti 100 volte a ricampionamento con rimpiazzo (bootstrap) in modo da avere una misura percentuale della robustezza dei nodi del cluster prodotto. Le analisi statistiche multivariate sono state effettuate con il software libero PAST.
La similarità fra le comunità complessive di pinete e abetine è stata misurata con gli indici di Sorensen Classic (Sc), basato sulla presenza/assenza delle specie, e Jaccard Classic (Jc), basato sulla abbondanza relativa delle specie, entrambe calcolati con il software EstimateS 9.1.0 ([10]). Il valore di questi indici varia fra 0 (nessuna somiglianza) e 1 (completa somiglianza). Inoltre, la testa delle comunità, rappresentata dal 75% degli esemplari rinvenuti nei due comprensori indagati, è stata scomposta in accordo con la dieta larvale delle specie in modo da poter condurre anche analisi di tipo funzionale.
Risultati
Nelle pinete dell’Altipiano della Sila sono stati campionati 10.487 individui appartenenti a 303 specie (Tab. 2, Appendice 1). La comunitàè dominata da Alcis repandata (Linnaeus 1758), Pennithera firmata (Hübner 1822), Idaea deversaria (Herrich-Schäffer 1847), Thaumetopoea pityocampa (Denis & Schiffermüller 1775), Epirrhoe galiata (Denis & Schiffermüller 1775), Aplocera praeformata (Hübner 1826), Dendrolimus pini (Linnaeus 1758), Hylaea mediterranea Sihvonen, Skou, Flamigni, Fiumi & Hausmann 2014, Pachetra sagittigera (Hufnagel 1766), Epirrhoe alternata (Muller 1764), Agrotis cinerea (Denis & Schiffermüller 1775), Scotopteryx luridata (Hufnagel 1767) che corrispondono al 50% di tutti gli individui. A. repandata da sola rappresenta quasi il 15% di tutta la comunità, mentre le altre specie sono più uniformemente ripartite. Per quanto riguarda la corologia sono tutte specie ad ampia distribuzione euro-asiatica, con le importanti eccezioni della mediterranea T. pityocampa e di H. mediterranea, endemica di Italia meridionale e Sicilia.
Tab. 2 - Composizione quali-quantitativa della testa della comunità (75% del totale degli individui) delle pinete della Sila. (ALP): Alimentazione Larvale Prevalente.
| Specie | SL_A1 | SL_A2 | SL_A3 | SL_B1 | SL_B2 | SL_B3 | SL_C1 | SL_C2 | SL_C3 | Totale | ALP |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Pennithera firmata | 27 | 228 | 25 | 40 | 47 | 2 | 101 | 164 | 18 | 652 | Conifere (23.9%) |
| Thaumetopoea pityocampa | 27 | 183 | 83 | 12 | 38 | 1 | 31 | 85 | 17 | 477 | |
| Dendrolimus pini | 25 | 18 | 70 | 40 | 23 | 2 | 23 | 40 | 13 | 254 | |
| Hylaea mediterranea | 7 | 121 | 2 | 8 | 3 | 0 | 9 | 66 | 1 | 217 | |
| Eupithecia indigata | 5 | 32 | 0 | 9 | 25 | 0 | 18 | 63 | 0 | 152 | |
| Sphinx pinastri | 8 | 7 | 5 | 27 | 6 | 2 | 14 | 32 | 1 | 102 | |
| Mythimna conigera | 0 | 0 | 2 | 15 | 22 | 7 | 2 | 1 | 1 | 50 | |
| Peribatodes rhomboidaria | 25 | 27 | 34 | 17 | 12 | 6 | 5 | 8 | 4 | 138 | Latifoglie (1.7%) |
| Scotopteryx luridata | 22 | 145 | 14 | 2 | 5 | 2 | 5 | 6 | 0 | 196 | Arbusti (5.7%) |
| Pseudoterpna coronillaria | 10 | 71 | 25 | 5 | 18 | 1 | 12 | 21 | 3 | 166 | |
| Scotopteryx angularia | 27 | 53 | 4 | 0 | 0 | 0 | 0 | 0 | 0 | 84 | |
| Alcis repandata | 150 | 439 | 83 | 344 | 76 | 16 | 127 | 270 | 33 | 1538 | Arbusti e piante erbacee (25.1%) |
| Diarsia mendica | 12 | 9 | 0 | 45 | 11 | 0 | 22 | 41 | 0 | 140 | |
| Chiasmia clathrata | 41 | 7 | 14 | 9 | 0 | 3 | 13 | 4 | 5 | 96 | |
| Xestia triangulum | 5 | 4 | 1 | 33 | 13 | 1 | 11 | 16 | 0 | 84 | |
| Idaea fuscovenosa | 29 | 10 | 41 | 0 | 0 | 0 | 0 | 0 | 0 | 80 | |
| Idaea aversata | 4 | 26 | 2 | 10 | 2 | 0 | 7 | 4 | 1 | 56 | |
| Epirrhoe galiata | 62 | 102 | 25 | 51 | 12 | 3 | 98 | 116 | 5 | 474 | Piante erbacee (29.7%) |
| Aplocera praeformata | 4 | 9 | 3 | 25 | 7 | 7 | 81 | 116 | 71 | 323 | |
| Epirrhoe alternata | 5 | 15 | 3 | 26 | 54 | 0 | 19 | 89 | 3 | 214 | |
| Agrotis cinerea | 16 | 6 | 26 | 7 | 14 | 23 | 54 | 35 | 31 | 212 | |
| Charanyca ferruginea | 34 | 29 | 2 | 13 | 21 | 0 | 42 | 22 | 1 | 164 | |
| Aplocera plagiata | 14 | 22 | 22 | 11 | 6 | 3 | 12 | 44 | 10 | 144 | |
| Cosmorhoe ocellata | 11 | 52 | 7 | 21 | 22 | 0 | 5 | 14 | 1 | 133 | |
| Eupithecia subfuscata | 39 | 8 | 2 | 25 | 6 | 0 | 10 | 28 | 2 | 120 | |
| Colostygia pectinataria | 0 | 5 | 0 | 54 | 15 | 2 | 14 | 16 | 5 | 111 | |
| Eulithis pyraliata | 8 | 43 | 1 | 6 | 1 | 0 | 7 | 12 | 0 | 78 | |
| Gymnoscelis rufifasciata | 9 | 4 | 20 | 16 | 4 | 0 | 8 | 13 | 2 | 76 | |
| Hypena proboscidalis | 3 | 7 | 0 | 27 | 8 | 5 | 6 | 9 | 2 | 67 | |
| Scotopteryx chenopodiata | 15 | 17 | 0 | 2 | 27 | 0 | 3 | 0 | 1 | 65 | |
| Charissa onustaria | 12 | 20 | 18 | 0 | 0 | 0 | 9 | 3 | 0 | 62 | |
| Conisania luteago | 7 | 7 | 24 | 3 | 2 | 4 | 9 | 2 | 2 | 60 | |
| Hoplodrina octogenaria | 4 | 6 | 10 | 6 | 3 | 0 | 17 | 12 | 1 | 59 | |
| Pachetra sagittigera | 53 | 19 | 23 | 9 | 3 | 1 | 49 | 32 | 25 | 214 | Graminacee (3.8%) |
| Luperina dumerilii | 2 | 1 | 2 | 3 | 50 | 21 | 2 | 6 | 2 | 89 | |
| Idaea deversaria | 12 | 391 | 74 | 0 | 0 | 0 | 30 | 14 | 1 | 522 | Piante erbaceee detrito (6.6%) |
| Eilema lurideola | 34 | 20 | 22 | 48 | 15 | 10 | 16 | 13 | 3 | 181 | Detrito, muschi e licheni (2.3%) |
| Itame messapiaria | 19 | 32 | 6 | 0 | 0 | 0 | 0 | 0 | 0 | 57 | Sconosciuta(1.4%) |
| Stilbia faillae | 5 | 19 | 0 | 6 | 1 | 0 | 8 | 12 | 2 | 53 |
Nelle abetine delle Serre Vibonesi sono stati campionati 5.025 individui appartenenti a 253 specie (Tab. 3, Appendice 2). La comunitàè dominata da Macaria liturata (Clerck 1759), Pungeleria capreolaria (Denis & Schiffermüller 1775), Lithosia quadra (Linnaeus 1758), Alcis repandata (Linnaeus 1758), Dendrolimus pini (Linnaeus 1758), Colostygia pectinataria (Knoch 1781), Peribatodes rhomboidaria (Denis & Schiffermüller 1775), Lymantria monacha (Linnaeus 1758), Sphinx pinastri Linnaeus 1758, Thera britannica (Turner 1925), Dysstroma truncata (Hufnagel 1767) e Peribatodes secundaria (Denis & Schiffermüller 1775) che corrispondono al 50% degli individui catturati. Le specie appartenenti alla comunità sono rappresentate, tendenzialmente, da un basso numero di individui e mostrano abbondanze relative ripartite in modo piuttosto uniforme. La specie più abbondante (M. liturata) rappresenta, infatti, poco più dell’8% degli individui totali. Tutte le specie dominanti mostrano una corologia a gravitazione asiatico-europea.
Tab. 3 - Composizione quali-quantitativa della testa della comunità (75% del totale degli individui) delle abetine delle Serre.(ALP): Alimentazione Larvale Prevalente.
| Specie | SR_A1 | SR_A2 | SR_A3 | SR_B1 | SR_B2 | SR_B3 | SR_C1 | SR_C2 | SR_C3 | Totale | ALP |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Macaria liturata | 27 | 59 | 0 | 29 | 77 | 3 | 47 | 176 | 2 | 420 | Conifere (39.1%) |
| Pungeleria capreolaria | 22 | 42 | 2 | 29 | 60 | 8 | 22 | 100 | 17 | 302 | |
| Dendrolimus pini | 23 | 14 | 3 | 31 | 25 | 2 | 65 | 80 | 5 | 248 | |
| Sphinx pinastri | 22 | 7 | 0 | 16 | 14 | 1 | 50 | 23 | 10 | 143 | |
| Thera britannica | 5 | 9 | 1 | 8 | 11 | 3 | 31 | 43 | 21 | 132 | |
| Peribatodes secundaria | 10 | 24 | 0 | 24 | 19 | 1 | 9 | 18 | 1 | 106 | |
| Hylaea mediterranea | 13 | 28 | 0 | 7 | 8 | 0 | 9 | 13 | 1 | 79 | |
| Thera variata | 1 | 13 | 2 | 5 | 9 | 0 | 0 | 6 | 5 | 41 | |
| Lymantria monacha | 8 | 18 | 3 | 24 | 14 | 0 | 66 | 10 | 2 | 145 | Conifere e latifoglie (3.9%) |
| Peribatodes rhomboidaria | 16 | 37 | 10 | 11 | 24 | 21 | 11 | 7 | 15 | 152 | Latifoglie (15.1%) |
| Colocasia coryli | 4 | 2 | 0 | 9 | 11 | 0 | 19 | 38 | 0 | 83 | |
| Hypomecis roboraria | 23 | 4 | 0 | 8 | 7 | 0 | 8 | 22 | 2 | 74 | |
| Epirrita christyi | 9 | 4 | 0 | 3 | 9 | 0 | 2 | 24 | 4 | 55 | |
| Ourapteryx sambucaria | 1 | 6 | 0 | 6 | 1 | 0 | 2 | 25 | 1 | 42 | |
| Watsonalla cultraria | 0 | 0 | 0 | 8 | 2 | 2 | 2 | 15 | 7 | 36 | |
| Ennomos quercinaria | 0 | 2 | 0 | 1 | 12 | 0 | 0 | 20 | 0 | 35 | |
| Xanthia aurago | 0 | 0 | 0 | 0 | 0 | 0 | 9 | 22 | 2 | 33 | |
| Campaea margaritata | 1 | 3 | 0 | 2 | 7 | 1 | 1 | 15 | 0 | 30 | |
| Ligdia adustata | 5 | 16 | 4 | 0 | 2 | 0 | 0 | 1 | 1 | 29 | |
| Alcis repandata | 9 | 34 | 5 | 13 | 38 | 15 | 37 | 123 | 13 | 287 | Arbusti e piante erbacee (13.1%) |
| Dysstroma truncata | 12 | 39 | 5 | 15 | 23 | 1 | 10 | 16 | 9 | 130 | |
| Idaea aversata | 6 | 6 | 1 | 3 | 7 | 1 | 2 | 12 | 0 | 38 | |
| Ectropis crepuscularia | 6 | 21 | 1 | 5 | 2 | 1 | 0 | 2 | 0 | 38 | |
| Colostygia pectinataria | 18 | 16 | 1 | 33 | 29 | 2 | 23 | 42 | 16 | 180 | Piante erbacee (14.9%) |
| Hypena proboscidalis | 7 | 6 | 1 | 2 | 22 | 5 | 8 | 18 | 2 | 71 | |
| Ecliptopera silaceata | 13 | 8 | 0 | 3 | 5 | 1 | 13 | 19 | 2 | 64 | |
| Eugnorisma depuncta | 4 | 13 | 1 | 6 | 7 | 0 | 12 | 8 | 3 | 54 | |
| Gymnoscelis rufifasciata | 9 | 3 | 2 | 10 | 6 | 2 | 1 | 5 | 12 | 50 | |
| Xanthorhoe vidanoi | 5 | 7 | 3 | 6 | 8 | 0 | 4 | 8 | 6 | 47 | |
| Euplexia lucipara | 5 | 8 | 2 | 5 | 7 | 1 | 5 | 7 | 0 | 40 | |
| Xanthorhoe biriviata | 16 | 4 | 1 | 4 | 3 | 0 | 0 | 0 | 0 | 28 | |
| Lasionycta calberlai | 4 | 4 | 0 | 6 | 9 | 0 | 3 | 2 | 0 | 28 | |
| Noctua pronuba | 7 | 7 | 0 | 2 | 9 | 0 | 7 | 36 | 4 | 72 | Piante erbacee e graminacee (1.9%) |
| Protodeltote pygarga | 11 | 10 | 0 | 10 | 8 | 5 | 2 | 1 | 1 | 48 | Graminacee (2.1%) |
| Apamea monoglypha | 0 | 0 | 0 | 1 | 4 | 0 | 3 | 23 | 0 | 31 | |
| Herminia tarsicrinalis | 6 | 22 | 6 | 9 | 4 | 0 | 0 | 1 | 0 | 48 | Detrito. muschi e licheni (9.9%) |
| Lithosia quadra | 166 | 9 | 10 | 15 | 4 | 7 | 38 | 12 | 35 | 296 | |
| Eilema deplana | 21 | 4 | 2 | 1 | 0 | 0 | 0 | 0 | 0 | 28 |
La somiglianza di queste due comunitàè piuttosto bassa (Sc = 0.568; Jc = 0.396), anche se in entrambe le tipologie forestali dominano le specie legate alle conifere che, nelle pinete, sono seguite da una componente più legata ad arbusti e piante erbacee (Tab. 2), mentre nelle abetine da una componente più o meno equivalente di specie legate a latifoglie e piante erbacee (Tab. 3).
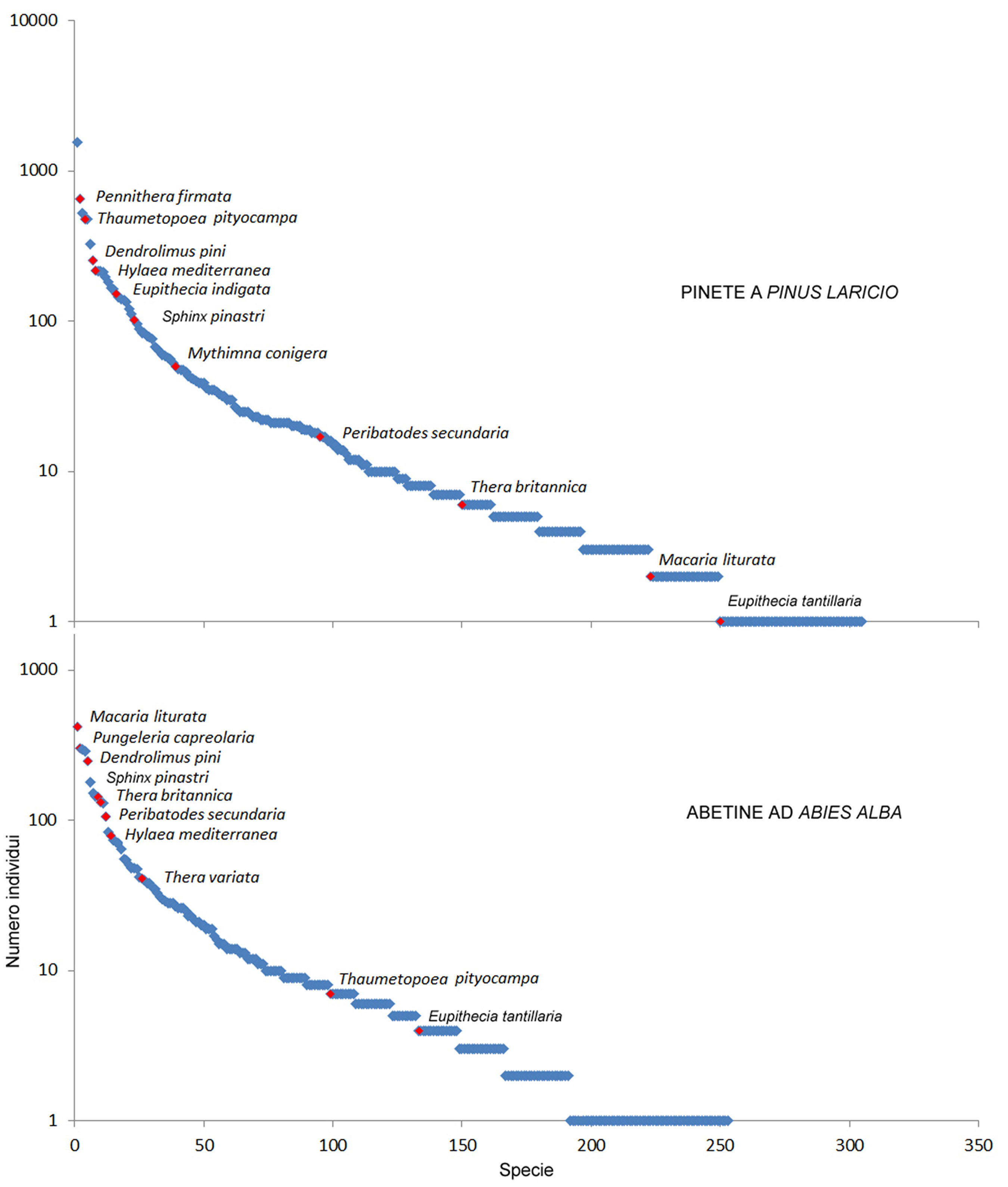
I lepidotteri le cui larve sono infeudate alle conifere dominanti, cioè Pinus nigra calabrica e Abies alba nei due scenari indagati, sono particolarmente frequenti nella testa delle comunità e differiscono in modo sostanziale nelle due tipologie forestali, soprattutto in funzione della dieta larvale (Fig. 2). Pennithera firmata, Eupithecia indigata (Hübner 1813) e Mythimna conigera (Denis & Schiffermüller 1775), le cui larve si sviluppano su Pinus, sono del tutto assenti nelle abetine. D’altro canto, Macaria liturata, Pungeleria capreolaria e Thera variata (Denis & Schiffermüller 1775), le cui larve si alimentano a spese di Abies, sono praticamente assenti nelle pinete, ad eccezione di un unico esemplare di M. liturata.
Fig. 2 - Strutture di comunità. Vengono mostrate le strutture di comunità dei Macrolepidotteri delle pinete (in alto) e delle abetine (in basso) in scala logaritmica. In rosso sono indicate le specie troficamente legate alle conifere in regime di monofagia o oligofagia.
Accanto a queste vi è un contingente di specie comuni e abbondanti in entrambe le tipologie forestali, le cui larve sono oligofaghe su diverse specie di conifere (Dendrolimus pini, Hylaea mediterranea, Sphinx pinastri e Peribatodes secundaria).
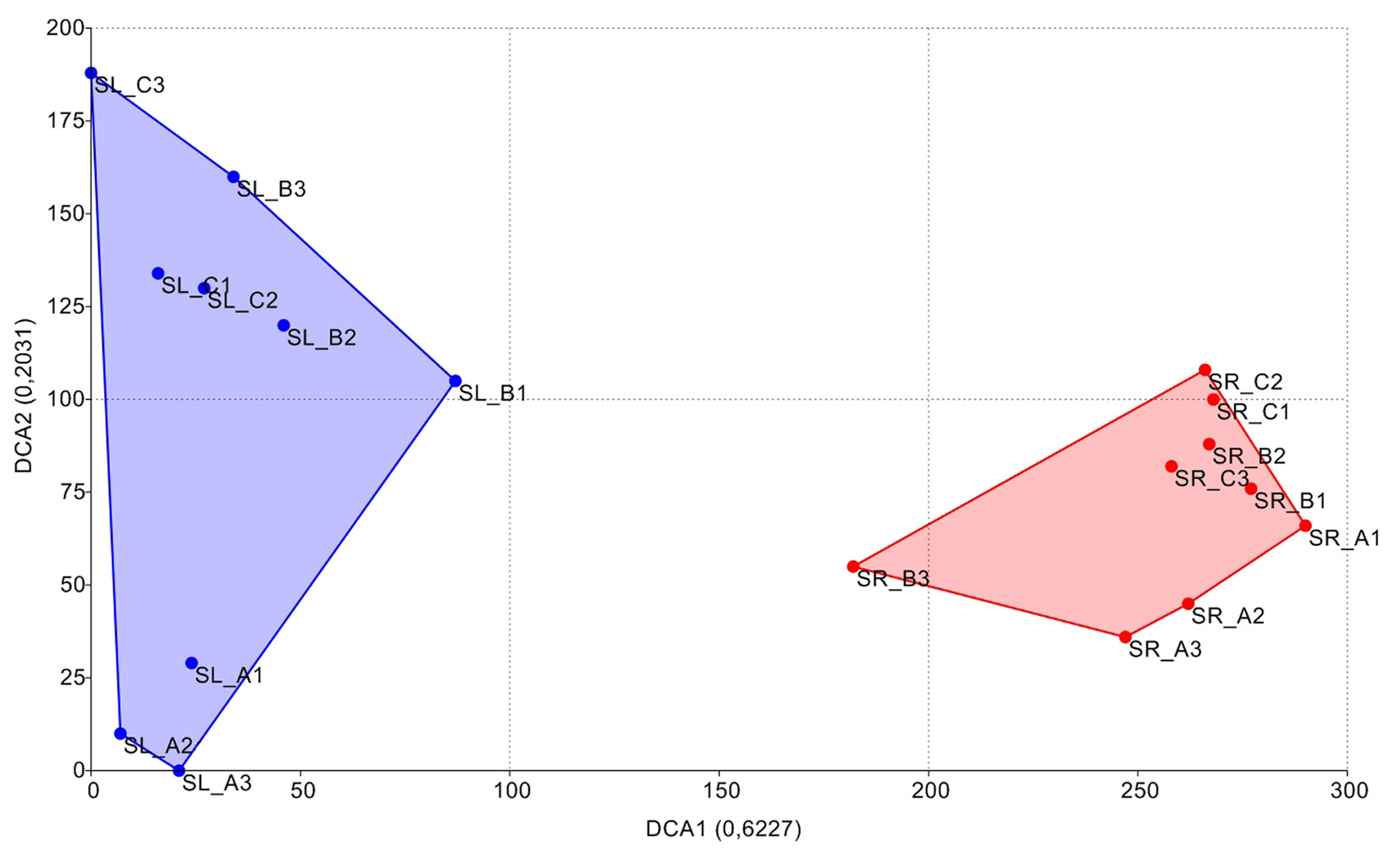
Queste differenze nella composizione specifica delle comunità e nelle abbondanze relative delle specie che le compongono spiegano la chiara separazione sul piano cartesiano individuato dai primi due assi della DCA (Detrended Correspondence Analysis) delle comunità delle due foreste di conifere (Fig. 3). I convex hulls che racchiudono i siti indagati hanno molto spesso sul loro perimetro le comunità degli stadi iniziali della successione ecologica. Questo è stato osservato sia nelle pinete che nelle abetine, dove solo SR_C3, che però è un bosco di recente diradamento, è incluso all’interno del poligono (Fig. 3). Ciò mostra una maggiore omogeneità fra le comunità più strettamente forestali e una marcata differenziazione di queste con quelle di ambienti più aperti.
Fig. 3 - Detrended Correspondence Analysis (DCA). L’analisi è stata eseguita sulle abbondanze delle specie; in blu i siti di campionamento delle pinete, in rosso quelli delle abetine.
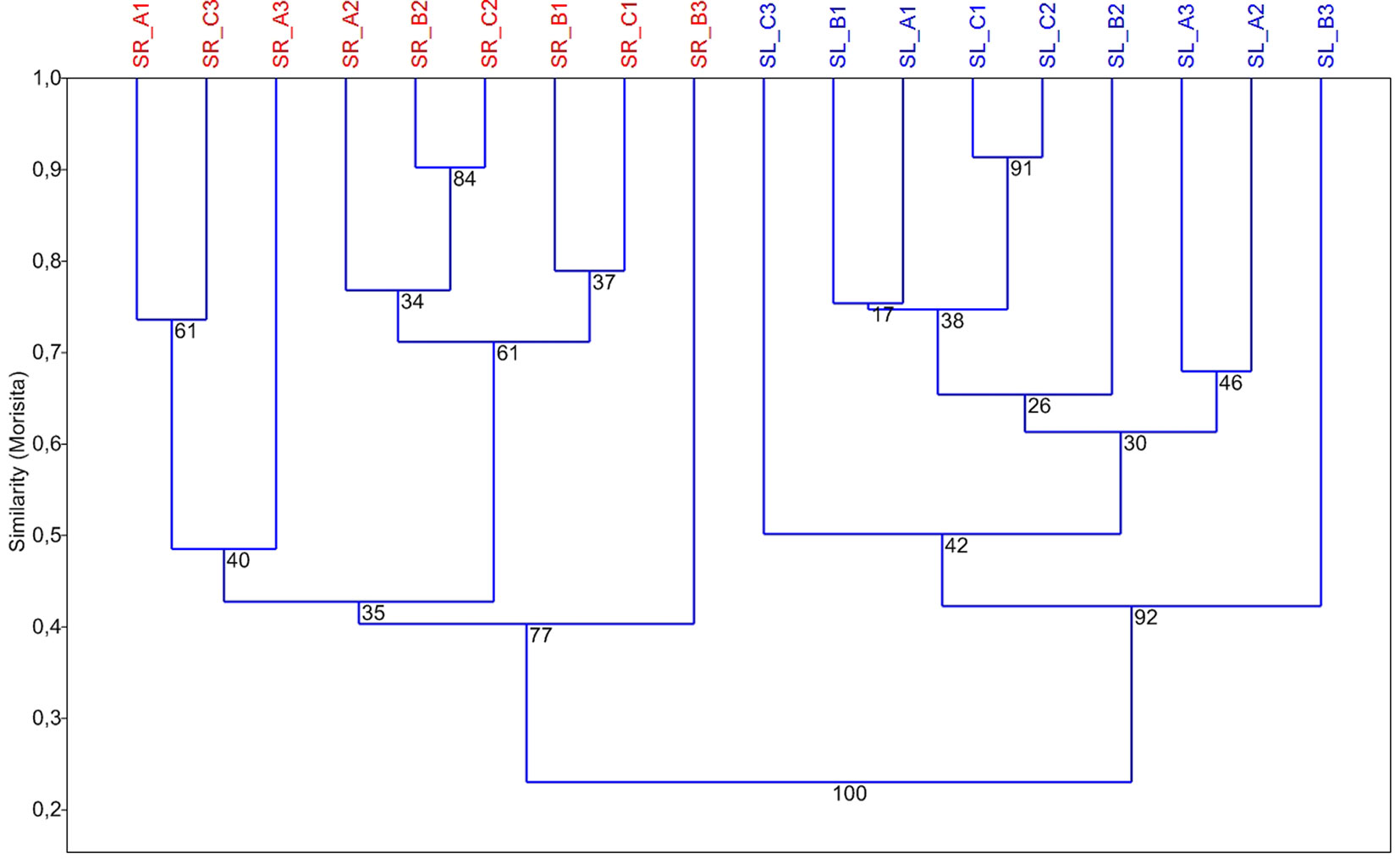
La Cluster Analysis ha confermato la distinzione delle comunità di pineta da quelle di abetina, il cui nodo è confermato nel 100% delle reiterazioni. Altri nodi molto robusti (>70%) separano alcuni ambienti aperti (SR_B3, SL_B3) dagli altri e uniscono boschi con le stesse caratteristiche strutturali (SR_B2 con SR_C2) o vicini fra loro (SL_C1 con SL_C2 - Fig. 4).
Fig. 4 - Cluster Analysis delle comunità rilevate (paired group, Morisita’s index). La “robustezza” dei nodi è indicata come percentuale delle reiterazioni che hanno dato esito identico.
Discussione
Le comunità rinvenute nelle pinete della Sila e nelle abetine delle Serre Vibonesi sono chiaramente distinte, mostrando bassi valori di similarità dovuti principalmente alle diverse preferenze trofiche delle specie che compongono la testa delle comunità. Fra le specie le cui larve si nutrono di conifere, solo Dendrolimus pini, Hylaea mediterranea e Sphinx pinastri sono comuni in entrambe i boschi. Di queste, nelle abetine di Collemeluccio ([23]) e di Rosello ([29]) sembra essere assente solo D. pini pur essendo noto che le sue larve sono polifaghe su conifere ([5]). Le differenze fra le comunità possono quindi essere dovute non solo a differenze biologiche, ma anche alla storia biogeografica di un comprensorio. A questo proposito è molto interessante notare la presenza nella testa della comunità delle pinete di Eupithecia indigata, assente nell’Appennino a nord della Calabria, ma molto comune in Sila, anche in rimboschimenti non diradati di circa 30 anni e ritenuta presente in Calabria solo dubitativamente fino a un decennio addietro ([21]).
Anche il microclima riveste un ruolo chiave nel definire le comunità di Lepidotteri. In Sila i suoli delle pinete hanno generalmente una tessitura in cui predomina la componente sabbiosa e le precipitazioni sono meno abbondanti rispetto alle Serre, con carattere spesso nevoso in inverno. Inoltre, la spessa coltre di aghi sul suolo delle pinete limita la presenza di piante erbacee all’interno dei boschi più fitti. La quota, mediamente più alta delle stazioni silane, contribuisce a differenziare le due aree indagate. Il complesso di questi fattori determina un microclima tendenzialmente più secco e freddo in Sila che favorisce una vegetazione erbacea più xerofila e la presenza di numerosi arbusti come Cytisus spp. e Prunus spp. Al contrario, le Serre sono caratterizzate da una piovosità estremamente elevata e con meno fluttuazioni durante l’anno che, associata a un suolo in cui la componente argillosa è notevolmente maggiore, favorisce lo sviluppo di un’abbondante lettiera, di un cospicuo strato di muschi e licheni e di un sottobosco composto da piante francamente igrofile.
L’assetto paesaggistico delle due aree di ricerca è anch’esso piuttosto differente. La Sila è un vasto altopiano caratterizzato da pendii morbidi che hanno favorito agricoltura e pascolo che hanno modificato il paesaggio. Ne deriva un’alternanza fra boschi di notevole estensione e aree aperte anch’esse proporzionalmente molto estese. A queste si aggiungono vari ambienti di transizione quali pascoli e coltivi abbandonati, arbusteti, piccoli acquitrini legati all’irrigazione, rimboschimenti non trattati o aree disboscate in tempi relativamente recenti, ecc. Sulle Serre, invece, i rilievi sono più aspri e l’estensione è minore, il che non ha permesso lo sviluppo di attività agricolo-pastorali importanti, mentre lo sfruttamento delle risorse forestali è da sempre la principale attività e per motivi storici ha spesso seguito dinamiche ecologicamente non troppo depauperanti. Di conseguenza il bosco è meno frammentato, le aree aperte sono di piccole dimensioni e la vegetazione erbaceo-arbustiva presente è prevalentemente composta da specie tipicamente legate al sottobosco.
Tutto ciò ha influenzato le due comunità di Lepidotteri in modo significativo. In Sila sono favorite le specie praticole come Aplocera praeformata e Agrotis cinerea, quest’ultima caratterizzante anche i pascoli silani d’alta quota in faggeta ([26]). Sulle Serre invece troviamo specie tipicamente legate al sottobosco, sia tra le specie dominanti (Colostygia pectinataria, Ecliptopera silaceata Denis & Schiffermüller 1775, Xanthorhoe vidanoi Parenzan & Hausmann 1994), sia nella coda della comunità, con specie rare e faunisticamente rilevanti come Naenia typica (Linnaeus 1758) e Chalyptra thalictri (Borkhausen 1790). Per gli stessi motivi sulle Serre sono favorite le specie detritivore (Herminia tarsicrinalis Knoch 1782) o legate a muschi e licheni (Lithosia quadra).
La maggiore presenza di latifoglie frammiste agli abeti nei boschi delle Serre e la presenza di radure e cespuglieti nel paesaggio montano della Sila, dunque, sembrano causare questo pattern di distribuzione delle specie, attribuendo un significato importante alla vegetazione associata alle conifere dominanti nel determinare la composizione delle comunità. La diversità di specie di Lepidotteri notturni legate alla vegetazione erbaceo-arbustiva in Sila potrebbe anche essere favorita dalla mancanza di associazioni vegetali stabili delle pinete. A seconda dell’esposizione e delle condizioni ecologiche locali, infatti, il loro sottobosco può essere ricco delle piante tipiche dei querceti e castagneti, dei pascoli aridi, o delle faggete.
L’interesse biogeografico dei boschi di Abies alba delle Serre Vibonesi è stato recentemente sottolineato da Infusino et al. ([14]), i quali hanno evidenziato come le abetine ospitino una fauna non particolarmente ricca di specie ma molto peculiare e spesso con popolazioni piuttosto isolate. È questo ad esempio il caso di Hypomecis roboraria (Denis & Schiffermüller 1775), Phragmitiphila nexa (Hübner 1808), Apamea Epomidion (Haworth 1809), Odontopera bidentata (Clerck 1759) e Chalyptra thalictri. Le ultime due inoltre mostrano una distribuzione eurasiatica con il Molise e l’Abruzzo rispettivamente che rappresentano per entrambe il loro precedente limite meridionale di areale ([22]). Le popolazioni delle Serre sono quindi molto isolate, rivestendo un particolare interesse biogeografico.
Da questo punto di vista anche i boschi della Sila a Pinus nigra calabrica hanno fornito nuovi dati su specie interessanti come A. epomidion e O. bidentata, entrambe segnalate solo di recente in Calabria ([14]). Ma la specie più interessante è stata sicuramente Nothocasis rosariae Scalercio et al. ([28]), specie recentemente descritta proprio per la Sila, il cui areale, ancora in corso di definizione, comprende Sila, Pollino ed Epiro (Grecia - [28]).
Conclusioni
Le comunità di Lepidotteri notturni ospitati da abetine e pinete in Calabria mostrano dei caratteri decisamente peculiari, in parte dovuti alle preferenze alimentari delle larve delle specie legate alle rispettive conifere dominanti e in parte da attribuire alla differente composizione del mosaico paesaggistico. Le abetine rappresentano ambienti decisamente più stabili, con una composizione floristica tipica e scarsa presenza di ambienti aperti, per lo più dovuti ai tagli selvicolturali. Il paesaggio delle pinete, invece, è più diversificato soprattutto da fattori di disturbo antropici che hanno complicato il mosaico, creando ampi pascoli, arbusteti e aree coltivate. Inoltre, anche il microclima più umido delle abetine contribuisce nel determinare differenze apprezzabili nelle due comunità soprattutto nella componente detritivora associata al sottobosco. Queste osservazioni possono contribuire ad una pianificazione ecosostenibile degli interventi forestali, ancor più quando tali interventi insistono su territori e/o habitat sottoposti a tutela naturalistica.
Ringraziamenti
Si ringraziano la Dott.ssa Silvia Greco per il supporto nell’attività di campo, i signori Carlo Di Marco, Franco Calabrese, Gino Scarpelli, Massimo ed Ettore Salerno per il supporto tecnico. Il lavoro è stato finanziato dal Progetto “ALForLab” (PON03PE_0002 4_1) cofinanziato dal Programma Operativo Nazionale Ricerca e Competitivita’ (PON R&C) 2007-2013, attraverso il Fondo Europeo di Sviluppo Regionale (FESR) e risorse nazionali (Fondo di Rotazione (FDR) - Piano di Azione e Coesione (PAC) MIUR).
References
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Online | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar