Wild boar (Sus scrofa) as a driving force of vegetation changes in an urban mediterranean forest affecting species richness and biodiversity within a protected area
Forest@ - Journal of Silviculture and Forest Ecology, Volume 17, Pages 71-77 (2020)
doi: https://doi.org/10.3832/efor3284-017
Published: Aug 04, 2020 - Copyright © 2020 SISEF
Research Articles
Abstract
The Insugherata Protected Area is a remnant urban forest located on the outskirt of the city of Rome; it is rich in native plant species and biodiversity and provides several ecosystem services. Since 2004 the environmental pressure on this fragmented forest ecosystem strongly increased due to the ingression of wild boar (Sus scrofa) which currently has a permanent population in the Reserve and is considered a “pest” impacting several habitats. In 1994, before wild boars ingression, a vegetation survey was undertaken in the Reserve and 20 years later, in 2015, they were repeated in the same plots, being the presence of wild boars the only known change in pressures occurred over time. The comparison of the flora assemblage between the two periods showed a decrease in number of plant species (-15.8%), particularly in the understory. Geophyte was the life form more affected with a decrease in number of species (-22.6%) and coverage (-29.7%) from 1994 to 2015. Also species indicator of environment quality (i.e., orchids) and of biogeographical plant communities disappeared overtime, together with locally rare species, indicating a severe impact on biodiversity not only limited to plant richness. The consistent vegetation changes occurred between the two periods were also computed with a plant community turnover of approximately 40% (Sørensen index of dissimilarity) and one-way analysis of similarities p<0.05 (ANOSIM). Management of the wild boar population is needed in order to favor habitat conservation and reduce local biodiversity loss, as stated in the designation legislative framework of the Reserve.
Keywords
Vegetation remnants, Urban biodiversity, Urban forest, Wildlife pressure
Introduzione
I residui di vegetazione forestale in ambiente urbano e periurbano, oltre a fornire servizi ecosistemici quali il miglioramento della qualità dell’aria, la mitigazione locale del clima, e ad offrire aree con funzione di svago e valore estetico-culturale ([41]), sono riconosciuti come luoghi iconici naturali ([35]) e rappresentano dei siti di protezione di specie e di genotipi locali fondamentali per la conservazione della biodiversità ([33]). Nonostante l’oggettiva importanza di questi habitat marginali, la loro conservazione è sempre a rischio a causa della progressiva frammentazione e delle molteplici pressioni a cui sono sottoposti ([20]). Le loro ridotte dimensioni, infatti, riducono le loro capacità di resilienza ed aumentano gli effetti delle continue minacce di origine antropica (quali l’inquinamento, incendi, o l’eccessivo pascolo nelle zone dove è presente, oltre all’avanzare dell’urban sprawl). Per verificare il loro status di conservazione è importante realizzare monitoraggi periodici degli habitat, possibilmente sempre negli stessi siti ([12]), in maniera tale che si possa disporre di una serie di dati continua nel tempo con cui rilevare e quantificare il grado di eventuale alterazione di questi lembi di vegetazione forestale anche in relazione al modificarsi delle pressioni ([18]).
L’isolamento e la frammentazione degli habitat marginali possono essere contrastati attraverso aree di collegamento, note come corridoi ecologici, che riducono le discontinuità tra le aree. Di fatto i corridoi sono “infrastrutture” realizzate o favorite dall’uomo, e contestualmente alla loro realizzazione dovrebbe essere assicurata anche la loro gestione ([28]), in maniera che i corridoi non favoriscano la diffusione di specie non indigene o dannose che all’interno di aree frammentate possono più facilmente impattare gli ecosistemi ([29]).
Nella regione mediterranea una delle specie considerate più impattanti (specie ecosystem allogenic engineers, sensu [31]) è sicuramente il cinghiale (Sus scrofa), che per le sue caratteristiche biologiche (elevata capacità riproduttiva, plasticità ecologica, comportamento alimentare onnivoro ed opportunista), l’assenza o la scarsa incidenza di predatori naturali e le difficoltà gestionali di riduzione della densità, è in grado di impattare negativamente gli habitat frammentati ([7], [45], [26]); in habitat di fatto alterati il cinghiale può impattare come una specie invasiva, anche se la specie è di origine euroasiatica e quindi appartenente alla biocenosi della penisola italiana ([32]). Per poter gestire e mitigare la pressione del cinghiale sugli ecosistemi naturali è importante anche riuscire a quantificare l’entità degli impatti; la possibilità di confrontare lo stato degli habitat prima e dopo la comparsa di specie impattanti quali il cinghiale, non solo può essere utile a quantificarne gli impatti ma permette anche di avere informazioni sullo stato iniziale in caso di ripristino ambientale, in particolare all’interno delle Aree Protette la cui normativa di istituzione include, tra le altre finalità, la conservazione della biodiversità.
Nell’area di Roma nord la presenza del cinghiale si è diffusa in maniera più massiccia e documentata a partire dal 2005 circa ([13], [38], [2]), grazie anche al sistema ambientale costituito dalla rete delle aree protette periurbane, che ha favorito la diffusione della specie dalle aree verdi del sistema naturale/rurale esteso di Veio-Bracciano alle aree con esse in contatto, tra cui la Riserva dell’Insugherata, in cui non era anteriormente nota e dove ora, invece, ha una elevata densità ([42], [44]). I cinghiali, infatti, entrano nelle aree periurbane, dagli habitat naturali/rurali circostanti, sfruttando i corridoi ecologici alla ricerca di cibo e preferendo gli ambienti frammentati ([14]).
Scopo del presente lavoro è quello di valutare l’impatto, su un ecosistema forestale urbano, della comparsa di una popolazione stabile di cinghiali attraverso l’analisi dei dati vegetazionali derivanti da 20 rilievi floristici ripetuti a 20 anni di distanza nelle stesse stazioni, permettendo così di confrontare due diversi stadi, prima e dopo la presenza/ invasione dei cinghiali all’interno della Riserva Regionale dell’Insugherata.
Materiali e metodi
Area di studio
La Riserva Naturale Regionale dell’Insugherata è un’area protetta ufficialmente istituita con Legge Regionale n. 29 del 1997 che si estende per circa 700 ha nel settore Nord Ovest di Roma. Il reticolo idrografico è caratterizzato da brevi corsi d’acqua confluenti nel Fosso dell’Acqua Traversa, affluente di destra del Tevere, che hanno inciso nei sedimenti sabbioso-argillosi un sistema di basse valli piuttosto aperte, occupate da vegetazione semi-naturale. I versanti ad esposizione prevalentemente settentrionale presentano formazioni mesofile con elementi caratteristici sia dell’orizzonte della faggeta sia dei boschi planiziali, ascrivibili all’associazione Aquifolio-Fagetum subass. carpinetosum betuli; i versanti ad esposizione meridionale sono occupati da formazioni miste a roverella e sughera, localmente prevalenti l’una sull’altra, ricadenti nell’ordine Quercetalia pubescenti-petraeae; le esposizioni intermedie o le poche stazioni sommitali boscate sono occupate da cedui invecchiati di cerro con farnetto riconducibili all’alleanza Teucrio siculi-Quercion cerridis; estremamente localizzate sono le facies a dominanza di leccio, che occupano gli affioramenti tufacei a pendenza elevata, ascrivibili all’associazione Orno-Quercetum ilicis ([6]). Nel complesso, l’area è contraddistinta da un sorprendente grado di integrità ambientale, come indicato da diversi studi locali che hanno indagato, oltre alla componente vegetale ([46], [16]) anche varie comunità animali ([47], [23], [39]).
Pressioni
Al fine di valutare quali siano stati i principali cambiamenti nelle pressioni avvenuti durante i 20 anni trascorsi, sono stati verificate, sulla base dei dati disponibili negli archivi dell’Ente di Gestione della Riserva e da letteratura scientifica disponibile, eventuali differenze temporali nei regimi di: incendi, pascolo animali da allevamento, agricoltura, animali selvatici (cinghiali). Visto l’arco temporale ridotto, per poter valutare trend di lungo termine dei dati termopluviometrici, non sono state prese in considerazione in questo studio eventuali variazioni climatiche. Deve essere riconosciuto però che studi recenti su ambienti alpini e di tundra dimostrano come all’aumento della temperatura dovuto ai cambiamenti climatici corrisponda una diversità nella composizione floristica ([24], [49]).
Flora
Nel 1994 venne condotta un’indagine fitosociologica sulle formazioni forestali della Tenuta dell’Insugherata, ora Riserva Naturale Regionale; dal plot complessivo dei rilievi di flora, nel 2015, per lo scopo di questo studio, ne sono stati selezionati 20 in modo casuale ma tale da garantire un’omogenea distribuzione tra le differenti esposizioni e cenosi ambientali dell’area. In corrispondenza delle stazioni di questi 20 rilievi originali è stato quindi ripetuto il campionamento della flora secondo le stesse modalità adottate precedentemente nel 1994 e nello stesso periodo dell’anno.
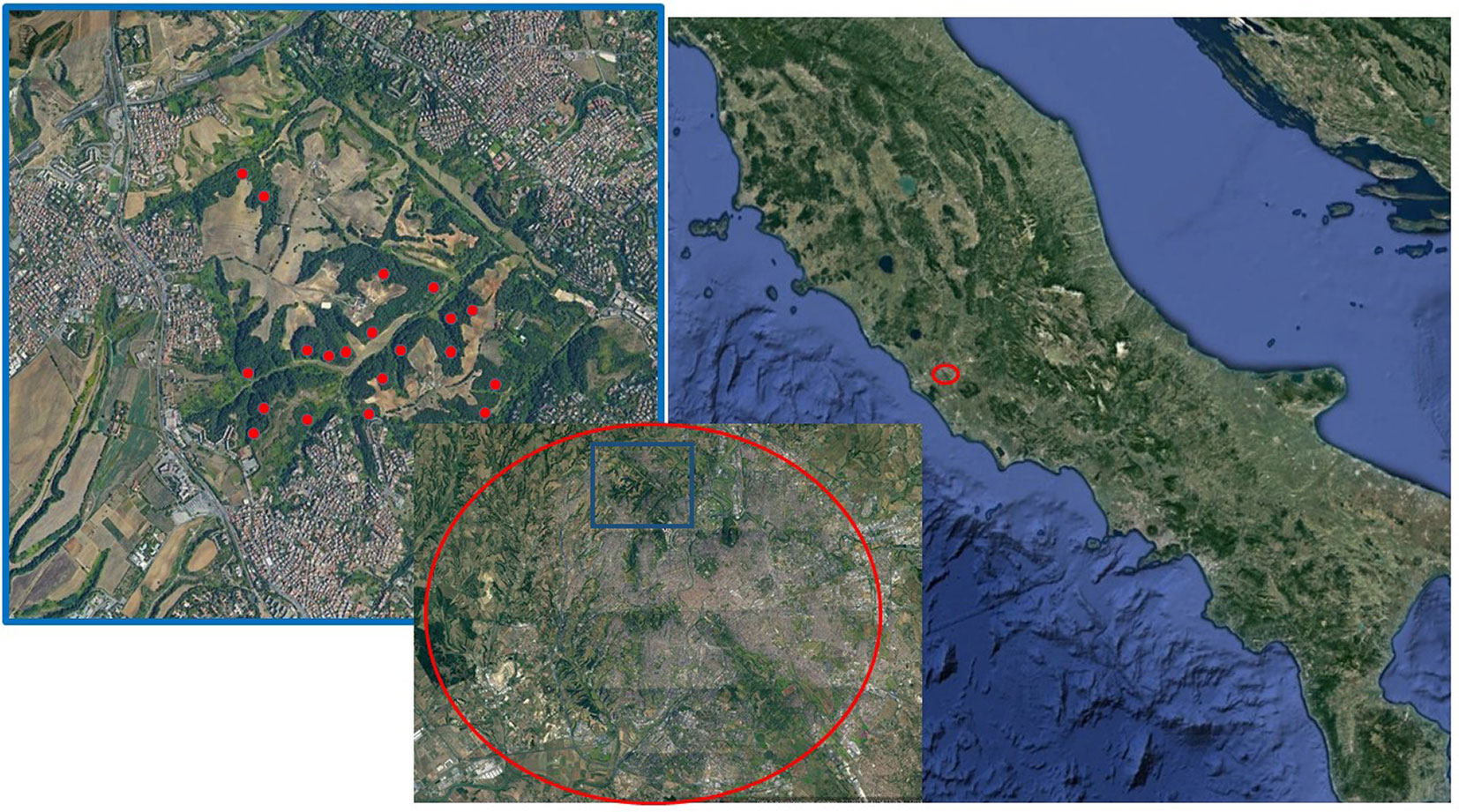
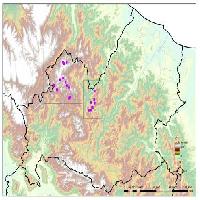
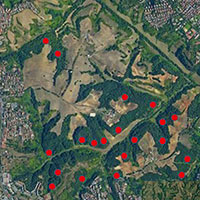
Va precisato che la posizione delle stazioni originali nel 1994, non esistendo all’epoca apparecchiature GPS commerciali per la rilevazione delle coordinate geografiche, era stata individuata di volta in volta semplicemente mediante analisi sul campo di stralci della Carta Tecnica Regionale con scala 1:10.000 e equidistanza 5 m. La posizione delle stazioni in cui sono stati eseguiti i rilievi nel 1994, e poi ripetuti con georeferenziazione nel 2015, è riportata nello stralcio cartografico in Fig. 1.
Fig. 1 - Localizzazione della Riserva Naturale Regionale dell’Insugherata e delle stazioni da 10×10 metri rilevate per la prima volta nel 1994 e successivamente nel 2015.
Nello specifico è stato utilizzato il metodo di rilievo floristico elaborato da Braun-Blanquet e modificato da Pignatti ([43]), per il quale alle specie campionate all’interno di un popolamento elementare, approssimativamente corrispondente ad una stazione di un quadrato di 10 metri di lato, vengono attribuiti indici di abbondanza-dominanza; successivamente ogni specie è stata assegnata alla relativa forma biologica di appartenenza (Ch: camerofite; G: geofite; H: emicriptofite; T: terofite).
Per accertare e quantificare l’alterazione degli habitat, prima e dopo l’ingresso del cinghiale nell’area, sono state analizzate, in modalità appaiata, le variazioni in diversi parametri/test, intesi come indicatori floristici, tra i rilievi del 1994 e quelli del 2015, pur essendo consapevoli che alcuni di questi non sono indipendenti tra loro. La “scomposizione” in diversi indicatori però favorisce un’analisi più precisa delle entità vegetazionali più impattate dalla presenza dei cinghiali e del danno alla conservazione della biodiversità. I parametri/test considerati sono:
(1) Abbondanza totale di specie vegetali e media (± errore standard, ES) della variazione percentuale di specie per stazione come parametro indicatore di impatto sulla ricchezza e diversità floristica.
(2) Numero totale e copertura (come somma delle coperture percentuali) di specie erbacee (Ch+G+H+T) e media (± ES) della variazione percentuale di specie erbacee per stazione, in quanto nell’arco di tempo considerato eventuali impatti sono più valutabili su specie con ciclo vitale breve, piuttosto che su specie arboree.
(3) Numero totale e copertura (come somma delle coperture percentuali) delle geofite (G) e media (± ES) della variazione percentuale di specie geofite per stazione, in quanto forma biologica particolarmente sensibile all’effetto del rooting del cinghiale in ambiente forestale.
(4) Presenza di specie appartenenti a gruppi sistematici sentinella e dalla valenza fortemente iconica quali le orchidee (specie censite nei rilievi: Limodorum abortivum, Ophrys fuciflora, Orchys provincialis).
(5) Presenza/assenza di specie erbacee di alto valore conservazionistico e biogeografico per la Riserva in quanto specie caratteristiche di associazione o di alleanza fitosociologiche, quali Drymochloa drymeia subsp. exaltata, caratteristica della suballeanza Doronico orientalis-Fagenion sylvaticae (Ubaldi, Zanotti, Puppi, Speranza & Corbetta ex Ubaldi 1995) e Ornithogalum pyrenaicum, specie caratteristica dell’associazione Aquifolio-Fagetum subass. carpinetosum betuli, oltre che dell’associazione Ornithogalo-pyrenaici Carpinetum.
(6) Numero totale di specie erbacee definite “localmente minacciate” rilevate nelle due campagne di rilievi, comprendenti: taxa localmente rari, cioè esclusivi dell’Insugherata o presenti a Roma in meno di 4 quadranti ([15]), rari nel Lazio ([5]) e tutelati ai sensi della L.R. 61/74.
(7) L’indice di similarità di Sørensen, espresso come media (± ES) per stazione, basato sui dati di presenza/assenza, utilizzato per misurare la somiglianza tra i due periodi come rapporto tra le specie condivise ed il numero di specie esclusive nel 1994 e nel 2015.
(8) Il test statistico ANOSIM (procedura non parametrica per gruppi di osservazioni multivariate che utilizza il rango delle distanze), con numero di permutazioni N= 9999 e distanza Bray-Curtis, è stato utilizzato (come in [12] per i cambiamenti di vegetazione in due diversi periodi) per verificare se le differenze fra i rilievi dei due periodi sono significative.
(9) Numero di specie aliene, come potenziale indice del livello di disturbo.
Disturbo del suolo in superficie
Durante ogni rilievo effettuato nell’anno 2015 è stato rilevato anche il valore della percentuale di superficie del rilievo interessata, all’atto del rilievo, da disturbo riconducibile all’attività di rooting del cinghiale. Non essendo nota, al tempo della prima campagna di rilievi, la presenza del cinghiale nell’area di studio, non venne previsto ovviamente il rilevamento dei relativi segni di scavo. Era tuttavia previsto, nella scheda di rilevamento, un campo per la stima e l’annotazione di eventuali forme di alterazione superficiale del suolo; non essendo mai stata esplicitamente annotata attività di rooting nei rilievi del 1994, questa si può ritenere nulla, come di fatto era la presenza del cinghiale.
Per ognuna delle 20 stazioni è stata investigata la relazione (attraverso la correlazione di Pearson) tra la percentuale di rooting in atto durante i rilievi del 2015 ed i cambiamenti nella vegetazione misurati attraverso la differenza 1994-2015 dei seguenti parametri/indicatori floristici (la numerazione segue quanto riportato nel precedente paragrafo “Flora”): 1-numero di specie; 3-numero di geofite; 7-indice di Sørensen. I dati sono stati anche aggregati in base all’esposizione prevalente in mesofili (con esposizione Nord, N=11 rilievi) e termofili (con esposizione Sud, N= 9 rilievi) al fine di evidenziare eventuali correlazioni statistiche con l’utilizzo trofico da parte dei cinghiali.
Risultati
Pressioni
Dagli archivi dell’Ente Gestore Riserva Naturale dell’Insugherata non risultano incendi boschivi nel periodo preso in considerazione. In particolare la consultazione del database degli incendi boschivi, disponibile on-line sul sito ArcGis Online, aggiornato a partire dal 2007, e del Catasto delle aree percorse dal fuoco rilevate dal CFS sul comune di Roma dal 2004, ha consentito di accertare l’assenza di eventi nell’area di studio fino a tutto il 2015. Il pascolo degli animali allevati, peraltro non praticabile nelle superfici boscate oggetto della presente indagine, ha registrato solo un progressivo calo nella Riserva. La superficie agricola è rimasta simile, ancorché limitatamente variabile in funzione delle normali rotazioni colturali. Viceversa, la presenza di animali selvatici erbivori, quale il cinghiale, le cui prime segnalazioni nel territorio della Riserva risalgono al 2000 per divenire rilevanti dal 2008 ([3]), è aumentata esponenzialmente ed al momento la sua presenza può essere considerata “problematica” e con una popolazione in crescita ([44], [2]); in particolare il Piano di gestione del cinghiale all’interno della Riserva dell’Insugherata, recentemente approvato, ha evidenziato segni di presenza in tutto il territorio e un costante aumento delle segnalazioni dei cittadini dal 2009 al 2019 ([3]); non è stato possibile, però, reperire nessuna stima della densità del cinghiale nell’area.
Flora
Nella Tab. 1 sono riassunti i risultati per i diversi parametri analizzati.
Tab. 1 - Per parametro/test sono mostrati i risultati per dati aggregati (complessivi) e la media (± errore standard) per stazione (deviazione standard in parentesi). La numerazione si riferisce all’ordine dei parametri/test riportati nel testo (paragrafo “Flora”). I risultati si riferiscono alle 20 stazioni rilevate nel 1994 e nel 2015.
| No | Parametro / Test | Differenza % complessiva |
Variazione % media per stazione |
|---|---|---|---|
| 1 | Tutte le specie | -15.8 | -14.2 ± 5.9 (26.8) |
| 2 | Erbacee | -20.9 | -19.9 ± 8.4 (26.0) |
| 3 | Geofite | -23 | -15.1 ± 7.9 (23.2) |
| 4 | Orchidee | -100 | - |
| 5 | Alto valore conservazionistico/biogeografico | -50 | - |
| 6 | Localmente minacciate | -26 | - |
| 7 | Indice Sørensen | 0.59 ± 0.03 (0.12) | |
| 8 | Test ANOSIM | R value= 0.069; p(same)=0.0474 | |
| 9 | Specie aliene | Nessuna specie riportata nei due periodi |
|
(1) Il numero complessivo di specie rilevate ammontava a 133 nei rilievi nel 1994 ed è sceso a 112 nel 2015, determinando una riduzione di entità pari al 15.8%. Il numero medio di specie per stazione è invece passato da 36.3 nei rilievi del 1994 a 29.7 del 2015. Per ogni stazione c’è stata una diminuzione media pari al 14.2 ± 5.9%.
(2) Il numero complessivo di specie erbacee è passato da 91 a 72 con una riduzione pari al 20.9%, mentre l’incidenza delle specie erbacee sul totale è passata dal 68.4% del 1994 al 64.3% del 2015. Relativamente alla somma delle coperture totali, la riduzione è stata del 6.5%. I gruppi di rilievi ad esposizione N e S hanno registrato differenze consistenti: nei primi il numero delle erbacee totali è passato da 61 a 56 (-8.2%), mentre nei secondi è passato da 69 a 48 (-30.4%). Per ogni stazione c’è stata una diminuzione media pari al 19.9 ± 8.4%.
(3) Il numero complessivo di specie geofite è passato da 31 specie nel 1994 a 24 specie nel 2015, con una riduzione pari a circa il 22.6%. L’incidenza delle geofite (G) sullo spettro biologico totale è invece passata dal 23.3% al 21.4%. La copertura totale relativa alle geofite si è complessivamente ridotta del 29.7%. Non si sono riscontrate sostanziali differenze tra rilievi ad esposizione N e S: nei primi le geofite sono passate da 27 a 21 specie totali (-22%), nei secondi sono passate da 18 a 13 (-28%). Per ogni stazione c’è stata una diminuzione media pari al 15.1 ± 7.9%.
(4) Delle tre specie di orchidee presenti nei rilievi nel 1994 nessuna è stata ritrovata nei rilievi del 2015.
(5) Drymochloa drymeia subsp. exaltata è stata ritrovata nella stazione originale anche se con una copertura minore nel 2015 (valore +, inferiore all’1% di copertura) rispetto al 1994 (valore 1 pari a circa 10% di copertura). Ornithogalum pyrenaicum, presente in 3 delle 20 stazioni nel 1994 (con valore +) non è stata ritrovata nei rilievi del 2015.
(6) Il numero totale di specie “localmente minacciate” è passato dalle 19 rinvenute nei rilievi del 1994 alle 14 censite in quelli del 2015, con una riduzione del 26.3%.
(7) L’indice di similarità di Sørensen ha riportato un valore pari a 0.59 ± 0.03 con un valore minimo di 0.27 ed un valore massimo di 0.78.
(8) Il test statistico ANOSIM ha confermato quanto evidenziato dagli altri parametri, rivelando differenze significative nella vegetazione tra i vecchi ed i nuovi rilievi (R value= 0.0694; p(same)=0.04745).
(9) Nessuna specie aliena è stata trovata all’interno delle stazioni nei due diversi campionamenti.
Disturbo del suolo
Nelle stazioni di rilevamento del 1994 non vi era presenza di disturbo del suolo, mentre nel 2015, 19 stazioni su 20 mostravano evidenza di alterazione del suolo. Nelle stazioni esposte a nord il valore percentuale medio di disturbo del suolo è pari al 17.0 ± 5.2% della superficie rilevata, mentre nelle stazioni esposte a sud è pari al 7.0 ± 1.2%. Non sono state evidenziate relazioni statistiche significative tra percentuale di disturbo del suolo (rooting) rilevata nel 2015 e cambiamenti di vegetazione per stazione.
Discussione
Nell’area romana, come in tutto il Lazio ed in linea con il trend osservato in tutta la penisola italiana, il numero di individui di cinghiale è enormemente aumentato a partire dagli anni 2000 ([4]) ed è tuttora in progressivo incremento, determinando localmente condizioni di vere e proprie “invasioni” anche in ambiti urbani e peri-urbani, di difficile gestione e con il rischio potenziale di impatto sugli ecosistemi forestali ([21]).
La flora è un ottimo indicatore dell’impatto del rooting dei cinghiali; dai nostri rilievi è emerso come ci sia stata una sostanziale diminuzione di specie vegetali (oltre il 15%) nell’arco temporale considerato. Il parametro si riferisce alle aree di rilievo, risultando comunque un indicatore pertinente degli impatti su tutta la Riserva Naturale dell’Insugherata. Deve comunque essere messo in evidenza che le conclusioni ottenute sono limitate dall’assenza di una valutazione sincronica degli impatti dovuta alla mancanza di dati provenienti da aree di controllo, cioè recintate e precluse ai cinghiali. Similarmente, le conclusioni potrebbero essere limitate poiché non sono state messe in relazione con variazioni climatiche in corso, data la ridotta finestra temporale considerata.
Anche gli altri indicatori utilizzati per valutare l’impatto, tutti relativi alla flora e quindi parzialmente dipendenti tra loro, hanno evidenziato alterazioni a carico dell’ambiente. In particolare, le specie erbacee sono diminuite, in numero, di oltre il 20%. Le specie erbacee sono un ottimo indicatore dell’alterazione dell’habitat. A differenza delle fanerogame, infatti, il loro ciclo vitale breve fa sì che in caso di disturbo (non distruttivo come può essere quello, ad esempio, di un incendio), in una finestra temporale relativamente breve, il rinnovamento delle specie possa essere a rischio. In ambiente urbano e periurbano le forme biologiche possono essere utilizzate come indicatori ecologici come già dimostrato in uno studio realizzato nella stessa città ([25]). Diverso il caso di finestre temporali di lungo termine (>50 anni) dove il ciclo di vita di alberi ed arbusti (e la loro relativa biomassa) possono essere indicatori di cambiamenti legati a fattori ecologici ([27]).
In presenza di intensa e prolungata pressione da rooting, le geofite sono le specie più a rischio di depauperamento ([36]). Il nostro studio conferma tale relazione, evidenziando come le specie appartenenti a questa forma abbiano subìto un forte impatto, testimoniato da una riduzione del numero di specie pari a circa il 23%, senza significative differenze tra stazioni mesofile e termofile. Analogo andamento ha mostrato la copertura totale delle geofite, ridottasi complessivamente del 30% circa. In generale, però, la diminuzione non è stata costante in tutte le stazioni.
Negli studi di Burrascano et al. ([10], [11]) è emerso come, analizzando sincronicamente aree sottoposte a diversi livelli di rooting, la presenza di cinghiali determini grandi differenze nella composizione ed abbondanza delle specie nello strato erbaceo di boschi mediterranei. Similmente, uno studio in faggete in Svizzera ha evidenziato come in presenza di cinghiali la copertura vegetale ed il numero di individui di piante diminuiscano rispetto ad aree dove l’accesso agli animali è precluso ([50]). Analogamente, in tutt’altro ecosistema (praterie alpine sui Pirenei), Bueno et al. ([9]) evidenziano come il rooting dei cinghiali è particolarmente manifesto in aree protette e su suoli profondi che possono provvedere a fornire cibo quale rizomi, bulbi e invertebrati. Nel particolare, il nostro studio ha anche evidenziato come i cambiamenti a carico della vegetazione non possano essere messi in relazione con il rooting attualmente in atto, suggerendo come sia il continuo perdurare di danneggiamenti della componente erbacea reiterati nel tempo a portare al depauperamento della flora, favorendo inizialmente le re-seeders (terofite) rispetto alle re-sprouters (cioè con ripresa da gemme dopo disturbo); il rapporto tra queste categorie ecologiche in presenza di fattori di disturbo, anche se rovesciato, è già ampiamente studiato nel ciclo degli incendi ([34], [17]) dove a bassa frequenza di impatto solo le re-sprouters resistono mentre ad alta frequenza anche queste vengono danneggiate. Questo trend di depauperamento nella Riserva dell’Insugherata è evidenziato dal valore della somma delle coperture relative alle geofite rispetto a quella aggregata di tutte le specie erbacee.
La presenza dei cinghiali, con la loro caratteristica mobilità e la cui diffusione è funzione principalmente della risorsa alimentare, costituisce un elevato fattore di disturbo per il suolo in quanto: (i) ne altera sia la struttura fisica che la composizione chimica ([37]); (ii) causa cambiamenti nella struttura dell’humus ([22]) e del ciclo di mineralizzazione di C ed N nel suolo ([50]). Nei nostri rilievi il disturbo medio del suolo per rilievo è risultato all’incirca del 13%, ma è stato anche evidenziato come nelle cenosi mesofile esposte a nord il disturbo del suolo sia maggiore rispetto a quelle termofile esposte a sud, come già osservato per le foreste decidue boreali in Svezia ([48]).
Nei rilievi replicati nel 2015, purtroppo, è emersa l’assenza delle 3 specie di orchidee rinvenute nello studio del 1994, configurando oltre che una grave perdita in termini di biodiversità (nessuna delle 3 specie a Roma ha una diffusione superiore a 4 quadranti dell’Atlante della Flora - [15], e una, Orchis provincialis, è esclusiva dell’Insugherata), anche un notevole impoverimento in termini di attrattività dell’area, dato il valore anche estetico ed evocativo delle specie. La scomparsa delle orchidee, in generale, è indicatore di un peggioramento ecologico dell’habitat ([8]). L’impatto sulle orchidee è stato anche riportato in uno studio in zone umide in Spagna dove a seguito dei corridoi ecologici della rete Natura2000 la densità dei cinghiali è aumentata ([40]).
L’abbondanza di Drymochloa drymeia subsp. exaltata è diminuita, anche se in maniera poco significativa, nei rilievi più recenti, mentre non è stato ritrovato Ornithogalum pyrenaicum. Dal punto di vista conservazionistico, l’impatto su queste due specie indicatrici delle peculiarità ecologiche e biogeografiche delle formazioni studiate, rappresenta un grosso danno per la tutela dell’integrità ambientale della Riserva. Analoga considerazione deve essere fatta per le specie “localmente minacciate” o localmente rare, la cui conservazione dovrebbe essere uno degli obiettivi primari della Riserva. Si sono ridotte, come numero totale di specie, da 19 a 14, con una riduzione pari al 26.3% e se il trend fosse esteso a tutta la Riserva, si avrebbe un’ulteriore prova di come una elevata densità di cinghiali, in assenza di fattori o azioni in grado di limitarla, metta di fatto a rischio la conservazione delle specie vegetali e, presumibilmente, anche le finalità istituzionali dell’Area Protetta.
Anche l’indice di similarità di Sorensen evidenzia come ci sia stato un turnover di specie, o meglio un replacement di specie, pari a circa il 40 % (complemento a 1 dell’indice di Sorensen o indice di dissimilarità di Sorensen), dato confermato dal test ANOSIM che ha evidenziato differenze statisticamente significative tra le specie presenti nei vecchi e i nuovi rilievi.
Infine, la presenza di cinghiali non è stata accompagnata, nei rilievi, dall’ingressione di specie esotiche; il fatto, per quanto importante dal punto di vista della dinamica degli habitat alterati non deve, però, stupire più di tanto. Nella scelta dei rilievi nel 1994, infatti, le aree di indagine erano state individuate all’interno di formazioni boschive non impattate. Nonostante l’attuale presenza dei cinghiali, le stazioni scelte per i rilievi della flora presentano una buona struttura vegetale (la media di 30 specie per quadrato è elevata rispetto alla media delle aree circostanti - [1]) e sono sufficientemente distanti da zone con presenza di specie aliene che possano funzionare da potenziali source. Considerando che affinché un ambiente possa venire colonizzato da specie vegetali non indigene devono coesistere simultaneamente presenza di germoplasma “esotico” e un ambiente alterato che favorisca il rinnovamento della specie più aggressiva ([19]), si comprende come di per sé l’assenza di specie non indigene non possa essere sempre indice di integrità ambientale.
Conclusioni
Lo studio si basa sul confronto di rilievi floristici realizzati nelle stesse stazioni a distanza di oltre 20 anni. In questa finestra temporale l’unica sostanziale variazione di pressione nota incorsa nell’ecosistema forestale urbano della Riserva Naturale Regionale dell’Insugherata è stata l’ingressione, attraverso corridoi ecologici da aree verdi circostanti, del cinghiale (Sus scrofa), che a partire dal 2000 circa è progressivamente proliferato nella Riserva. Lo studio ha evidenziato un impoverimento nella vegetazione, in particolare a carico specie dello strato erbaceo e, tra queste, delle geofite, che, pur in assenza di uno studio specifico causa-effetto, può essere ragionevolmente ricondotto alla presenza continuativa della popolazione di cinghiale nell’area. Da sottolineare la specifica vulnerabilità all’azione trofica del cinghiale, tra le geofite, delle orchidee (anche se le specie con bulbo-tubero presentano una fenologia intermedia tra geofite e emicriptofite).
Da quanto detto si evidenzia l’urgenza dell’attuazione di forme di gestione della presenza dei cinghiali all’interno della Riserva Naturale dell’Insugherata, al fine di ridurne l’impatto sulle biocenosi naturali di fatto meno resilienti ai disturbi a causa delle dimensioni dell’area e della frammentazioni degli habitat. La pressione dei cinghiali, infatti, è potenzialmente in grado di causare perdite nette di biodiversità e conseguenti alterazioni nella struttura funzionale delle comunità ecologiche presenti.
Ringraziamenti
Per il presente lavoro si ringrazia l’Ente RomaNatura, in particolare il guardiaparco Fabrizio Foschi per i dati relativi agli incendi boschivi, il prof. Sandro Pignatti che ha curato la supervisione dei rilievi nel 1994, il Dott. Andrea Monaco per preziosi consigli sul testo. L’utilizzo dell’indice di Sorensen è stato approfondito sul gruppo facebook “ecologia-statistica” amministrato dal Dott. Stefano Giustino e calcolato con il softwarePAST - Paleontological statistics ([30]). Si ringrazia il Dott. Maurizio Cutini per i consigli sugli studi ecologici di lungo termine.
References
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Online | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar