Towards the establishment of the Italian network of old-growth forests: the understorey plant diversity perspective
Forest@ - Journal of Silviculture and Forest Ecology, Volume 19, Pages 63-66 (2022)
doi: https://doi.org/10.3832/efor4142-019
Published: Jun 16, 2022 - Copyright © 2022 SISEF
Commentaries & Perspectives
Abstract
The publication of the Decree that has established the Italian network of old-growth forests opens new opportunities for nature conservation and new challenges for scientists. A fundamental criterion for the identification of old-growth forests is related to a “characteristic biodiversity” due to the absence of disturbances for at least sixty years. In this contribution we mainly discuss shortcomings, potential interpretation and perspectives related to the application of this criterion for the vascular plants living in the understorey. We show that the understorey diversity (both taxonomic and functional) patterns with forest maturity are strongly context-dependent and stand structural features are fundamental drivers. As a consequence, considering the impressive heterogeneity of Italian forests, the strict threshold included in the Decree (sixty years since the last disturbance) can hardly be used to distinguish a “characteristic biodiversity”. Finally, we invite all the Italian scientists dealing with forest ecosystems to strongly collaborate in order to accept the challenge introduced by the Decree.
Keywords
Forest Policy, Forest Specialist Species, Functional Diversity, Plant Diversity, Species Richness
Uno sguardo verso il basso, verso il sottobosco
Con l’approvazione del Decreto del 18 novembre 2021 “Linee guida per l’identificazione delle aree definibili come boschi vetusti” e la relativa creazione della Rete Nazionale dei Boschi Vetusti (art.7 comma 13-bis del decreto legislativo 3 aprile 2018, n. 34; “Testo unico in materia di foreste e filiere forestali” - TUFF) si apre una fase nuova nella conservazione della biodiversità forestale in Italia.
Le linee guida stabiliscono i seguenti criteri per l’identificazione dei boschi vetusti: (i) superficie di almeno 10 ha; (ii) la presenza di specie autoctone spontanee coerenti con il contesto biogeografico; (iii) una biodiversità caratteristica conseguente all’assenza di disturbi da almeno sessanta anni; (iv) la presenza di stadi seriali legati alla rigenerazione e alla senescenza spontanee.
È evidente come la grande opportunità fornita dal Decreto rappresenti anche una sfida, non solo amministrativa e gestionale (le Regioni sono infatti chiamate a stabilire gli iter per il riconoscimento dei boschi vetusti che successivamente dovranno essere oggetto di monitoraggio) ma soprattutto scientifica, chiamando forestali, ecologi, zoologi e botanici ad una nuova fase di collaborazione al di fuori della rigida logica dei settori scientifici e della “nicchia” di riferimento.
La recente rassegna di Motta et al. ([16]) sullo stato dell’arte della ricerca Italiana nel settore evidenzia una notevole produzione scientifica, ma allo stesso tempo rende note una serie di carenze di informazioni che il mondo scientifico italiano è chiamato a colmare nel prossimo futuro per rispondere alle esigenze del Decreto, ad esempio lo scarso utilizzo di parametri strutturali quantitativi, così come la limitata integrazione tra approcci che mettano in relazione struttura forestale e biodiversità.
In questo contributo poniamo l’attenzione sulla diversità vegetale, con particolare riferimento alle specie vascolari presenti nel sottobosco. Queste, pur rappresentando meno del 1% della biomassa forestale, possono costituire oltre il 90% della diversità vegetale e contribuire fino al 20% alla produzione della lettiera ([13]). Il contributo della diversità vegetale del sottobosco è ancora più evidente se consideriamo le faggete del territorio Italiano che comprendono il maggior numero di siti con carattere di vetustà e che sono spesso caratterizzate da uno strato arboreo dominante monospecifico ([16]). In tali condizioni, è quindi evidente come la declinazione vegetale di alcuni tra i criteri indispensabili per il riconoscimento di un bosco vetusto, ossia la presenza di specie autoctone e di una “biodiversità caratteristica” (Decreto 18/11/2021) conseguente all’assenza di disturbi da almeno sessanta anni, debba necessariamente tenere conto della diversità vegetale presente nel sottobosco (il cosiddetto understorey), e non solo dello strato arboreo.
Per il primo criterio sopra citato, esistono validi ed aggiornati strumenti a supporto dell’identificazione delle specie autoctone spontanee coerenti con il contesto biogeografico (si vedano ad esempio le check-list delle specie autoctone e aliene d’Italia, con indicazione delle presenze per ciascuna regione amministrativa - [3], [12]). In merito al secondo criterio, riteniamo che l’attuale produzione scientifica non sia sufficiente per fornire dei chiari riferimenti concretamente applicabili. Con questo articolo ci poniamo quindi l’obiettivo di stimolare riflessioni e fornire suggerimenti per orientare la ricerca in merito all’individuazione dei boschi vetusti sulla base del Decreto del 18 novembre 2021.
Sulla “biodiversità caratteristica” e altri luoghi comuni
Il titolo di questo capitolo è volutamente provocatorio per evidenziare come la giustificata e naturale tendenza alla semplificazione e alla generalizzazione non deve distrarci dalla consapevolezza di avere di fronte ai nostri occhi ecosistemi estremamente complessi, dove molteplici componenti interagiscono a scale spaziali e temporali differenti. Non solo, tali interazioni, che danno luogo ai cosiddetti pattern, possono (e molto spesso sono) strettamente dipendenti dal contesto, sia esso rappresentato dalla biogeografia, dalle condizioni edafiche, dalle pratiche selvicolturali attuali e passate, ecc.
Declinare questa complessità rispetto alle esigenze di una norma che per sua natura è rigida (indica cioè un limite temporale ben definito, ossia 60 anni, non 50 o 70!), crediamo rappresenti una sfida interessante che il mondo scientifico che studia gli ecosistemi forestali dovrà cogliere.
Cosa si intende per “biodiversità caratteristica” conseguente all’assenza di disturbi da almeno sessanta anni? È possibile individuarla?
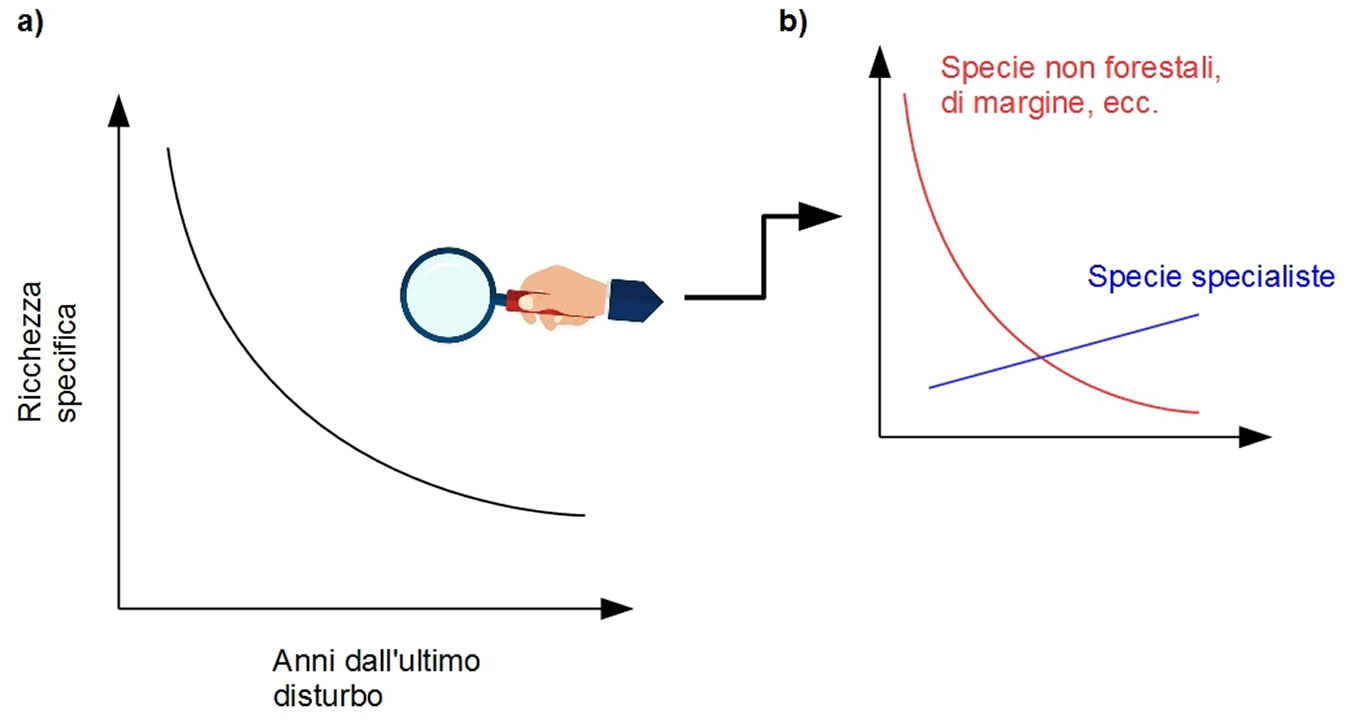
Focalizzandoci sulle specie vegetali del sottobosco e ragionando in termini di ricchezza specifica (una delle misure della diversità biologica), la “biodiversità caratteristica” dopo molti decenni dall’ultimo disturbo sarebbe rappresentata da un numero relativamente ridotto di specie, molto più basso rispetto alle fasi più prossime al disturbo. Un bosco vetusto può annoverare anche solo 15-20 specie vegetali rispetto ad un bosco oggetto di recenti interventi selvicolturali che può ospitare ben oltre le 100 specie (Fig. 1a - [1]). La minore ricchezza specifica dei boschi maturi è una delle motivazioni che spesso - in maniera a dir poco superficiale - viene richiamata per sostenere la tesi di un incremento dei tagli, sia in termini di estensione che di intensità.
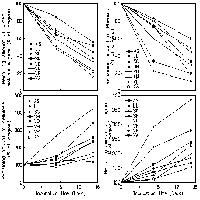
Fig. 1 - Quadro interpretativo della variazione della ricchezza di specie (a) e delle varie componenti individuate sulla base della preferenza di habitat (b) in funzione dell’età dall’ultimo disturbo. Lo schema concettuale si basa sui risultati ricavati da Bartha et al. ([1]) e Cervellini et al. ([9]).
Per comprendere più a fondo questo pattern di riduzione del numero delle specie verso fasi più mature del bosco, la ricchezza specifica può essere suddivisa in varie componenti (Fig. 1b), comprendenti ad esempio le specie specialiste di un determinato habitat forestale, le specie generaliste adattate a vivere in molteplici habitat forestali e le specie non forestali o di margine. Tali componenti riflettono diverse esigenze ecologiche e potrebbero quindi fornire un supporto per definire la “biodiversità caratteristica” dei boschi vetusti e a cascata anche gli obiettivi da porsi in termini di conservazione della stessa. Il risultato sarebbe molto probabilmente quello di una netta riduzione della componente delle specie non forestali e di margine e di un aumento delle specialiste di foresta, come già dimostrato da vari articoli ([1], [9] - Fig. 1b).
L’utilità di questo approccio per la definizione della “biodiversità caratteristica” dopo 60 anni dall’ultimo disturbo presenta però delle limitazioni rilevanti. Innanzitutto la classificazione delle specie sulla base della preferenza di habitat è un esercizio che dipende dal contesto ecologico di riferimento (una specie specialista di faggeta in Aspromonte può benissimo essere una specie di margine nelle faggete pre-Alpine), evidenziando quindi la necessità di approfondite conoscenze botaniche locali (si vedano i lavori svolti a partire da [15] fino ad [14]). In secondo luogo, le tendenze sono - ancora una volta - dipendenti dal contesto e, oltre che dagli anni dall’ultimo disturbo, dipendono dai cambiamenti e dalle dinamiche della struttura arborea che a loro volta influenzano la disponibilità delle risorse (luce, acqua, nutrienti) nel tempo e nello spazio. Non è quindi propriamente - o almeno non esclusivamente - l’età dall’ultimo disturbo a definire la biodiversità di una determinata foresta. Per essere ancora più chiari, una faggeta appenninica di 60 anni su substrato calcareo, caratterizzata da una esposizione a sud ed elevata inclinazione avrà molti meno caratteri di vetustà di una faggeta di 60 anni localizzata nella stessa area ma su substrato arenaceo con esposizione nord e scarsa inclinazione. Un valido approccio per ovviare ai problemi sopra citati potrebbe essere quello di comparare foreste relativamente omogenee dal punto di vista biogeografico, edafico, della storia gestionale, ecc. (si vedano i confronti tra foreste gestite e vetuste in [6]): in tal caso emergerebbero più facilmente indicazioni utili a rispondere al criterio stabilito dal decreto (ad esempio, valori soglia), senza però avere l’ambizione di generalizzare i risultati ottenuti.
Infine, crediamo sia importante porre l’attenzione su un ulteriore aspetto: la scala spaziale di riferimento, un fattore determinante in ecologia. Tutte le relazioni che osserviamo devono essere riferite ad una determinata scala spaziale; a scale diverse possono essere riscontrate risposte diverse di un medesimo oggetto d’indagine. Ciò è vero anche riguardo le specie specialiste di un dato habitat: il loro aumento lungo il gradiente di maturità della foresta osservato a scala di stand, potrebbe non avere riscontri a scale spaziali diverse. Studi a scala di paesaggio ([8]) o a scala molto fine (all’interno dello stand - [2]) evidenziano infatti risultati contrastanti. Questa consapevolezza non deve ulteriormente abbatterci rispetto alla difficoltà di ragionare su una “biodiversità caratteristica”, ma piuttosto stimolare una domanda ulteriore: a che scala valutiamo la biodiversità caratteristica conseguente all’assenza di disturbi da almeno sessanta anni?
Dalle specie alle funzioni
Nella continua ricerca di modelli generalizzabili e di fronte alle sfide dei cambiamenti globali, l’ecologia si è recentemente posta il problema di comparare ecosistemi costituiti da specie diverse. La soluzione è stata spesso quella di slegarsi dall’identità delle specie per ragionare in termini di funzioni (rappresentate dai caratteri funzionali), come ad esempio l’acquisizione e la conservazione delle risorse. Due specie completamente distanti dal punto di vista tassonomico possono svolgere la medesima funzione e, viceversa, specie appartenenti allo stesso genere possono avere funzionalità diametralmente opposte.
L’approccio funzionale può quindi fornire un supporto rispetto alla problematica in oggetto, fornendoci un quadro di riferimento più generalizzabile ai diversi contesti forestali. Occorre però riconoscere come lo stato delle conoscenze settoriali in Italia sia alquanto ridotto: i lavori che trattano di variazioni nella diversità funzionale vegetale sono pochi e non in grado di coprire l’eterogeneità che caratterizza gli ecosistemi forestali nazionali.
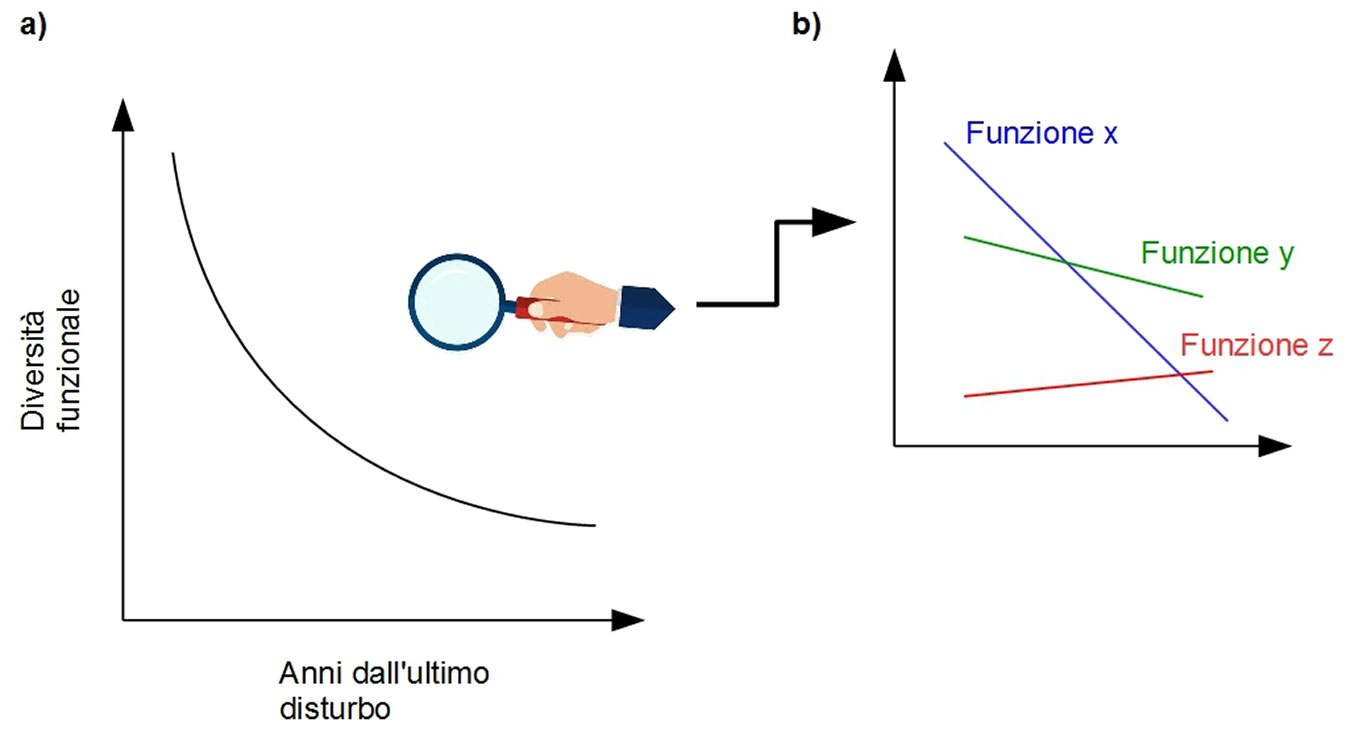
Riferendosi al gradiente in oggetto, ossia gli anni dall’ultimo disturbo, la letteratura scientifica disponibile indica una tendenza alla riduzione della diversità funzionale del sottobosco con la progressiva maturità della foresta ([17], [11]). Ciò è spiegato dal progressivo cambiamento di determinate condizioni ambientali che agiscono come un filtro rispetto alle possibili strategie funzionali attuabili dalle piante (Fig. 2a). Anche in questo caso, come nel caso della ricchezza specifica, scomporre la tendenza generale in varie componenti rappresenta un esercizio estremamente utile. Passando quindi dalla multifunzionalità espressa dalle varie specie, ai singoli caratteri funzionali (e quindi alle singole funzioni), si scopre come le variazioni siano funzione-dipendenti (Fig. 2b).
Fig. 2 - Quadro interpretativo della variazione della diversità funzionale del sottobosco, (a) comprendendo tutte le funzioni e (b) scomponendo i vari caratteri e le rispettive funzioni, rispetto agli anni dall’ultimo disturbo. Lo schema concettuale si basa sui risultati ricavati da Ottaviani et al. ([17]), Della Longa et al. ([11]), Chelli et al. ([10]).
È comunque evidente come non sia di per sé l’età dall’ultimo disturbo a determinare diversi livelli di diversità funzionale. Anche qui, un ruolo fondamentale è dato dalla struttura forestale che impatta sulla quantità ed eterogeneità delle risorse disponibili nel sottobosco influenzando diversamente le varie funzioni che compongono la diversità funzionale complessiva ([4], [10]). Emerge quindi, ad esempio, che la quantità di legno morto così come la presenza di alberi di grandi dimensioni - elementi questi direttamente o indirettamente dipendenti dalle pratiche gestionali locali e non solo dall’età della foresta ([9]) - possano influenzare la diversità funzionale e, nel caso specifico, aumentarla ([10]).
Verso una visione d’insieme dell’ecosistema-foresta
Per la diversità vegetale (sia essa intesa in senso tassonomico o funzionale) non esistono strumenti diagnostici oggettivi e generalizzabili in grado di permetterci di individuare una “biodiversità caratteristica” conseguente all’assenza di disturbi da almeno sessanta anni. L’ecologia raramente prevede separazioni nette, basandosi essenzialmente su tendenze continue, la cui “inclinazione” è strettamente dipendente dall’ecosistema osservato, dal contesto di riferimento (biogeografico, edafico, gestionale, ecc.) e dalla scala spaziale. Certamente non è l’età di un bosco (intesa come tempo trascorso dall’ultimo disturbo), o almeno non solo l’età, a determinare un certo “livello” di biodiversità. Questa constatazione rappresenta il principale limite all’applicazione del principio della “biodiversità caratteristica” previsto dal decreto del 18 novembre 2021. Nel migliore dei casi, l’età può essere considerata un proxy di una numerosa serie di fattori che agiscono direttamente o indirettamente nell’influenzare la biodiversità del sottobosco. A livello locale, tali fattori sono essenzialmente legati alla struttura forestale (tra i principali: altezza, densità degli alberi, presenza di alberi di grandi dimensioni, copertura e stratificazione delle chiome, quantità e tipologia di legno morto - [5], [10]) che a sua volta determina la disponibilità e l’eterogeneità spazio-temporale delle risorse al suolo. Se è quindi vero che il forestale avrà bisogno del botanico per determinare la biodiversità (vegetale) di un bosco, è altrettanto vero che il botanico avrà bisogno del forestale per individuare i fattori che condizionano tale diversità. Questo esempio di interdipendenza va necessariamente ampliato anche alle discipline che si occupano delle altre componenti della biodiversità forestale (si vedano i validi tentativi di [18], [7]).
Infine, rispetto al concetto di “biodiversità caratteristica” siamo dispiaciuti di non aver proposto soluzioni concrete, anzi, probabilmente questo articolo ha posto più domande che soluzioni. Ma non è forse attraverso le domande che la scienza progredisce?
References
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar
CrossRef | Google Scholar